Clear Sky Science · pt
Hiperpolarização da membrana interna induzida por peptídeos antimicrobianos está associada à sensibilização a antibióticos e à atenuação da escalada de CIM em patógenos Gram‑negativos multirresistentes
Por que esta pesquisa importa para a saúde cotidiana
Infecções letais estão cada vez mais difíceis de tratar à medida que bactérias aprendem a resistir aos nossos antibióticos mais potentes. Este estudo explora uma nova maneira de ajudar medicamentos existentes a voltar a funcionar, acrescentando uma pequena molécula de inspiração natural chamada peptídeo. O trabalho sugere que talvez não precisemos de antibióticos totalmente novos para cada ameaça; em vez disso, podemos “turboalimentar” os que já temos, ao mesmo tempo em que acalmamos a inflamação descontrolada que torna a sepse tão perigosa.
Uma molécula auxiliar para antibióticos em dificuldades
Os pesquisadores concentraram‑se em uma molécula modificada derivada de peixe chamada TP2‑5, um peptídeo com carga positiva que, por si só, pode matar algumas bactérias. Eles investigaram se usar quantidades muito pequenas desse peptídeo juntamente com antibióticos padrão poderia tornar germes multirresistentes mais fáceis de tratar. Trabalhando com cepas problemáticas de bactérias Gram‑negativas, como Escherichia coli resistente a drogas e Acinetobacter baumannii, descobriram que adicionar apenas um quarto da dose mínima de TP2‑5 necessária para inibir o crescimento permitiu que vários antibióticos diferentes — incluindo meropenem, colistina, ciprofloxacino e até a vancomicina, geralmente ineficaz — funcionassem muito melhor. Em testes de laboratório, combinações que usavam doses fracas de ambos os fármacos juntas puderam eliminar completamente bactérias que nenhum dos dois conseguia controlar sozinho.
Impedindo que a resistência cresça tão rápido
A resistência a antibióticos geralmente piora com o tempo quando as bactérias são expostas repetidamente a um medicamento. Para simular esse processo, a equipe cultivou E. coli resistente por três semanas sob exposição diária a antibióticos isolados, TP2‑5 isolado ou antibióticos mais TP2‑5 em baixa dose. Quando os antibióticos foram usados sozinhos, a quantidade necessária para interromper o crescimento bacteriano aumentou dramaticamente — até 128 vezes para alguns fármacos — sinalizando nova resistência forte. Quando os mesmos antibióticos foram combinados com TP2‑5, essa escalada foi muito mais branda, sugerindo que o peptídeo auxiliar pode desacelerar a capacidade de adaptação das bactérias. Enquanto isso, bactérias expostas apenas ao TP2‑5 mostraram pouca mudança em sua sensibilidade ao peptídeo, indicando que pode ser mais difícil para elas desenvolverem defesas fortes contra esse tipo de ataque que mira a membrana.
Como o peptídeo remodela a casca bacteriana
Para entender por que o TP2‑5 potencializa o efeito dos antibióticos, os cientistas examinaram a camada externa das bactérias Gram‑negativas, que atua tanto como armadura quanto como porteira. Usando corantes químicos que brilham quando membranas vazam ou mudam de voltagem, junto com criotomografia eletrônica que imagina células congeladas em três dimensões, mostraram que doses muito baixas e não letais de TP2‑5 afinam e perfuram sutilmente a camada externa enquanto deixam a membrana interna em um estado incomum de alta energia ou “hiperpolarizada”. Em doses mais altas, o mesmo peptídeo rasga as membranas. Experimentos de temporização revelaram que quando as bactérias são primeiro colocadas nesse estado hiperpolarizado e levemente permeável pelo TP2‑5, a exposição subsequente a antibióticos faz com que a membrana interna entre em colapso rapidamente e mate as células. O peptídeo prefere ligar‑se a componentes negativamente carregados chamados lipopolissacarídeos e a fosfolipídios específicos, abundantes nos envelopes Gram‑negativos, o que explica sua seletividade por esses patógenos.
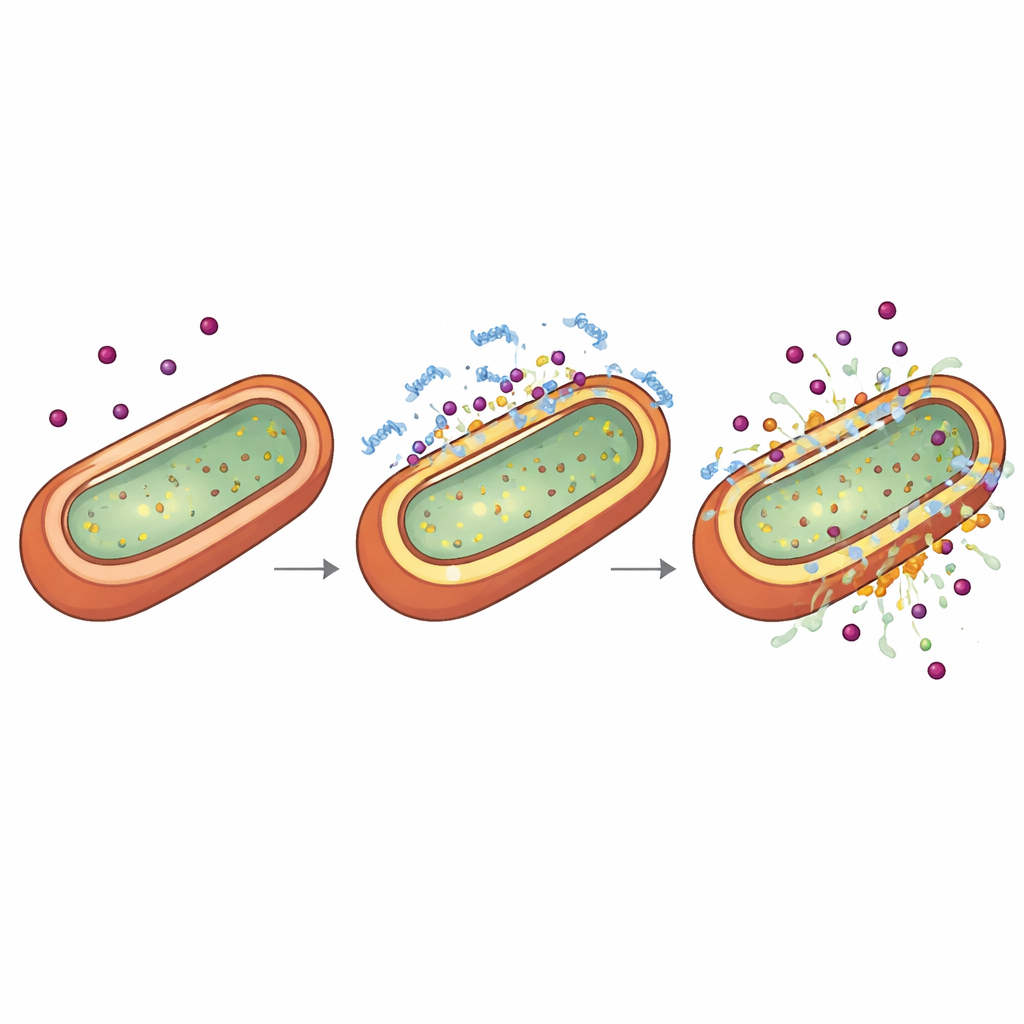
Acalmando a reação exagerada do corpo
Infecções graves não dependem apenas do microrganismo; a própria resposta imune do corpo frequentemente sai do controle, levando à sepse e à falência de órgãos. Como o TP2‑5 se liga a moléculas superficiais bacterianas que disparam inflamação, a equipe testou se ele também poderia reduzir essa hiperatividade imune. Em células imunes de camundongos, TP2‑5 bloqueou a ligação desses fragmentos bacterianos, atenuou vias de sinalização chave e reduziu de forma ampla a ativação de genes que dirigem a inflamação. Em modelos animais, incluindo um sistema de infecção em lagarta, um modelo de pneumonia resistente a drogas e uma cirurgia padrão de sepse em camundongos, TP2‑5 sozinho ou combinado com antibióticos reduziu a contagem bacteriana, diminuiu marcadores de lesão orgânica, reduziu mensageiros inflamatórios no sangue e, notavelmente, produziu 100% de sobrevivência no modelo de sepse polimicrobiana, onde antibióticos padrão ajudaram mas não protegeram totalmente.
Equilibrando eficácia e segurança
Qualquer novo anti‑infeccioso deve causar mais dano aos microrganismos do que aos pacientes. TP2‑5 mostrou esse tipo de seletividade em culturas de células humanas e de camundongo, onde efeitos nocivos apareceram apenas em concentrações muitas vezes superiores às necessárias para bloquear bactérias. Em camundongos, tanto a administração intravenosa quanto a direcionada aos pulmões não causaram perda de peso significativa, dano orgânico ou anormalidades nas células sanguíneas em níveis relevantes para tratamento. O peptídeo tende a se acumular principalmente no fígado e é gradualmente eliminado ao longo de vários dias, apoiando a ideia de que pode ser administrado em doses auxiliares sem toxicidade óbvia.
O que isso significa para tratamentos futuros
Este trabalho apresenta o TP2‑5 como um parceiro “sensibilizador de membrana” para antibióticos existentes: ele afrouxa o revestimento protetor dos superagentes Gram‑negativos em um estado energizado especial que os torna mais fáceis de matar, ao mesmo tempo em que captura gatilhos inflamatórios que podem levar pacientes à sepse letal. Embora o estudo não tenha provado que o estado hiperpolarizado incomum seja a causa direta da melhor atividade dos fármacos, a forte correlação temporal e de efeito sugere que é uma peça importante do quebra‑cabeça. Se peptídeos semelhantes puderem ser usados com segurança em humanos, eles poderiam estender a vida útil dos nossos antibióticos atuais e oferecer uma abordagem dupla — atacando as bactérias e acalmando a resposta do corpo — especialmente valiosa para infecções multirresistentes de difícil tratamento.
Citação: Yeh, JC., Hazam, P.K., Lin, YY. et al. Antimicrobial peptide-induced inner membrane hyperpolarization is associated with antibiotic sensitization and attenuated MIC escalation in multidrug-resistant Gram-negative pathogens. npj Antimicrob Resist 4, 33 (2026). https://doi.org/10.1038/s44259-026-00210-x
Palavras-chave: peptídeos antimicrobianos, adjuvantes de antibióticos, bactérias multirresistentes, sepse, infecções Gram‑negativas