Clear Sky Science · de
Peptidinduzierte Hyperpolarisation der inneren Membran ist mit Antibiotika-Sensibilisierung und abgeschwächter MIC-Steigerung bei multiresistenten gramnegativen Erregern assoziiert
Warum diese Forschung für die alltägliche Gesundheit wichtig ist
Tödliche Infektionen werden immer schwerer zu behandeln, da Bakterien gelernt haben, unseren stärksten Antibiotika zu widerstehen. Diese Studie untersucht einen neuen Ansatz, um bestehende Wirkstoffe wieder wirksam zu machen: das Hinzufügen eines kleinen, natürlich inspirierten Moleküls, eines Peptids. Die Arbeit legt nahe, dass wir nicht für jede Bedrohung völlig neue Antibiotika benötigen; stattdessen können wir die bereits vorhandenen Mittel „aufladen“ und gleichzeitig die übermäßige Entzündungsreaktion dämpfen, die Sepsis so gefährlich macht.
Ein Hilfsmolekül für angeschlagene Antibiotika
Die Forschenden konzentrierten sich auf ein modifiziertes, aus Fischen abgeleitetes Molekül namens TP2‑5, ein positiv geladenes Peptid, das allein einige Bakterien abtöten kann. Sie prüften, ob sehr geringe Mengen dieses Peptids zusammen mit Standardantibiotika resistente Erreger behandelbarer machen könnten. An problematischen Stämmen gramnegativer Bakterien wie multiresistenten Escherichia coli und Acinetobacter baumannii fanden sie, dass bereits ein Viertel der minimalen TP2‑5‑Dosis, die das Wachstum hemmt, mehrere verschiedene Antibiotika — darunter Meropenem, Colistin, Ciprofloxacin und sogar normalerweise unwirksames Vancomycin — deutlich wirksamer machte. In Labortests konnten Kombinationen mit niedrigen Dosen beider Wirkstoffe Bakterien vollständig eliminieren, die von den Einzelpräparaten nicht kontrolliert werden konnten.
Widerstandsentwicklung langsamer aufhalten
Antibiotikaresistenz verschlechtert sich normalerweise im Laufe der Zeit, wenn Bakterien wiederholt einem Wirkstoff ausgesetzt werden. Um diesen Prozess nachzubilden, züchtete das Team resistente E. coli drei Wochen lang unter täglicher Exposition gegenüber entweder Antibiotika allein, TP2‑5 allein oder Antibiotika plus niedrig dosiertem TP2‑5. Bei alleiniger Anwendung der Antibiotika stieg die zur Wachstumshemmung benötigte Menge dramatisch an — für einige Mittel um das bis zu 128‑Fache — was auf starke neu entstandene Resistenzen hinweist. Wurden dieselben Antibiotika mit TP2‑5 kombiniert, fiel diese Eskalation deutlich milder aus, was darauf hindeutet, dass das Hilfspeptid die Anpassungsfähigkeit der Bakterien verlangsamen kann. Bakterien, die nur TP2‑5 ausgesetzt waren, zeigten nur geringe Veränderungen in ihrer Empfindlichkeit gegenüber dem Peptid, was darauf hindeutet, dass es für sie schwerer sein könnte, starke Abwehrmechanismen gegen diese Art membrantargetierender Wirkung zu entwickeln.
Wie das Peptid die bakterielle Hülle umgestaltet
Um zu verstehen, warum TP2‑5 die Antibiotikawirkung verstärkt, untersuchten die Forschenden die äußere Hülle gramnegativer Bakterien, die sowohl als Rüstung als auch als Türsteher fungiert. Mit chemischen Farbstoffen, die aufleuchten, wenn Membranen undicht werden oder sich die Spannung ändert, sowie mit Kryo‑Elektronentomographie, die gefrorene Zellen dreidimensional abbildet, zeigten sie, dass sehr niedrige, nicht‑tödliche Dosen von TP2‑5 die äußere Schicht subtil verdünnen und punktieren, während sie die innere Membran in einen ungewöhnlich energiegeladenen oder „hyperpolarisierten“ Zustand versetzen. Bei höheren Dosen zerreißt dasselbe Peptid die Membranen. Zeitliche Experimente ergaben, dass, wenn Bakterien zuerst durch TP2‑5 in diesen hyperpolarisierten, leicht undichten Zustand versetzt werden, eine spätere Exposition gegenüber Antibiotika schnell ihre innere Membran kollabieren lässt und sie abtötet. Das Peptid bindet bevorzugt an negativ geladene Komponenten wie Lipopolysaccharide und bestimmte Phospholipide, die in gramnegativen Hüllen reichlich vorhanden sind, was seine Selektivität für diese Erreger erklärt.
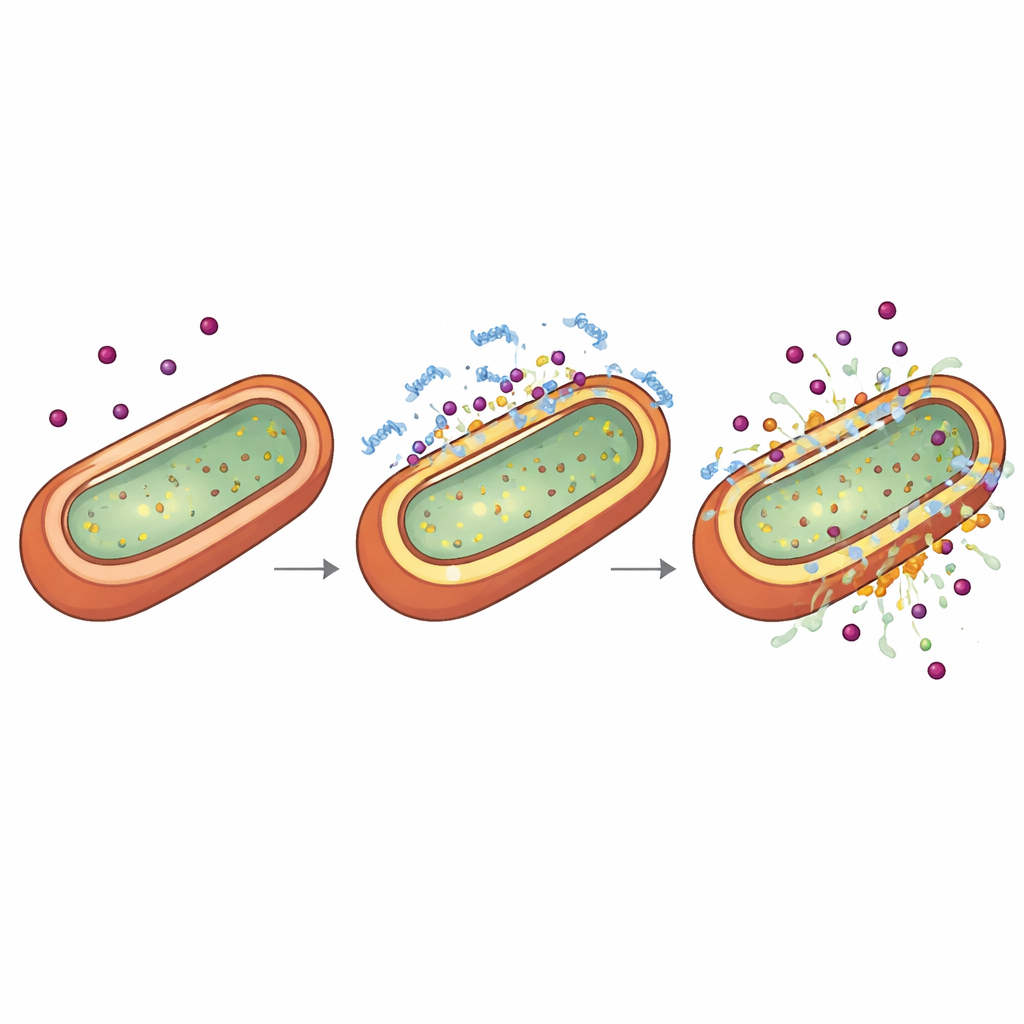
Die gefährliche Überreaktion des Körpers dämpfen
Schwere Infektionen hängen nicht nur vom Mikroorganismus ab; die eigene Immunantwort des Körpers gerät oft außer Kontrolle und führt zu Sepsis und Organversagen. Da TP2‑5 an bakterielle Oberflächenmoleküle bindet, die Entzündungen auslösen, prüfte das Team, ob es auch die Immunüberreaktion abschwächen kann. In Maus‑Immunzellen blockierte TP2‑5 die Bindung dieser bakteriellen Fragmente, dämpfte wesentliche Signalwege und reduzierte allgemein die Aktivierung von Genen, die Entzündungen antreiben. In Tiermodellen — einschließlich eines Raupeninfektionssystems, eines Modells für resistente Lungenentzündungen und einem Standard‑Maus‑Sepsis‑Versuch — senkte TP2‑5 allein oder in Kombination mit Antibiotika die Bakterienzahlen, verringerte Marker für Organschäden, reduzierte entzündliche Botenstoffe im Blut und erzielte bemerkenswerterweise 100% Überleben im polymikrobiellen Sepsis‑Modell, in dem Standardantibiotika zwar halfen, aber keinen vollständigen Schutz boten.
Zwischen Wirkung und Sicherheit abwägen
Jedes neue Antiinfektivum muss den Mikroben mehr schaden als den Patienten. TP2‑5 zeigte diese Selektivität in kultivierten menschlichen und murinen Zellen, wobei schädliche Effekte erst bei Konzentrationen auftraten, die um ein Vielfaches höher lagen als die zur Hemmung der Bakterien benötigten. Bei Mäusen führten sowohl intravenöse als auch lungengestützte Verabreichung bei therapeutisch relevanten Dosen zu keinem nennenswerten Gewichtsverlust, keinen Organschäden und keinen Auffälligkeiten im Blutbild. Das Peptid akkumulierte überwiegend in der Leber und wurde über mehrere Tage allmählich eliminiert, was die Vorstellung stützt, dass es in adjuvanten, unterstützenden Dosen ohne offensichtliche Toxizität verabreicht werden kann.
Was das für künftige Behandlungen bedeutet
Diese Arbeit stellt TP2‑5 als einen „membransensibilisierenden“ Partner für bestehende Antibiotika dar: Es lockert die schützende Hülle gramnegativer Supererreger in einen besonders energiegeladenen Zustand, der sie leichter angreifbar macht, und bindet gleichzeitig entzündungsfördernde Trigger, die Patienten in lebensbedrohliche Sepsis treiben können. Auch wenn die Studie nicht endgültig bewiesen hat, dass der ungewöhnliche hyperpolarisierte Zustand die direkte Ursache für die verbesserte Wirkstoffaktivität ist, deutet die enge zeitliche und wirkungsbezogene Verbindung darauf hin, dass er ein wichtiger Baustein ist. Können ähnliche Peptide sicher beim Menschen eingesetzt werden, könnten sie die Wirkdauer unserer aktuellen Antibiotika verlängern und einen zweigleisigen Ansatz bieten — Erreger bekämpfen und die Immunantwort beruhigen — was besonders wertvoll bei schwer zu behandelnden, multiresistenten Infektionen wäre.
Zitation: Yeh, JC., Hazam, P.K., Lin, YY. et al. Antimicrobial peptide-induced inner membrane hyperpolarization is associated with antibiotic sensitization and attenuated MIC escalation in multidrug-resistant Gram-negative pathogens. npj Antimicrob Resist 4, 33 (2026). https://doi.org/10.1038/s44259-026-00210-x
Schlüsselwörter: antimikrobielle Peptide, Antibiotika‑Adjuvantien, multiresistente Bakterien, Sepsis, gramnegative Infektionen