Clear Sky Science · fr
La hyperpolarisation de la membrane interne induite par un peptide antimicrobien est associée à la sensibilisation aux antibiotiques et à une atténuation de l’escalade de la CMI chez des pathogènes Gram‑négatifs multirésistants
Pourquoi cette recherche compte pour la santé quotidienne
Les infections mortelles deviennent plus difficiles à traiter à mesure que les bactéries développent des résistances à nos antibiotiques les plus puissants. Cette étude explore une nouvelle manière de rétablir l’efficacité des médicaments existants en ajoutant une petite molécule d’origine naturelle, un peptide. Les résultats suggèrent qu’il n’est pas toujours nécessaire de découvrir de nouveaux antibiotiques : on peut « suralimenter » ceux que nous possédons tout en atténuant l’inflammation incontrôlée qui rend le sepsis si dangereux.
Un moléculaire d’aide pour des antibiotiques en difficulté
Les chercheurs se sont concentrés sur une molécule modifiée d’origine piscicole nommée TP2‑5, un peptide chargé positivement qui, seul, peut tuer certaines bactéries. Ils ont testé si l’ajout de très petites quantités de ce peptide en association avec des antibiotiques courants pouvait faciliter le traitement de germes multirésistants. En travaillant sur des souches problématiques de bactéries Gram‑négatives comme des Escherichia coli et Acinetobacter baumannii résistants, ils ont constaté que l’ajout d’un quart seulement de la dose minimale de TP2‑5 nécessaire pour inhiber la croissance permettait à plusieurs antibiotiques — dont le méropénem, la colistine, la ciprofloxacine et même la vancomycine, habituellement inefficace — de fonctionner bien mieux. Dans des essais de laboratoire, des combinaisons utilisant de faibles doses des deux agents pouvaient éliminer complètement des bactéries que chaque médicament seul n’avait pas réussi à contrôler.
Limiter la montée rapide de la résistance
La résistance aux antibiotiques s’aggrave généralement avec le temps lorsque les bactéries sont exposées de façon répétée à un médicament. Pour reproduire ce processus, l’équipe a fait croître des E. coli résistants pendant trois semaines sous exposition quotidienne soit aux antibiotiques seuls, soit à TP2‑5 seul, soit aux antibiotiques associés à une faible dose de TP2‑5. Lorsque les antibiotiques étaient utilisés seuls, la quantité nécessaire pour arrêter la croissance bactérienne a augmenté de façon spectaculaire — jusqu’à 128 fois pour certains agents — signalant une résistance nouvelle et forte. Lorsque ces mêmes antibiotiques étaient associés à TP2‑5, cette escalade était beaucoup plus modérée, suggérant que le peptide adjuvant peut ralentir la capacité d’adaptation des bactéries. Parallèlement, les bactéries exposées à TP2‑5 seul ont montré peu de modification de leur sensibilité au peptide, laissant penser qu’il leur est plus difficile d’évoluer des défenses solides contre ce type d’attaque ciblant la membrane.
Comment le peptide remodèle l’enveloppe bactérienne
Pour comprendre pourquoi TP2‑5 renforce l’action des antibiotiques, les scientifiques ont examiné l’enveloppe externe des bactéries Gram‑négatives, qui fait office d’armure et de verrou d’entrée. À l’aide de colorants chimiques qui s’illuminent lorsque les membranes fuient ou changent de potentiel, et de cryo‑tomographie électronique qui image les cellules gelées en trois dimensions, ils ont montré que de très faibles doses non létales de TP2‑5 amincissent et perforent subtilement la couche externe tout en plaçant la membrane interne dans un état anormalement énergisé ou « hyperpolarisé ». À des doses plus élevées, le même peptide déchire les membranes. Des expériences temporelles ont révélé que lorsque les bactéries sont d’abord mises dans cet état hyperpolarisé et légèrement perméable par TP2‑5, une exposition ultérieure aux antibiotiques entraîne rapidement l’effondrement de la membrane interne et la mort cellulaire. Le peptide préfère se lier à des composants chargés négativement appelés lipopolysaccharides et à certaines phospholipides, abondants dans les enveloppes des Gram‑négatifs, ce qui explique sa sélectivité pour ces agents pathogènes.
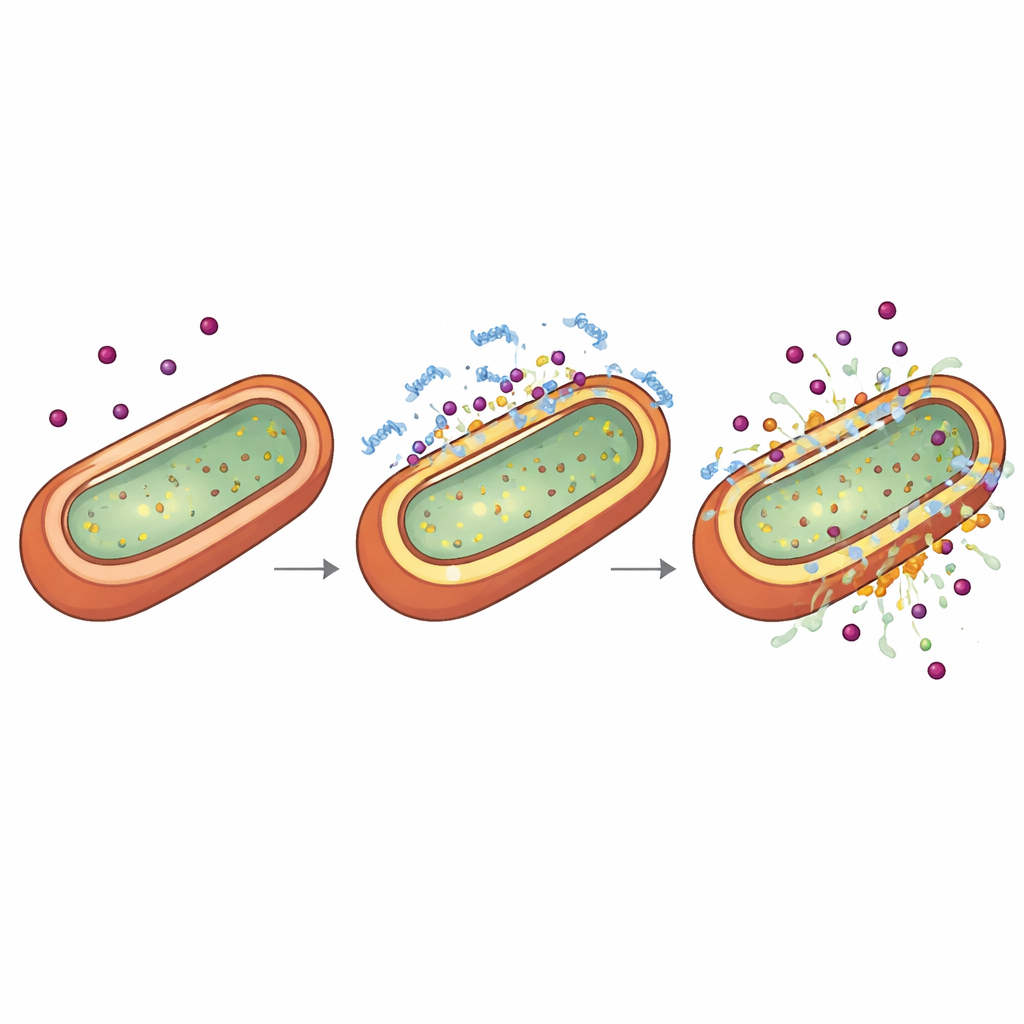
Calmer la réaction excessive dangereuse de l’organisme
Les infections sévères ne dépendent pas seulement du microbe : la réponse immunitaire elle‑même peut partir en spirale et provoquer un sepsis et une insuffisance d’organes. Parce que TP2‑5 se fixe aux molécules de surface bactériennes qui déclenchent l’inflammation, l’équipe a testé s’il pouvait aussi atténuer la réponse immunitaire excessive. Dans des cellules immunitaires de souris, TP2‑5 a bloqué la liaison de ces fragments bactériens, atténué des voies de signalisation clés et réduit de manière générale l’activation des gènes qui pilotent l’inflammation. Dans des modèles animaux — y compris un système d’infection chez la chenille, un modèle de pneumonie résistante aux médicaments et une chirurgie standard de sepsis chez la souris — TP2‑5 seul ou en combinaison avec des antibiotiques a réduit les charges bactériennes, diminué les marqueurs de lésion d’organe, abaissé les médiateurs inflammatoires dans le sang et, de manière frappante, a donné une survie de 100 % dans le modèle de sepsis polymicrobien, où les antibiotiques standards avaient aidé mais n’avaient pas totalement protégé.
Équilibrer puissance et sécurité
Tout nouvel anti‑infectieux doit nuire davantage aux microbes qu’aux patients. TP2‑5 a montré ce type de sélectivité dans des cultures de cellules humaines et de souris, où les effets nocifs n’apparaissaient qu’à des concentrations bien plus élevées que celles nécessaires pour bloquer les bactéries. Chez la souris, des administrations intraveineuses et dirigées vers les poumons n’ont entraîné ni perte de poids significative, ni atteinte d’organes, ni anomalies des cellules sanguines à des niveaux pertinents pour le traitement. Le peptide a eu tendance à s’accumuler principalement dans le foie et a été éliminé progressivement sur plusieurs jours, ce qui soutient l’idée qu’il peut être administré à des doses adjuvantes sans toxicité évidente.
Ce que cela signifie pour les traitements futurs
Ce travail présente TP2‑5 comme un partenaire « sensibilisant la membrane » pour les antibiotiques existants : il assouplit la couche protectrice des super‑bactéries Gram‑négatives en les plaçant dans un état énergisé particulier qui les rend plus faciles à éliminer, tout en neutralisant les déclencheurs de l’inflammation qui peuvent conduire les patients au sepsis mortel. Bien que l’étude n’ait pas prouvé que l’état hyperpolarisé inhabituel soit la cause directe de la meilleure activité des médicaments, le lien fort en termes de synchronie et d’effet suggère qu’il s’agit d’un élément important du mécanisme. Si des peptides similaires peuvent être utilisés en toute sécurité chez l’humain, ils pourraient prolonger la durée d’efficacité de nos antibiotiques actuels et offrir une approche à deux volets — viser les bactéries et calmer la réponse de l’hôte — particulièrement utile contre les infections multirésistantes difficiles à traiter.
Citation: Yeh, JC., Hazam, P.K., Lin, YY. et al. Antimicrobial peptide-induced inner membrane hyperpolarization is associated with antibiotic sensitization and attenuated MIC escalation in multidrug-resistant Gram-negative pathogens. npj Antimicrob Resist 4, 33 (2026). https://doi.org/10.1038/s44259-026-00210-x
Mots-clés: peptides antimicrobiens, adjuvants antibiotiques, bactéries multirésistantes, sepsis, infections à Gram négatif