Clear Sky Science · es
La hiperpolarización de la membrana interna inducida por péptidos antimicrobianos se asocia con la sensibilización a antibióticos y una menor escalada de la CIM en patógenos Gram negativos multirresistentes
Por qué esta investigación importa para la salud cotidiana
Las infecciones mortales son cada vez más difíciles de tratar a medida que las bacterias aprenden a resistir nuestros antibióticos más potentes. Este estudio explora una nueva forma de ayudar a que los fármacos existentes vuelvan a ser eficaces añadiendo una pequeña molécula de inspiración natural llamada péptido. El trabajo sugiere que puede que no necesitemos antibióticos completamente nuevos para cada amenaza; en su lugar, podemos “sobrealimentar” los que ya tenemos mientras atenuamos la inflamación descontrolada que hace que la sepsis sea tan peligrosa.
Una molécula auxiliar para antibióticos con dificultades
Los investigadores se centraron en una molécula modificada derivada de peces llamada TP2‑5, un péptido cargado positivamente que por sí solo puede matar algunas bacterias. Preguntaron si usar cantidades muy pequeñas de este péptido junto con antibióticos estándar podría facilitar el tratamiento de gérmenes multirresistentes. Trabajando con cepas problemáticas de bacterias Gram negativas como Escherichia coli resistente a fármacos y Acinetobacter baumannii, encontraron que añadir sólo una cuarta parte de la dosis mínima de TP2‑5 necesaria para inhibir el crecimiento permitió que varios antibióticos diferentes, incluidos meropenem, colistina, ciprofloxacino e incluso vancomicina —habitualmente ineficaz contra estos— funcionaran mucho mejor. En pruebas de laboratorio, las combinaciones que usaban dosis débiles de ambos fármacos juntas pudieron eliminar por completo bacterias que cada fármaco por separado no podía controlar.
Evitar que la resistencia aumente tan rápido
La resistencia a los antibióticos suele empeorar con el tiempo cuando las bacterias se exponen repetidamente a un fármaco. Para imitar este proceso, el equipo cultivó E. coli resistente durante tres semanas con exposición diaria a antibióticos solos, a TP2‑5 solo, o a antibióticos más TP2‑5 a baja dosis. Cuando los antibióticos se usaron por sí solos, la cantidad necesaria para detener el crecimiento bacteriano aumentó de forma dramática —hasta 128 veces para algunos fármacos—, lo que indica una fuerte nueva resistencia. Cuando los mismos antibióticos se emparejaron con TP2‑5, esta escalada fue mucho más leve, lo que sugiere que el péptido auxiliar puede ralentizar la capacidad de adaptación de las bacterias. Mientras tanto, las bacterias expuestas solo a TP2‑5 mostraron poco cambio en su sensibilidad al péptido, lo que apunta a que puede ser más difícil para ellas desarrollar defensas fuertes contra este tipo de ataque dirigido a la membrana.
Cómo el péptido remodela la envoltura bacteriana
Para entender por qué TP2‑5 potencia la acción de los antibióticos, los científicos examinaron la envoltura externa de las bacterias Gram negativas, que actúa tanto como armadura como portero. Usando tintes químicos que se iluminan cuando las membranas tienen fugas o cambian de voltaje, junto con criotomografía electrónica que imagen células congeladas en tres dimensiones, demostraron que dosis muy bajas y no letales de TP2‑5 adelgazan y perforan sutilmente la capa externa mientras ponen la capa interna en un estado inusualmente energizado o “hiperpolarizado”. A dosis más altas, ese mismo péptido destroza las membranas. Experimentos de sincronización revelaron que cuando las bacterias se colocan primero en este estado hiperpolarizado y ligeramente permeable por TP2‑5, la exposición posterior a antibióticos colapsa rápidamente su membrana interna y las mata. El péptido prefiere unirse a componentes cargados negativamente llamados lipopolisacáridos y a ciertos fosfolípidos, que son abundantes en las envolturas de Gram negativos, lo que explica su selectividad por estos patógenos.
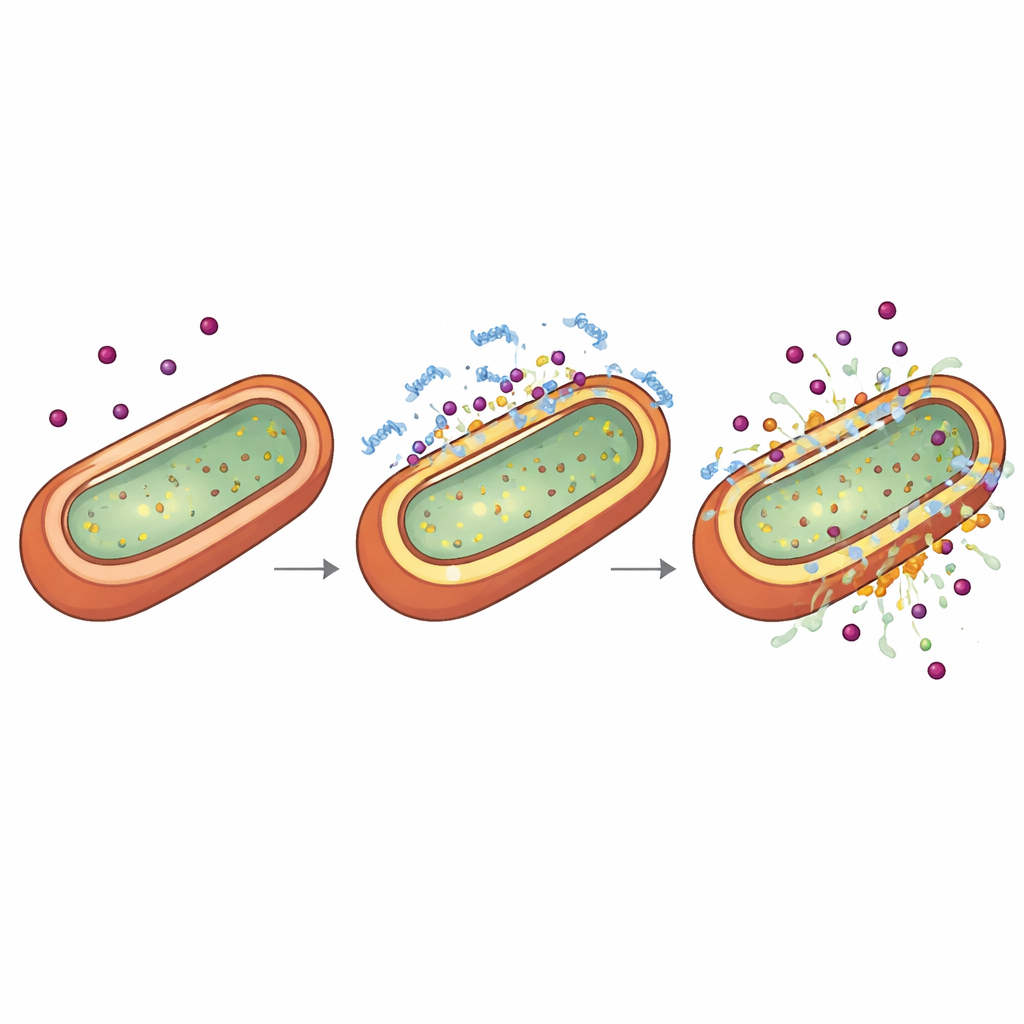
Apaciguar la sobrerreacción peligrosa del organismo
Las infecciones graves no dependen sólo del microbio; la propia respuesta inmune del organismo a menudo se desboca, conduciendo a sepsis y fallo orgánico. Dado que TP2‑5 se adhiere a moléculas superficiales bacterianas que desencadenan inflamación, el equipo probó si también podía atenuar la hiperactivación inmune. En células inmunitarias de ratón, TP2‑5 bloqueó la unión de esos fragmentos bacterianos, atenuó vías de señalización clave y redujo de forma generalizada la activación de genes proinflamatorios. En modelos animales, incluyendo un sistema de infección en oruga, un modelo de neumonía resistente a fármacos y una cirugía estándar de sepsis en ratón, TP2‑5 solo o combinado con antibióticos redujo el recuento bacteriano, disminuyó marcadores de daño orgánico, redujo mensajeros inflamatorios en sangre y, de forma llamativa, produjo 100 % de supervivencia en el modelo de sepsis polimicrobiana, donde los antibióticos estándar ayudaron pero no protegieron por completo.
Equilibrar eficacia y seguridad
Cualquier nuevo antiinfeccioso debe dañar más a los microbios que a los pacientes. TP2‑5 mostró este tipo de selectividad en cultivos de células humanas y de ratón, donde los efectos nocivos aparecieron sólo a concentraciones muchas veces superiores a las necesarias para bloquear bacterias. En ratones, tanto la administración intravenosa como la dirigida al pulmón no causó pérdida de peso significativa, daño orgánico ni anomalías en las células sanguíneas a niveles relevantes para el tratamiento. El péptido tendió a acumularse principalmente en el hígado y se eliminó gradualmente en el transcurso de varios días, lo que apoya la idea de que puede administrarse en dosis de adyuvante sin toxicidad obvia.
Lo que esto significa para tratamientos futuros
Este trabajo presenta a TP2‑5 como un socio “sensibilizador de membrana” para los antibióticos existentes: afloja la cubierta protectora de los supergérmenes Gram negativos colocándolos en un estado energizado especial que los hace más fáciles de matar, al tiempo que neutraliza desencadenantes inflamatorios que pueden empujar a los pacientes hacia una sepsis mortal. Aunque el estudio no demostró que el inusual estado hiperpolarizado sea la causa directa de la mejor actividad de los fármacos, el fuerte vínculo en tiempo y efecto sugiere que es una pieza importante del rompecabezas. Si péptidos similares pueden usarse con seguridad en humanos, podrían prolongar la vida útil de nuestros antibióticos actuales y ofrecer un enfoque de doble vía —golpear a las bacterias y calmar la respuesta del organismo— que resulta especialmente valioso frente a infecciones multirresistentes difíciles de tratar.
Cita: Yeh, JC., Hazam, P.K., Lin, YY. et al. Antimicrobial peptide-induced inner membrane hyperpolarization is associated with antibiotic sensitization and attenuated MIC escalation in multidrug-resistant Gram-negative pathogens. npj Antimicrob Resist 4, 33 (2026). https://doi.org/10.1038/s44259-026-00210-x
Palabras clave: péptidos antimicrobianos, adyuvantes antibióticos, bacterias multirresistentes, sepsis, infecciones por Gram negativos