Clear Sky Science · he
היפרפולריזציה של הממברנה הפנימית המושרת על‑ידי פפטיד אנטימיקרוביאלי קשורה לסנסיטיזציה לאנטיביוטיקה ולהאטת ההעלאה של MIC בפתוגנים גרם‑שליליים עמידים לרב‑תרופות
מדוע מחקר זה חשוב לבריאות היומיומית
זיהומים קטלניים הופכים לקשים יותר לטיפול ככל שהחיידקים מפתחים עמידות נגד האנטיביוטיקות החזקות שלנו. המחקר בוחן גישה חדשה שתוכל להחזיר את היעילות של תרופות קיימות על‑ידי הוספת מולקולה קטנה בהשראה טבעית שנקראת פפטיד. הממצאים מרמזים שאיננו חייבים למצוא אנטיביוטיקה חדשה לכל איום; במקום זאת, נוכל "להעצים" את אלה שכבר יש לנו ולבמקביל להרגיע את הדלקת הגורמת לספסיס להיות מסוכן כל‑כך.
מולקולת עזר לאנטיביוטיקות המתקשות
החוקרים התמקדו במולקולה משוננת שמקורה בדגים בשם TP2‑5, פפטיד בעל מטען חיובי שבמינונים מסוימים יכול להרוג חיידקים בעצמו. הם בדקו האם שימוש בכמויות מזעריות של פפטיד זה לצד אנטיביוטיקות סטנדרטיות יכול להפוך חיידקים עמידים לקלים יותר לטיפול. בעבודה עם זני בעיה של חיידקים גרם‑שליליים כמו Escherichia coli ו‑Acinetobacter baumannii עמידים לתרופות, הם מצאו שהוספה של רק רבע מהמינון המינימלי של TP2‑5 הדרוש לעיכוב גדילה איפשרה לכמה אנטיביוטיקות שונות — כולל מרופנאם, קוליסטין, ציפרופלוקסצין ואף ונקומיצין שבדרך כלל אינו יעיל — לפעול הרבה יותר טוב. בבדיקות מעבדה, שילובים שהשתמשו במינונים חלשים של שתי התרופות יחד יכלו לנקות לחלוטין חיידקים ששום תרופה לבדה לא יכלה לשלוט בהם.
עיכוב עליית העמידות
העמידות לאנטיביוטיקה בדרך כלל מחמירה עם הזמן כאשר חיידקים נחשפים לחומר שוב ושוב. כדי לדמות תהליך זה, הצוות גידל E. coli עמידים במשך שלושה שבועות תחת חשיפה יומית לאנטיביוטיקות בלבד, ל‑TP2‑5 בלבד, או לאנטיביוטיקות בתוספת TP2‑5 במינון נמוך. כאשר השתמשו רק באנטיביוטיקות, הכמות הנדרשת לעצור את הגדילה עלתה באופן דרמטי — עד פי 128 עבור חלק מהתרופות — דבר שמעיד על עמידות חדשה חזקה. כאשר אותן אנטיביוטיקות קושרו עם TP2‑5, העלייה היתה מתונה הרבה יותר, דבר שמעיד על כך שהפפטיד הסייע עשוי להאט את יכולת ההסתגלות של החיידקים. בינתיים, חיידקים שנחשפו ל‑TP2‑5 לבד הראו מעט שינוי ברגישותם לפפטיד, מה שרומז שקשה יותר להם להתפתח להגנות חזקות נגד סוג זה של התקפה שפוגעת בממברנה.
כיצד הפפטיד מעצב מחדש את מעטפת החיידק
כדי להבין מדוע TP2‑5 מגדיל את עוצמת האנטיביוטיקה, המדענים בחנו את מעטפת החיידקים הגרם‑שליליים, שמשמשת הן כשריון והן כשומרת סף. באמצעות צבעים כימיים שמתארים דליפות או שינוי במפל המתח של הממברנות, יחד עם טומוגרפיה קריואלקטרונית שמציגה תאים מוקפאים בתלת‑ממד, הם הראו שמינונים נמוכים מאוד, שאינם קטלניים, של TP2‑5 מדקיקים בעדינות ומחוררים את השכבה החיצונית בזמן שהם מכניסים את השכבה הפנימית למצב אנרגטי חריג או "היפרפולריזציה". במינונים גבוהים יותר אותו פפטיד קורע את הממברנות לגזרים. ניסויי תזמון הראו שכאשר החיידקים מועמדים תחילה למצב זה של היפרפולריזציה ודלילות קלה על‑ידי TP2‑5, חשיפה מאוחרת יותר לאנטיביוטיקה מובילה לקריסה מהירה של הממברנה הפנימית ולהרגם. לפפטיד יש העדפה לקשור רכיבים בעלי מטען שלילי שנקראים ליפופוליסכרידים ופוספוליפידים ספציפיים, השכיחים במעטפות גרם‑שליליות, מה שמסביר את בחירתו בפתוגנים אלה.
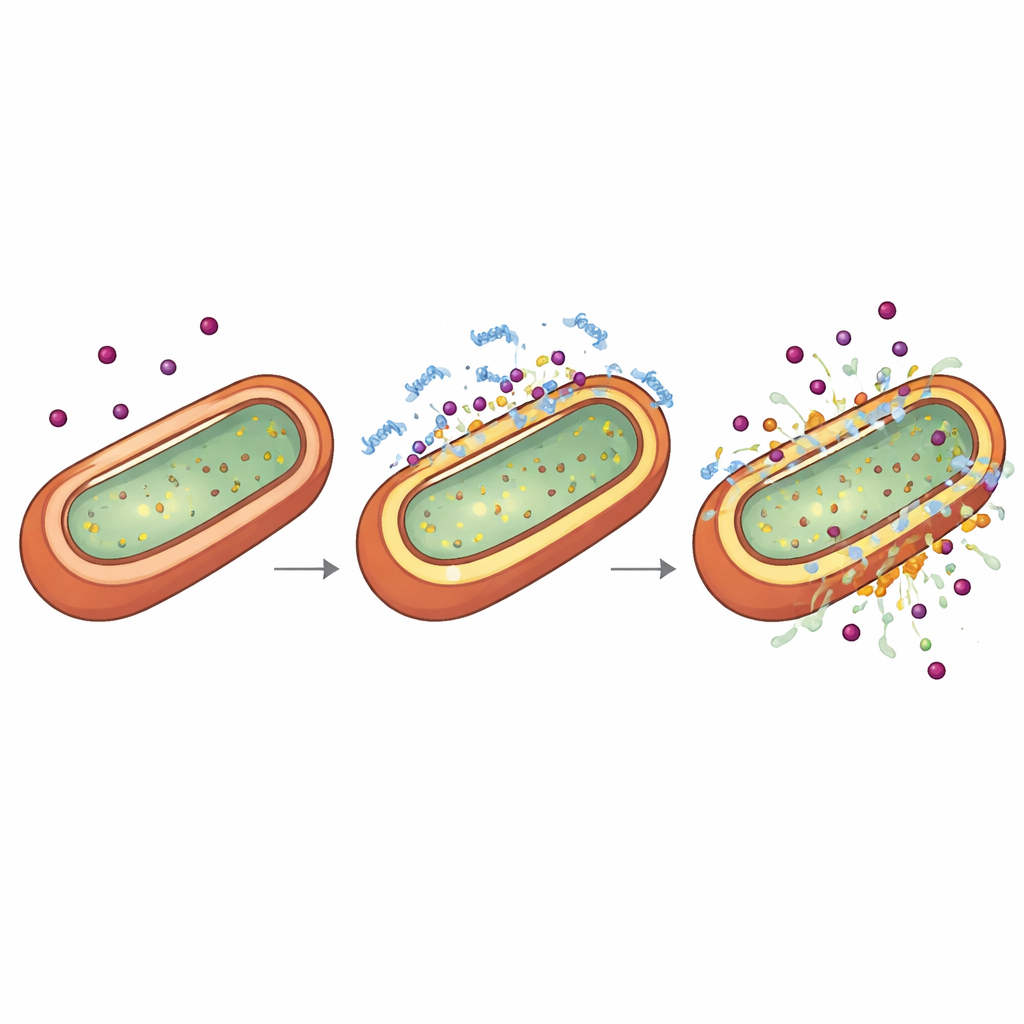
הרגעת תגובת היתר המסוכנת של הגוף
זיהומים חמורים אינם תלויים רק במיקרואורגניזם; תגובת המערכת החיסונית של הגוף לעתים קרובות מסלימה עד לספסיס ולכשל איברים. מאחר ש‑TP2‑5 נקשר למולקולות חיצוניות של חיידק שמפעילות דלקת, הצוות בדק האם הוא יכול גם להחליש את תגובת החיסון המופרזת. בתאי חיסון של עכברים, TP2‑5 חסם את הקשירה של שברי חיידק אלו, השתחל דרכים אותות מרכזיות, וצמצם באופן רחב את פעולת הגנים שמניעים דלקת. במודלים חייתיים, כולל מערכת זיהום בזחל, מודל דלקת ריאות עמידה לתרופות וניתוח סטנדרטי לספסיס בעכברים, TP2‑5 לבדו או בשילוב עם אנטיביוטיקה הקטין את כמות החיידקים, הוריד סמני נזק לאיברים, צימצם שליחי דלקת בדם, ובמפתיע השיג הישרדות של 100% במודל ספסיס פולימיקרוביאלי, שבו אנטיביוטיקות סטנדרטיות סייעו אך לא סיפקו הגנה מלאה.
איזון בין עוצמה ובטיחות
כל חומר אנטי‑מזהם חדש חייב להזיק למיקרובים יותר משהוא מזיק למטופלים. TP2‑5 הראה סלקטיביות כזו בתרביות של תאים אנושיים ועכבריים, כאשר השפעות מזיקות הופיעו רק בריכוזים גבוהים בהרבה מאלה הנדרשים לחסימת חיידקים. בעכברים, גם מינון תוך‑ורידי וגם כיוון ריאתי לא גרמו לאובדן משקל משמעותי, לנזק לאיברים או לשינויים תאי דם ברמות הרלוונטיות לטיפול. הפפטיד נטה להצטבר בעיקר בכבד ושרד להיסלק בהדרגה על פני מספר ימים, תומך ברעיון שניתן לתת אותו במינוני עזר ללא רעילות ברורה.
מה משמעות הדבר לטיפולים עתידיים
העבודה מציגה את TP2‑5 כ"שותף שמעורר את הממברנה" לאנטיביוטיקות קיימות: הוא מרכך את מעיל ההגנה של חיידקים גרם‑שליליים במצב אנרגטי מיוחד שמקל על הריגתם, ובמקביל קולט טריגרים דלקתיים שיכולים לדחוף מטופלים לספסיס קטלני. אף שהמחקר לא הוכיח שמצב ההיפרפולריזציה החריג הוא הסיבה הישירה לפעילות המוגברת של התרופות, הקשר החזק בזמן ובאפקט מרמז שהוא חלק חשוב בפאזל. אם פפטידים דומים יוכלו לשמש בבטחה בבני אדם, הם עשויים להאריך את חיי השימוש של האנטיביוטיקות הנוכחיות שלנו ולהציע גישה דו‑צדדית — פגיעה בחיידקים והרגעת תגובת הגוף — שהיא חשובה במיוחד בזיהומים עמידים וקשים לטיפול.
ציטוט: Yeh, JC., Hazam, P.K., Lin, YY. et al. Antimicrobial peptide-induced inner membrane hyperpolarization is associated with antibiotic sensitization and attenuated MIC escalation in multidrug-resistant Gram-negative pathogens. npj Antimicrob Resist 4, 33 (2026). https://doi.org/10.1038/s44259-026-00210-x
מילות מפתח: פפטידים אנטימיקרוביאליים, מערימים אנטיביוטיים, חיידקים עמידים לרב‑תרופות, ספסיס, זיהומים גרם‑שליליים