Clear Sky Science · sv
Möjliggör multitarget-läkemedelsupptäckt genom latent evolutionär optimering och syntesmedveten prioritering (EVOSYNTH)
Varför det är viktigt att utforma smartare läkemedel
Många allvarliga sjukdomar, från Alzheimers sjukdom till ovarialcancer, uppstår inte på grund av ett enda felaktigt protein utan genom hela nätverk av rubbade signalvägar. Att behandla sådana tillstånd med ett läkemedel riktat mot ett enda mål räcker ofta inte, medan att ge patienter flera läkemedel kan ge toxiska biverkningar och komplexa doseringsscheman. Denna studie presenterar EVOSYNTH, ett beräkningsramverk som syftar till att designa enskilda molekyler som säkert och effektivt kan påverka flera sjukdomsrelaterade mål samtidigt — och, avgörande, som kemister faktiskt kan framställa i laboratoriet.
Från enkla mål till många reglage
Traditionell läkemedelsupptäckt har i stor utsträckning jagat ”magiska kulor” som binder hårt till ett protein utan att störa andra. Med tiden har det blivit tydligt att detta tillvägagångssätt har svårt att hantera komplexa sjukdomar med flera återkopplingsslingor och reservvägar. Att lägga till fler läkemedel — polyfarmakostrategin — kan förbättra täckningen men ökar risken för farliga läkemedelsinteraktioner, oförutsägbar farmakologi och betungande behandlingsplaner. Multimålsläkemedel erbjuder en mellangata: en genomtänkt molekyl som modulerar flera nyckelproteiner samtidigt, i idealfallet så att ett helt nätverk skjuts tillbaka mot hälsa. Utmaningen är att hitta sådana molekyler och samtidigt säkerställa att de är praktiska att syntetisera, vilket är extremt svårt att göra för hand.
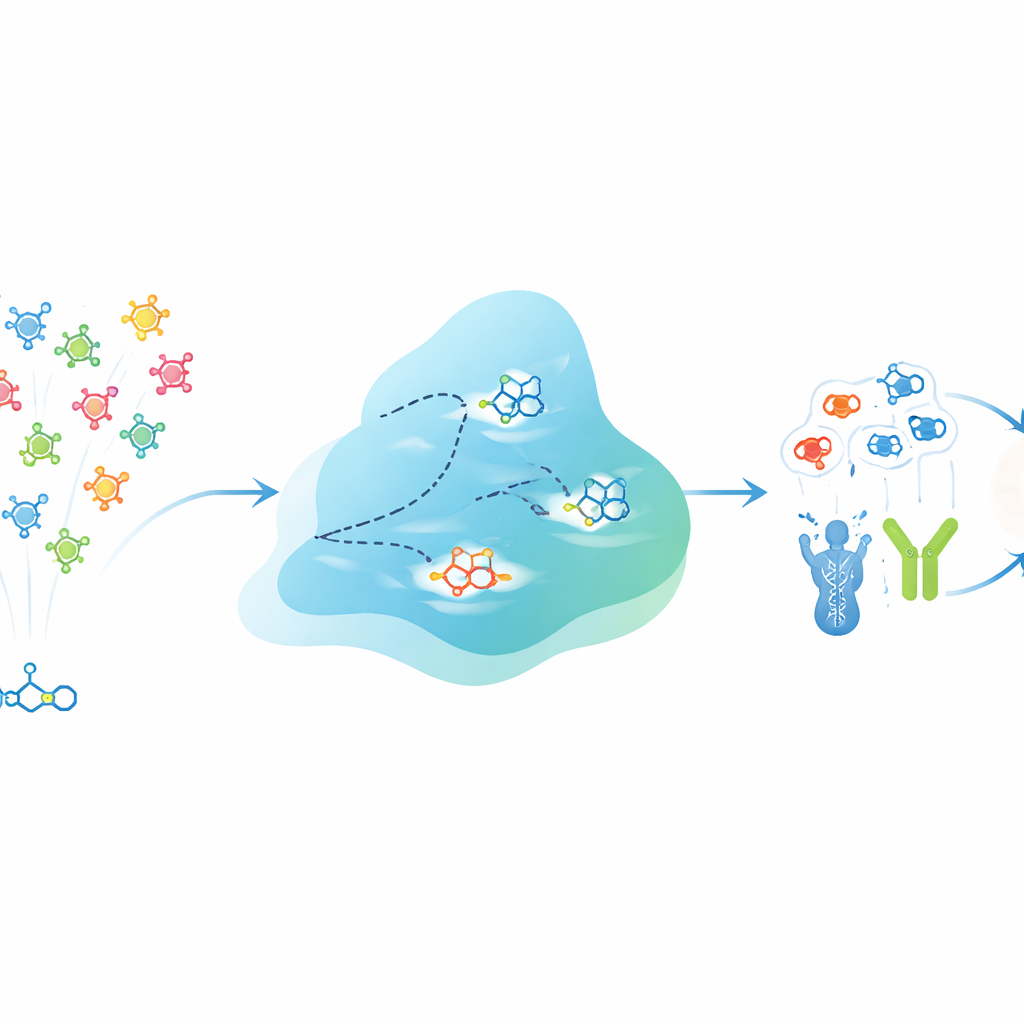
En digital evolutionär motor för molekyler
EVOSYNTH angriper denna utmaning genom att behandla potentiella läkemedel som en population som kan ”evolvera” inne i en dator. Istället för att förändra verkliga molekyler i ett provrör arbetar systemet i ett abstrakt, komprimerat rum som kodar både strukturen hos varje molekyl och dess förutspådda beteende mot olika proteintargets. Ett specialiserat neuralt nätverk lär sig detta rum så att närliggande punkter tenderar att motsvara molekyler med liknande multimålsaktivitet. En diffusionsprocess spelar sedan rollen som mutation och stökar försiktigt om dessa punkter för att generera nya virtuella molekyler. Efter varje omgång utvärderas kandidater för hur starkt de förväntas binda flera valda proteiner samtidigt, medan hårda filter kasserar de som inte uppfyller grundläggande krav på läkemedelslikhet, toxicitet eller, för hjärnsjukdomar, förmåga att passera blod-hjärnbarriären.
Designa läkemedel som faktiskt kan tillverkas
En viktig innovation i EVOSYNTH är att det inte stannar vid virtuell aktivitet. Många föreslagna molekyler från AI-modeller ser lovande ut på skärmen men är oöverkomligt svåra eller dyra att syntetisera. För att undvika detta fallgropar integrerar författarna ett syntesplaneringssystem kallat SPARROW i sitt arbetsflöde. Detta verktyg bygger reaktionsnätverk som kopplar varje kandidat tillbaka till lättinköpta byggstenar och uppskattar antalet steg, kostnaden för startmaterial och tillförlitligheten hos varje reaktion. Istället för att bara förkasta omöjliga molekyler i efterhand använder EVOSYNTH dessa nätverksomfattande beräkningar för att prioritera kandidater som erbjuder den bästa kompromissen mellan terapeutiskt löfte och verklig tillverkningsbarhet, inklusive möjligheter att återanvända intermediärer och dela steg mellan flera toppföreningar.
Realistiska tester vid hjärnsjukdom och cancer
För att demonstrera vad EVOSYNTH kan göra tillämpade forskarna det på två krävande fallstudier. För Alzheimers sjukdom sökte de molekyler som kunde blockera både JNK3 och GSK3β, två enzymer som implicerats i nervcellsdöd och onormal proteinansamling i hjärnan. För ovarialcancer riktade de in sig på ett par proteiner involverade i tillväxtsignalering och DNA-reparation, PI3K och PARP1, som har visat sig fungera särskilt väl när de hämmats tillsammans. Med utgångspunkt i kända enkla mål-läkemedel som ”frö”-strukturer genererade EVOSYNTH och förfinade nya strukturer över många generationer. Jämfört med en närbesläktad metod och en annan avancerad generativ modell producerade EVOSYNTH konsekvent kandidatmolekyler med starkare förväntad aktivitet mot båda målen, större strukturell variation och lägre likhet med ursprungsskelettet — tecken på att den utforskar verkligt ny kemisk terräng snarare än att tröska om samma motiv.
Att balansera effekt, mångfald och kostnad
När teamet granskade de bästa molekylerna ur syntessynpunkt blev fördelarna med deras tillvägagångssätt ännu tydligare. Under realistiska begränsningar — endast omkring tio föreningar kan gå vidare till experimentell testning — kombinerade EVOSYNTHs toppval högre förväntad terapeutisk avkastning med färre reaktionssteg, färre distinkta startmaterial och avsevärt lägre uppskattade materialkostnader än de som föreslogs av konkurrerande metoder. Intressant nog framträdde denna kostnadseffektivitet även om systemet inte uttryckligen tränades för att minimera syntetisk svårighet. Istället gjorde dess tendens att generera familjer av relaterade men ändå olika molekyler att syntesplaneraren kunde återanvända byggstenar och reaktionssekvenser, vilket naturligt favoriserade designer som skulle skala bättre i laboratoriet.
Vad detta innebär för framtidens läkemedel
För en icke-specialist är huvudpoängen att EVOSYNTH erbjuder ett sätt att intelligent söka genom det enorma rummet av möjliga molekyler, och leta inte bara efter dem som påverkar flera sjukdomsreglage samtidigt utan också efter dem som kemister kan framställa utan heroiska insatser. Genom att tätt koppla förutsägelser av multimålsaktivitet till kontroller av säkerhet, hjärngenomträngning och syntetisk praktik flyttar ramverket datorstödd läkemedelsdesign ett steg närmare att producera verkliga, testbara föreningar. Även om det nuvarande arbetet fokuserar på par av mål och förlitar sig på datoruppskattad bindning snarare än fullständiga experimentella data är tillvägagångssättet generellt. Med fortsatt förfining kan liknande system hjälpa till att designa en ny generation av mångsidiga läkemedel som är både biologiskt sofistikerade och tillverkbara i större skala.
Citering: Nguyen, V.T.D., Pham, P. & Hy, TS. Enabling multi-target drug discovery through latent evolutionary optimization and synthesis-aware prioritization (EVOSYNTH). Commun Chem 9, 133 (2026). https://doi.org/10.1038/s42004-026-01945-4
Nyckelord: multimåls läkemedelsdesign, AI-driven läkemedelsupptäckt, evolutionär optimering, syntetisk tillgänglighet, polyfarmakologi