Clear Sky Science · ja
潜在進化最適化と合成を考慮した優先順位付けによるマルチターゲット創薬の実現(EVOSYNTH)
より賢い薬を設計することが重要な理由
アルツハイマー病から卵巣がんに至る多くの重篤な疾患は、単一の異常タンパク質から生じるのではなく、途切れた経路の網が関与しています。こうした病態に対して単一の標的に向けた一剤で治療することは不十分な場合が多く、複数の薬を投与すると有害な副作用や複雑な投薬スケジュールを招きます。本研究はEVOSYNTHという計算フレームワークを紹介します。これは、複数の病態関連標的を安全かつ効果的に同時に作用させうる単一分子を設計することを目指し、重要な点として化学者が実際に実験室で合成可能な分子を重視します。
単一標的から複数のスイッチへ
従来の創薬は「魔法の弾丸」――ひとつのタンパク質に強く結合し他をほとんど無視する化合物――を追い求めてきました。しかし、時間が経つにつれて、フィードバックループや代替経路を含む複雑な疾患にはこの手法が限界を持つことが明らかになりました。薬を増やすポリファーマシー戦略はカバレッジを上げる一方で、危険な薬物相互作用や体内での予測困難な挙動、患者の負担増を招きます。マルチターゲット薬はその中間を目指します。複数の主要タンパク質を同時に適切に調節し、理想的にはネットワーク全体を健康な状態へと戻すように設計された一つの分子です。問題は、そのような分子を見つけ出し、かつ合成可能であることを確保するのが手作業では非常に困難だという点です。
分子のためのデジタル進化エンジン
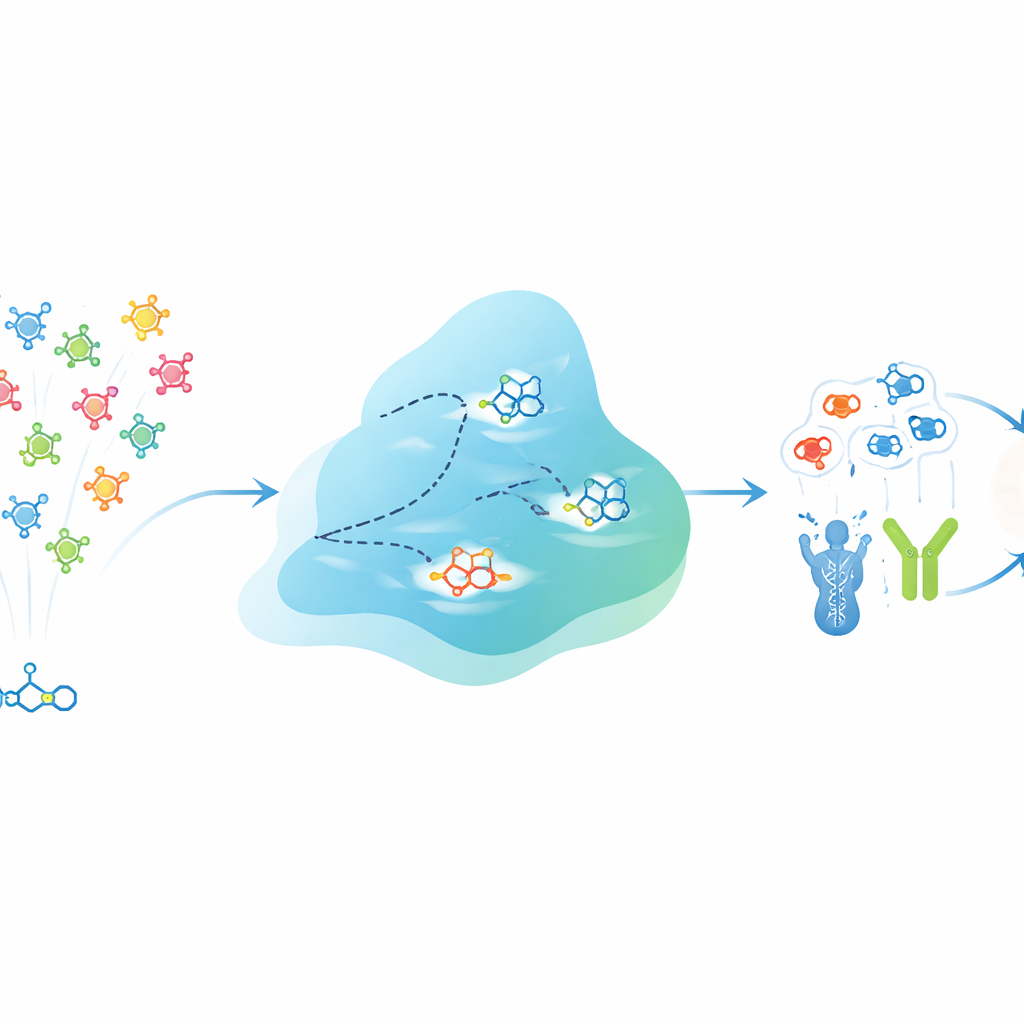
EVOSYNTHは、候補薬物をコンピュータ内で「進化」させる集団として扱うことでこの課題に取り組みます。実際の分子を試験管で変化させる代わりに、システムは各分子の構造と複数のタンパク質標的に対する予測挙動の両方を符号化した抽象的かつ圧縮された空間で動作します。特殊なニューラルネットワークがこの空間を学習し、近接する点が類似したマルチターゲット活性を持つ分子に対応するようにします。拡散過程が突然変異の役割を果たし、これらの点を穏やかに摂動して新しい仮想分子を生成します。各世代ごとに候補は選択した複数のタンパク質に対してどれだけ強く結合すると予測されるかで評価され、薬物様性、毒性、脳疾患の場合は血液脳関門透過性などの基本的要件を満たさないものは厳しいフィルターで除外されます。
実際に合成できる薬を設計する
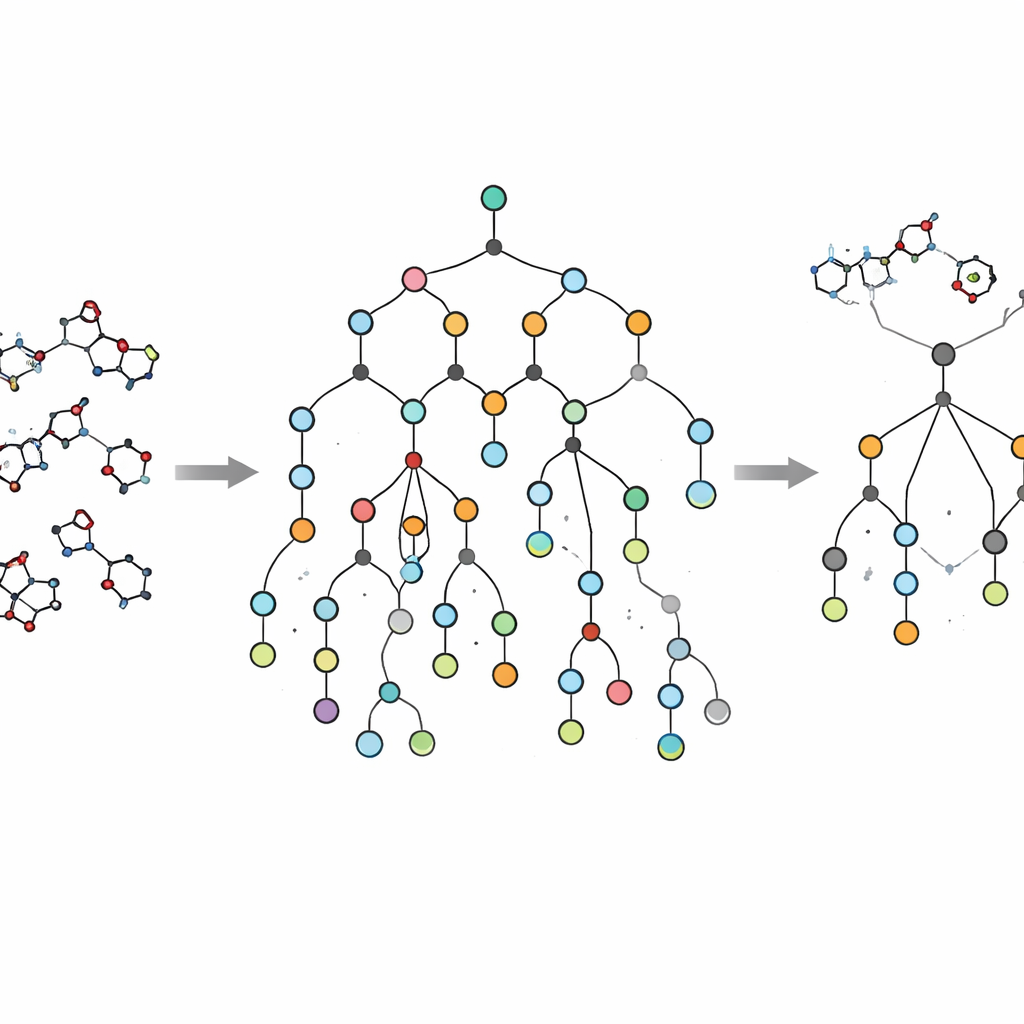
EVOSYNTHの重要な革新は、仮想的な活性で終わらせない点にあります。多くのAIモデルが提案する分子は画面上では有望に見えても、合成が極めて困難か高価で実用的でないことが多いです。この落とし穴を避けるため、著者らはSPARROWという合成計画システムをワークフローに組み込みます。このツールは各候補分子を容易に購入できる出発物質につなぐ反応ネットワークを構築し、ステップ数、出発材料のコスト、各反応の信頼性を見積もります。合成不可能な分子を事後的に単に却下するのではなく、EVOSYNTHはネットワーク全体の計算結果を用いて治療的見込みと実世界での製造可能性との間の最良のトレードオフを提供する候補を優先します。これには中間体の再利用や複数の上位化合物間で反応段階を共有する機会も含まれます。
脳疾患とがんでの現実的な試験
EVOSYNTHの能力を示すため、研究者らは2つの厳しいケースに適用しました。アルツハイマー病では、神経細胞死や異常タンパク蓄積に関与する酵素JNK3とGSK3βの両方を阻害できる分子を目指しました。卵巣がんでは、成長シグナル伝達とDNA修復に関与し、同時阻害で特に効果が示されているPI3KとPARP1のペアを標的としました。既知の単一標的薬を“シード”骨格として出発し、EVOSYNTHは多くの世代にわたり新しい構造を生成・洗練しました。密接に関連する別手法や他の先進的生成モデルと比較して、EVOSYNTHは一貫して両標的に対する予測活性が強く、構造的多様性が高く、元の骨格との類似度が低い候補分子を生み出しました。これは同じモチーフを繰り返し微調整するのではなく、実際に新しい化学空間を探索している兆候です。
効力、多様性、コストのバランス
研究チームが合成の観点から上位の分子を検討すると、アプローチの利点はさらに明確になりました。現実的な制約――実験検証に進めるのは約10化合物程度――の下で、EVOSYNTHの上位選択は治療上の期待利得が高いだけでなく、反応ステップ数が少なく、出発材料の種類が少なく、推定材料コストが競合手法よりも大幅に低いことが示されました。興味深いことに、この費用対効果はシステムが合成の難易度を明示的に最小化するように訓練されていたためではありません。むしろ、関連性のあるが多様な分子群を生成する傾向により、合成プランナーが出発物質や反応経路を再利用でき、実験室でのスケールアップに向く設計を自然に優先した結果です。
今後の薬にとっての意義
専門外の読者にとっての重要なポイントは、EVOSYNTHが膨大な候補分子空間を賢く探索する手段を提供し、複数の病態スイッチを同時に狙えるだけでなく化学者が大きな苦労なく合成できる分子を見つけ出せる点です。マルチターゲット活性の予測を安全性、脳への浸透、合成の実用性に関するチェックと密接に結びつけることで、このフレームワークは計算創薬を実際に検証可能な化合物に近づけます。現時点の研究は標的ペアに焦点を当て、結合予測は計算値に依存しており実験データが完全にそろっているわけではありませんが、手法自体は汎用的です。さらなる改良により、同様のシステムは生物学的に高度でかつスケール可能に製造可能な次世代の多目的薬の設計を支援する可能性があります。
引用: Nguyen, V.T.D., Pham, P. & Hy, TS. Enabling multi-target drug discovery through latent evolutionary optimization and synthesis-aware prioritization (EVOSYNTH). Commun Chem 9, 133 (2026). https://doi.org/10.1038/s42004-026-01945-4
キーワード: マルチターゲット薬物設計, AI駆動創薬, 進化的最適化, 合成しやすさ, ポリファーマコロジー