Clear Sky Science · it
Abilitare la scoperta di farmaci multi-target tramite ottimizzazione evolutiva latente e prioritarizzazione consapevole della sintesi (EVOSYNTH)
Perché progettare farmaci più intelligenti è importante
Molte malattie gravi, dall’Alzheimer al carcinoma ovarico, non derivano da una singola proteina difettosa ma da intere reti di percorsi alterati. Trattare tali condizioni con un singolo farmaco mirato a un unico bersaglio spesso non basta, mentre somministrare più farmaci può causare effetti collaterali tossici e regimi terapeutici complessi. Questo studio presenta EVOSYNTH, un quadro computazionale che mira a progettare molecole singole in grado di colpire contemporaneamente in modo sicuro ed efficace più bersagli legati alla malattia e, cosa cruciale, che i chimici possano effettivamente sintetizzare in laboratorio.
Da bersagli singoli a molteplici interruttori
La scoperta di farmaci tradizionale ha perseguito per lo più composti “proiettile magico” che si legano strettamente a una proteina lasciando intatte le altre. Col tempo è diventato chiaro che questo approccio fatica di fronte a malattie complesse che coinvolgono molti circuiti di retroazione e vie di riserva. Aggiungere più farmaci — la strategia della polifarmacologia — può migliorare la copertura ma aumenta il rischio di interazioni farmaco–farmaco pericolose, comportamenti imprevedibili nell’organismo e piani terapeutici gravosi. I farmaci multi-target offrono una via di mezzo: una singola molecola progettata con cura che modula contemporaneamente diverse proteine chiave, idealmente riportando l’intera rete verso uno stato di salute. La difficoltà sta nel trovare tali molecole e nel garantire che restino pratiche da sintetizzare: un compito estremamente difficile da svolgere manualmente.
Un motore di evoluzione digitale per molecole
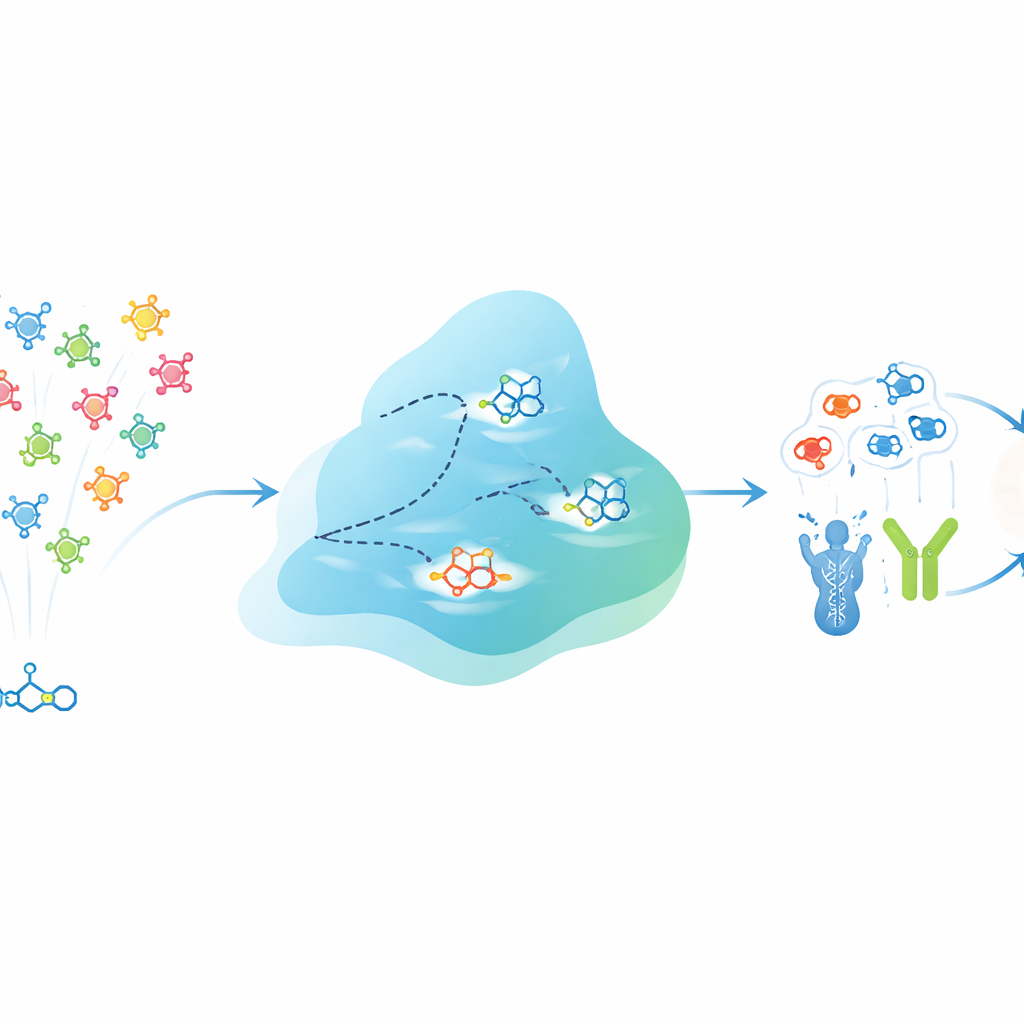
EVOSYNTH affronta questa sfida trattando i potenziali farmaci come una popolazione che può “evolvere” all’interno di un computer. Invece di modificare molecole reali in una provetta, il sistema lavora in uno spazio astratto e compresso che codifica sia la struttura di ogni molecola sia il suo comportamento previsto contro diversi bersagli proteici. Una rete neurale specializzata apprende questo spazio in modo che punti vicini tendano a corrispondere a molecole con attività multi-target simile. Un processo di diffusione svolge quindi il ruolo di mutazione, perturbando delicatamente questi punti per generare nuove molecole virtuali. Dopo ogni ciclo, i candidati vengono valutati in base alla forza prevista del loro legame con più proteine scelte contemporaneamente, mentre filtri rigorosi scartano quelli che non soddisfano requisiti fondamentali di drug-likeness, tossicità o, per le malattie cerebrali, la capacità di attraversare la barriera emato-encefalica.
Progettare farmaci che possano davvero essere sintetizzati
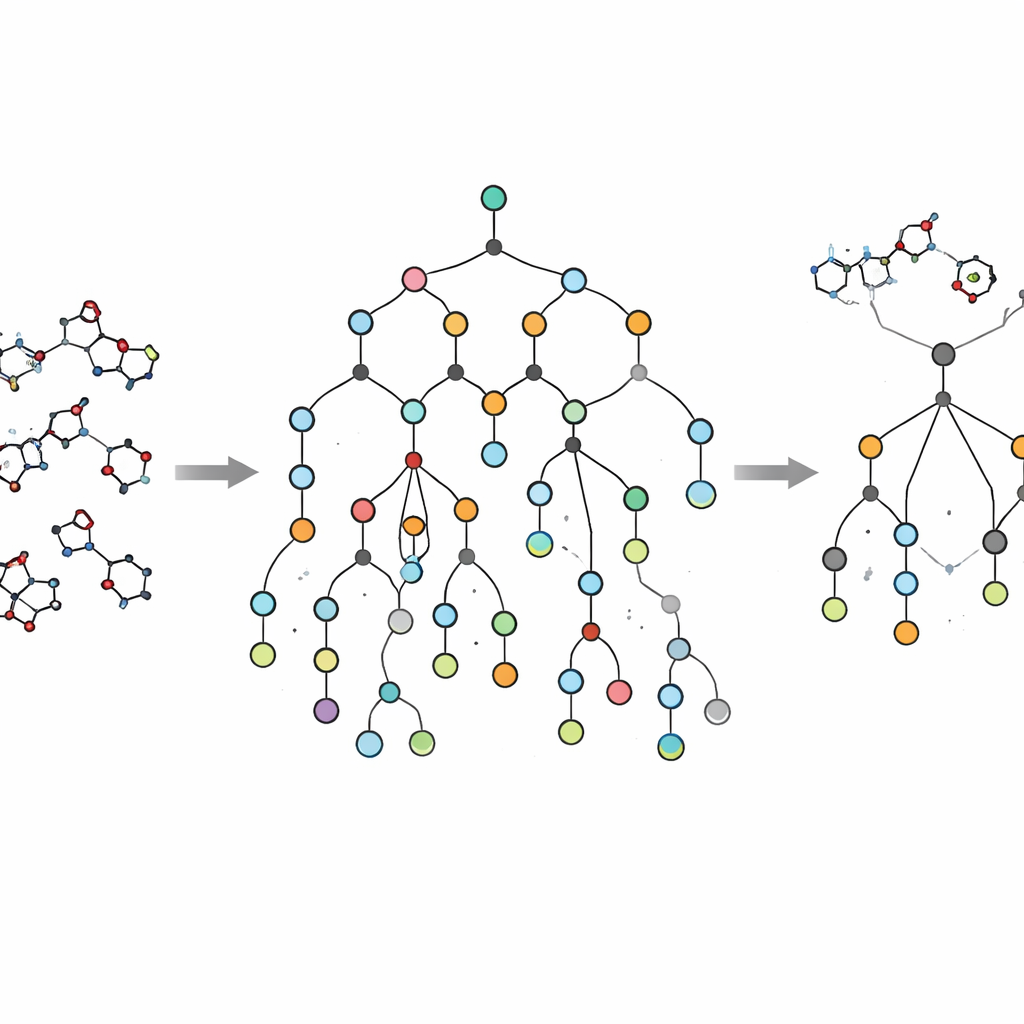
Un’innovazione importante di EVOSYNTH è che non si limita all’attività virtuale. Molte molecole proposte dai modelli di intelligenza artificiale appaiono promettenti sullo schermo ma sono proibitivamente difficili o costose da sintetizzare. Per evitare questo scoglio, gli autori integrano nel loro flusso di lavoro un sistema di pianificazione della sintesi chiamato SPARROW. Questo strumento costruisce reti di reazioni che collegano ciascuna molecola candidata a blocchi di partenza facilmente acquistabili, stimando il numero di passaggi, il costo dei materiali di partenza e l’affidabilità di ogni reazione. Invece di rifiutare semplicemente molecole impraticabili a posteriori, EVOSYNTH utilizza questi calcoli a livello di rete per priorizzare i candidati che offrono il miglior compromesso tra potenziale terapeutico e producibilità reale, incluse opportunità di riutilizzare intermedi e condividere passaggi tra diversi composti principali.
Test realistici in malattie cerebrali e cancro
Per dimostrare le capacità di EVOSYNTH, i ricercatori lo hanno applicato a due casi di prova impegnativi. Per l’Alzheimer hanno cercato molecole in grado di bloccare sia JNK3 sia GSK3β, due enzimi implicati nella morte neuronale e nell’accumulo anomalo di proteine nel cervello. Per il carcinoma ovarico, hanno mirato a una coppia di proteine coinvolte nel segnale di crescita e nella riparazione del DNA, PI3K e PARP1, che si sono dimostrate particolarmente efficaci quando inibite insieme. Partendo da farmaci noti che colpiscono un singolo bersaglio come scheletri “seed”, EVOSYNTH ha generato e affinato nuove strutture attraverso molte generazioni. Rispetto a un metodo strettamente correlato e a un altro modello generativo avanzato, EVOSYNTH ha prodotto in modo costante molecole candidate con attività prevista più forte su entrambi i bersagli, maggiore varietà strutturale e minore somiglianza con lo scaffold originale — segnali che sta esplorando un vero nuovo territorio chimico invece di ritoccare indefinitamente lo stesso motivo.
Bilanciare potenza, diversità e costo
Quando il team ha esaminato le migliori molecole dal punto di vista della sintesi, i vantaggi del loro approccio sono diventati ancora più evidenti. Sotto limiti realistici — solo circa dieci composti possono procedere ai test sperimentali — le scelte migliori di EVOSYNTH combinavano un rendimento terapeutico atteso più elevato con meno passaggi di reazione, meno materiali di partenza distinti e costi stimati dei materiali sostanzialmente inferiori rispetto a quelli proposti da metodi concorrenti. Interessante, questa convenienza in termini di costi è emersa nonostante il sistema non sia stato esplicitamente addestrato per minimizzare la difficoltà sintetica. Invece, la sua tendenza a generare famiglie di molecole correlate ma diverse ha permesso al pianificatore di sintesi di riutilizzare blocchi di costruzione e sequenze di reazione, favorendo naturalmente design che si scalano meglio in laboratorio.
Cosa significa per i farmaci del futuro
Per un non specialista, la conclusione chiave è che EVOSYNTH offre un modo per esplorare in modo intelligente l’immenso spazio delle molecole possibili, cercando non solo quelle che colpiscono contemporaneamente più interruttori di malattia ma anche quelle che i chimici possono realizzare senza sforzi eroici. Accoppiando strettamente le previsioni di attività multi-target con controlli su sicurezza, penetrazione cerebrale e praticità sintetica, il quadro avvicina la progettazione computazionale di farmaci alla produzione di composti reali e sperimentabili. Sebbene il lavoro attuale si concentri su coppie di bersagli e si basi su stime al computer dell’affinità piuttosto che su dati sperimentali completi, l’approccio è generale. Con ulteriori perfezionamenti, sistemi simili potrebbero aiutare a progettare una nuova generazione di farmaci multiuso biologicamente sofisticati e producibili su scala.
Citazione: Nguyen, V.T.D., Pham, P. & Hy, TS. Enabling multi-target drug discovery through latent evolutionary optimization and synthesis-aware prioritization (EVOSYNTH). Commun Chem 9, 133 (2026). https://doi.org/10.1038/s42004-026-01945-4
Parole chiave: progettazione di farmaci multi-target, scoperta di farmaci guidata dall'IA, ottimizzazione evolutiva, accessibilità sintetica, polifarmacologia