Clear Sky Science · pl
Umożliwienie odkrywania leków wielocelowych przez ukrytą optymalizację ewolucyjną i priorytetyzację z uwzględnieniem syntezy (EVOSYNTH)
Dlaczego ważne jest projektowanie mądrzejszych leków
Wiele poważnych chorób, od choroby Alzheimera po raka jajnika, nie wynika z jednej wadliwej białka, lecz z całych sieci zaburzonych szlaków. Leczenie takich schorzeń jednym lekiem skierowanym na jeden cel często okazuje się niewystarczające, podczas gdy podawanie pacjentom wielu leków może powodować toksyczne działania niepożądane i skomplikowane schematy dawkowania. W tym badaniu przedstawiono EVOSYNTH — ramy obliczeniowe mające na celu projektowanie pojedynczych cząsteczek zdolnych bezpiecznie i skutecznie oddziaływać na kilka związanych z chorobą celów jednocześnie — i co istotne, które chemicy faktycznie mogą wytworzyć w laboratorium.
Od pojedynczych celów do wielu przełączników
Tradycyjne odkrywanie leków w dużej mierze dążyło do „magicznych pocisków” — związków silnie wiążących się z jednym białkiem i niezakłócających reszty. Z czasem okazało się, że takie podejście ma problemy w chorobach z wieloma pętlami sprzężenia zwrotnego i drogami zapasowymi. Dodanie kolejnych leków — strategia polifarmakologii — może zwiększyć pokrycie, ale jednocześnie zwiększa ryzyko niebezpiecznych interakcji lek–lek, nieprzewidywalnego zachowania w organizmie i uciążliwych schematów leczenia. Leki wielocelowe oferują środkową drogę: jedną przemyślaną cząsteczkę, która jednocześnie moduluje kilka kluczowych białek, dążąc do przywrócenia równowagi całej sieci. Problem w tym, że znalezienie takich związków i zapewnienie, że pozostaną praktyczne do syntezy, jest niezwykle trudne do wykonania ręcznie.
Cyfrowy silnik ewolucyjny dla cząsteczek
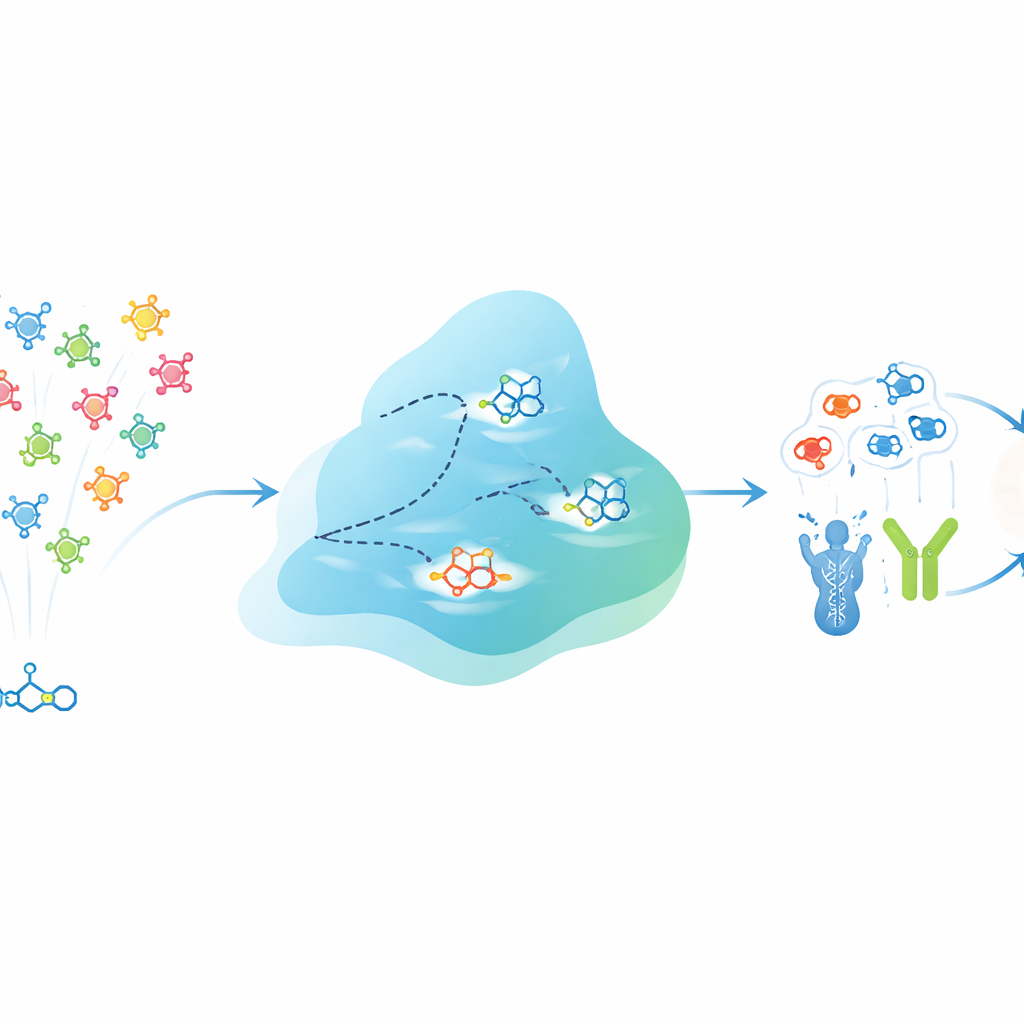
EVOSYNTH rozwiązuje to wyzwanie, traktując potencjalne leki jak populację, która może „ewoluować” w komputerze. Zamiast modyfikować rzeczywiste cząsteczki w probówce, system operuje w abstrakcyjnej, skompresowanej przestrzeni, która koduje zarówno strukturę każdej cząsteczki, jak i jej przewidywane zachowanie wobec różnych białkowych celów. Specjalistyczna sieć neuronowa uczy się tej przestrzeni tak, że pobliskie punkty odpowiadają zwykle cząsteczkom o podobnej aktywności wielocelowej. Proces dyfuzji pełni rolę mutacji, delikatnie perturbując te punkty, by generować nowe wirtualne cząsteczki. Po każdej rundzie kandydaci są oceniani pod kątem przewidywanej siły wiązania z wieloma wybranymi białkami jednocześnie, a twarde filtry odrzucają te, które nie spełniają podstawowych wymagań dotyczących zgodności z właściwościami leku, toksyczności lub, w przypadku chorób mózgu, zdolności przejścia przez barierę krew–mózg.
Projektowanie leków, które da się faktycznie wytworzyć
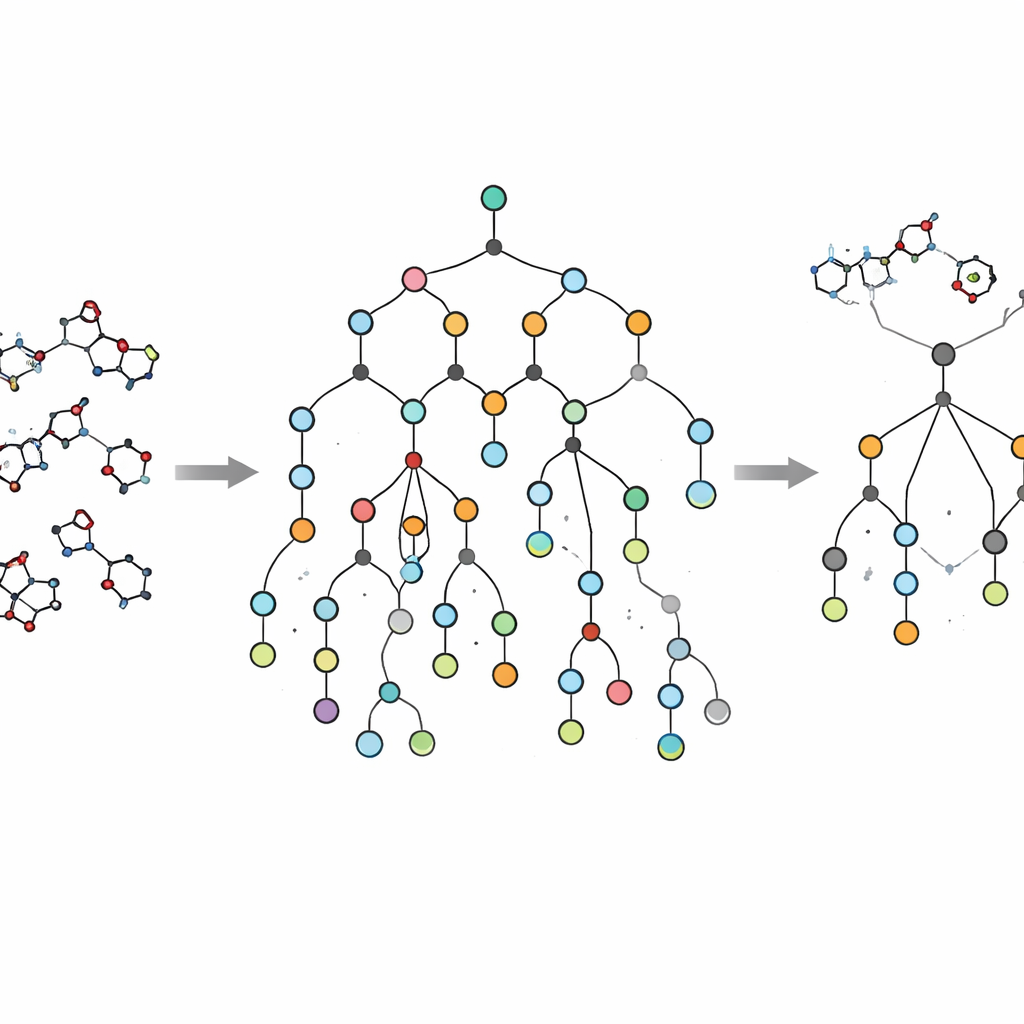
Istotną innowacją EVOSYNTH jest to, że nie zatrzymuje się na wirtualnej aktywności. Wiele proponowanych cząsteczek przez modele sztucznej inteligencji wygląda obiecująco na ekranie, ale jest zabójczo trudnych lub kosztownych do syntezy. Aby uniknąć tej pułapki, autorzy zintegrowali system planowania syntezy o nazwie SPARROW z ich procesem. To narzędzie buduje sieci reakcji łączące każdy kandydat z łatwo dostępnymi na rynku blokami budulcowymi, oszacowując liczbę kroków, koszt materiałów wyjściowych oraz niezawodność każdej reakcji. Zamiast po fakcie odrzucać niemożliwe do syntezy cząsteczki, EVOSYNTH używa tych obliczeń obejmujących całą sieć do priorytetyzacji kandydatów oferujących najlepszy kompromis między obiecującym potencjałem terapeutycznym a rzeczywistą możnością wytworzenia, w tym możliwości ponownego użycia pośredników i dzielenia etapów syntezy między wieloma wiodącymi związkami.
Realistyczne testy w chorobach mózgu i nowotworach
Aby pokazać możliwości EVOSYNTH, badacze zastosowali go do dwóch wymagających przypadków testowych. Dla choroby Alzheimera poszukiwali cząsteczek, które mogłyby blokować zarówno JNK3, jak i GSK3β — dwa enzymy zaangażowane w obumieranie komórek nerwowych i nieprawidłowe gromadzenie białek w mózgu. Dla raka jajnika skupili się na parze białek zaangażowanych w sygnalizację wzrostu i naprawę DNA, PI3K i PARP1, które wykazują szczególnie dobrą współpracę przy jednoczesnej inhibicji. Rozpoczynając od znanych leków skierowanych na pojedyncze cele jako „zasiewowych” rusztowań, EVOSYNTH generował i udoskonalał nowe struktury przez wiele pokoleń. W porównaniu z blisko spokrewnioną metodą i innym zaawansowanym modelem generatywnym, EVOSYNTH konsekwentnie produkował kandydatów o silniejszej przewidywanej aktywności względem obu celów, większej różnorodności strukturalnej i mniejszym podobieństwie do pierwotnego rusztowania — oznaki, że eksploruje prawdziwie nowy obszar chemiczny, zamiast bez końca modyfikować ten sam motyw.
Równoważenie mocy, różnorodności i kosztów
Gdy zespół przyjrzał się najlepszym cząsteczkom przez pryzmat syntezy, zalety ich podejścia stały się jeszcze bardziej widoczne. W realistycznych ograniczeniach — tylko około dziesięciu związków może przejść do testów eksperymentalnych — najlepsze wybory EVOSYNTH łączyły wyższy oczekiwany zwrot terapeutyczny z mniejszą liczbą etapów reakcji, mniejszą liczbą różnych materiałów początkowych i istotnie niższymi szacunkowymi kosztami materiałowymi niż propozycje konkurencyjnych metod. Co ciekawe, ta opłacalność syntetyczna pojawiła się mimo że system nie był wprost trenowany do minimalizowania trudności syntezy. Zamiast tego tendencja do generowania rodzin powiązanych, a jednocześnie różnorodnych cząsteczek pozwoliła planerowi syntezy na ponowne wykorzystanie bloków budulcowych i sekwencji reakcji, naturalnie faworyzując projekty lepiej skalowalne w laboratorium.
Co to oznacza dla przyszłych leków
Dla osoby niezajmującej się specjalistycznie kluczowe przesłanie jest takie, że EVOSYNTH oferuje sposób inteligentnego przeszukiwania ogromnej przestrzeni możliwych cząsteczek, szukając nie tylko tych, które jednocześnie wyłączają kilka „przełączników” chorobowych, ale także tych, które chemicy mogą wytworzyć bez herosów wysiłków. Dzięki ścisłemu powiązaniu przewidywań aktywności wielocelowej z kontrolami bezpieczeństwa, penetracji mózgu i praktyczności syntezy, rama ta przybliża projektowanie leków obliczeniowych do wytwarzania rzeczywistych, testowalnych związków. Chociaż obecna praca koncentruje się na parach celów i opiera się na komputerowych estymatach wiązania, a nie pełnych danych eksperymentalnych, podejście jest ogólne. Przy dalszym udoskonaleniu podobne systemy mogłyby pomóc zaprojektować nową generację leków wielozadaniowych, które będą zarówno biologicznie zaawansowane, jak i możliwe do wyprodukowania na skalę przemysłową.
Cytowanie: Nguyen, V.T.D., Pham, P. & Hy, TS. Enabling multi-target drug discovery through latent evolutionary optimization and synthesis-aware prioritization (EVOSYNTH). Commun Chem 9, 133 (2026). https://doi.org/10.1038/s42004-026-01945-4
Słowa kluczowe: projektowanie leków wielocelowych, odkrywanie leków napędzane przez AI, optymalizacja ewolucyjna, dostępność syntetyczna, polifarmacologia