Clear Sky Science · pt
Habilitando a descoberta de fármacos multitarget por meio de otimização evolutiva latente e priorização consciente da síntese (EVOSYNTH)
Por que projetar medicamentos mais inteligentes importa
Muitas doenças graves, da doença de Alzheimer ao câncer de ovário, não nascem de uma única proteína defeituosa, mas de redes inteiras de vias alteradas. Tratar essas condições com um único medicamento direcionado a um alvo normalmente é insuficiente, enquanto administrar vários medicamentos pode gerar efeitos colaterais tóxicos e esquemas de dosagem complexos. Este estudo apresenta o EVOSYNTH, uma estrutura computacional que visa projetar moléculas únicas capazes de atingir de maneira segura e eficaz vários alvos relacionados à doença ao mesmo tempo — e, crucialmente, que químicos possam realmente sintetizar no laboratório.
De alvos únicos a muitos interruptores
A descoberta tradicional de fármacos buscou em grande parte compostos “bala de prata” que se ligam fortemente a uma proteína e preservam as demais. Com o tempo, ficou claro que essa abordagem tem dificuldades frente a doenças complexas envolvendo múltiplos loops de feedback e rotas alternativas. Acrescentar mais medicamentos — a estratégia de polifarmácia — pode ampliar a cobertura, mas aumenta o risco de interações perigosas entre fármacos, comportamento imprevisível no organismo e regimes de tratamento onerosos. Medicamentos multitarget oferecem um caminho intermediário: uma única molécula cuidadosamente projetada que modula várias proteínas-chave ao mesmo tempo, idealmente empurrando toda uma rede de volta ao equilíbrio. O desafio é que encontrar tais moléculas, e garantir que permaneçam práticas de sintetizar, é extremamente difícil manualmente.
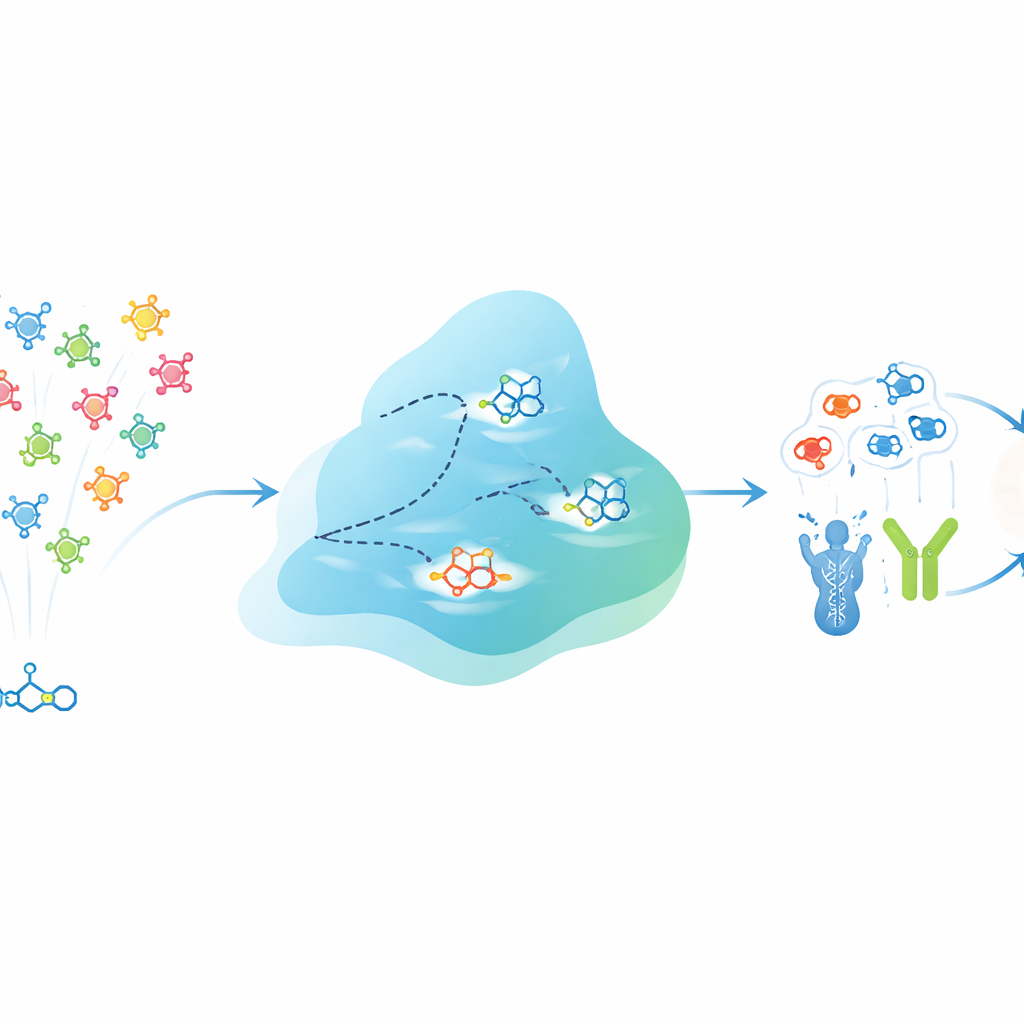
Um motor de evolução digital para moléculas
O EVOSYNTH enfrenta esse desafio tratando candidatos a fármacos como uma população que pode “evoluir” dentro de um computador. Em vez de alterar moléculas reais em um tubo de ensaio, o sistema opera em um espaço abstrato e comprimido que codifica tanto a estrutura de cada molécula quanto seu comportamento previsto contra diferentes alvos proteicos. Uma rede neural especializada aprende esse espaço de modo que pontos próximos tendam a corresponder a moléculas com atividade multitarget similar. Um processo de difusão então exerce o papel de mutação, perturbando suavemente esses pontos para gerar novas moléculas virtuais. Após cada rodada, os candidatos são avaliados quanto à força prevista de ligação a vários alvos escolhidos, enquanto filtros rígidos descartam os que falham em requisitos básicos de drug-likeness, toxicidade ou, para doenças cerebrais, a capacidade de cruzar a barreira hematoencefálica.
Projetando fármacos que realmente podem ser feitos
Uma inovação importante do EVOSYNTH é que ele não para na atividade virtual. Muitas moléculas propostas por modelos de inteligência artificial parecem promissoras na tela, mas são proibitivamente difíceis ou caras de sintetizar. Para evitar esse problema, os autores integram um sistema de planejamento de síntese chamado SPARROW ao fluxo de trabalho. Essa ferramenta constrói redes de reações que conectam cada molécula candidata a blocos de construção facilmente adquiríveis, estimando o número de etapas, o custo dos materiais iniciais e a confiabilidade de cada reação. Em vez de simplesmente rejeitar moléculas impossíveis a posteriori, o EVOSYNTH usa esses cálculos em nível de rede para priorizar candidatos que oferecem o melhor equilíbrio entre promessa terapêutica e fabricabilidade no mundo real, incluindo oportunidades de reutilizar intermediários e compartilhar etapas entre vários compostos de destaque.
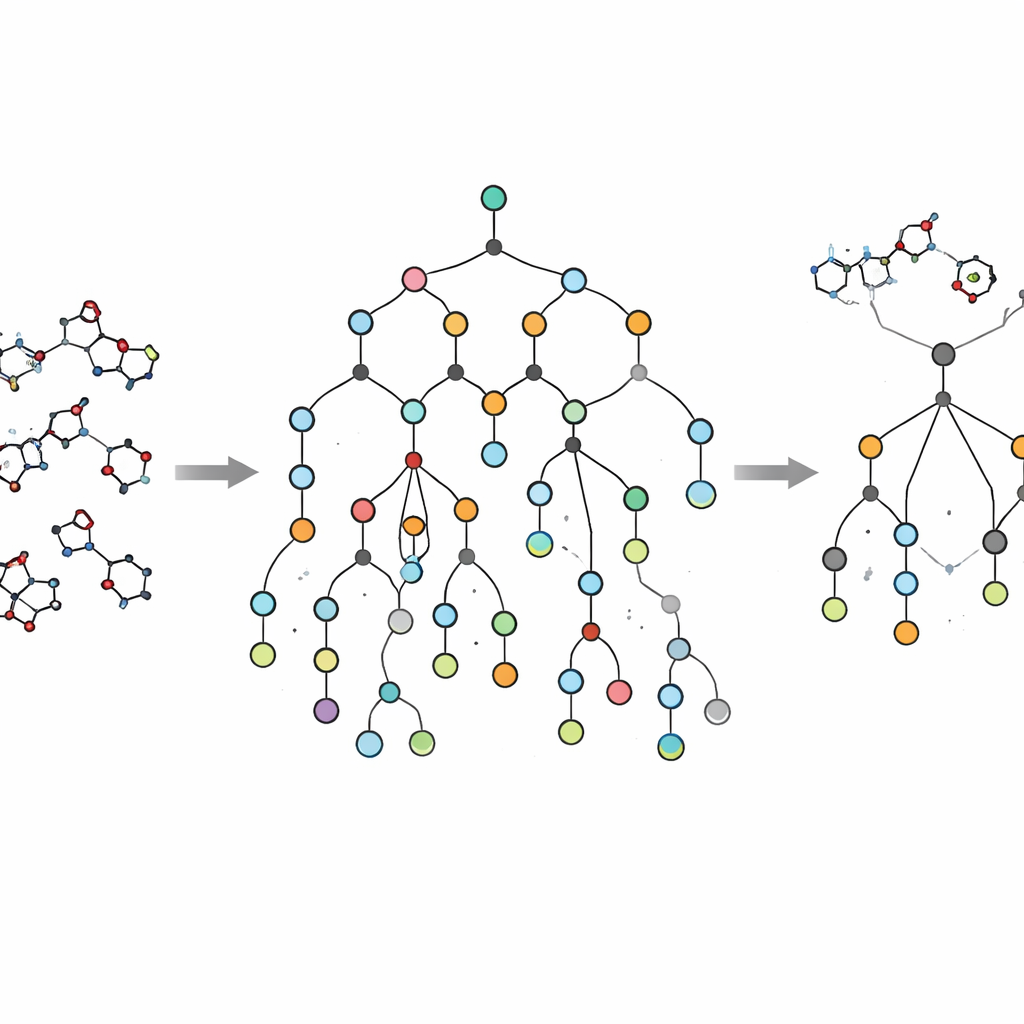
Testes realistas em doenças cerebrais e câncer
Para demonstrar o que o EVOSYNTH é capaz de fazer, os pesquisadores o aplicaram a dois casos de teste exigentes. Para a doença de Alzheimer, buscaram moléculas que pudessem bloquear tanto JNK3 quanto GSK3β, duas enzimas implicadas na morte de neurônios e no acúmulo anormal de proteínas no cérebro. Para o câncer de ovário, miraram um par de proteínas envolvidas em sinalização de crescimento e reparo de DNA, PI3K e PARP1, que mostraram eficácia quando inibidas em conjunto. Partindo de fármacos conhecidos de alvo único como “scaffolds” semente, o EVOSYNTH gerou e refinou novas estruturas ao longo de muitas gerações. Em comparação com um método relacionado e outro modelo generativo avançado, o EVOSYNTH produziu consistentemente candidatos com atividade prevista mais forte em ambos os alvos, maior variedade estrutural e menor similaridade ao scaffold original — sinais de que está explorando um território químico genuinamente novo em vez de ajustar repetidamente o mesmo motivo.
Equilibrando potência, diversidade e custo
Quando a equipe examinou as melhores moléculas sob a ótica da síntese, as vantagens da abordagem tornaram-se ainda mais claras. Dentro de limites realistas — apenas cerca de dez compostos podem avançar para testes experimentais — as principais seleções do EVOSYNTH combinaram maior retorno terapêutico esperado com menos etapas de reação, menos matérias-primas distintas e custos estimados de material substancialmente menores do que os propostos por métodos concorrentes. Curiosamente, essa relação custo-benefício surgiu mesmo sem o sistema ter sido explicitamente treinado para minimizar a dificuldade sintética. Em vez disso, sua tendência a gerar famílias de moléculas relacionadas, porém diversas, permitiu ao planejador de síntese reutilizar blocos de construção e sequências de reação, favorecendo naturalmente projetos com melhor escalabilidade no laboratório.
O que isso significa para medicamentos futuros
Para um público não especializado, a principal conclusão é que o EVOSYNTH oferece uma forma de buscar de maneira inteligente o imenso espaço de moléculas possíveis, procurando não apenas aquelas que atingem vários “interruptores” da doença ao mesmo tempo, mas também as que químicos podem produzir sem esforço heróico. Ao acoplar estreitamente previsões de atividade multitarget com checagens de segurança, penetração cerebral e praticidade sintética, a estrutura aproxima o desenho computacional de fármacos de produzir compostos reais e testáveis. Embora o trabalho atual se concentre em pares de alvos e dependa de estimativas computacionais de ligação em vez de dados experimentais completos, a abordagem é geral. Com refinamentos adicionais, sistemas similares podem ajudar a projetar uma nova geração de medicamentos multipropósito que sejam ao mesmo tempo biologicamente sofisticados e fabricáveis em escala.
Citação: Nguyen, V.T.D., Pham, P. & Hy, TS. Enabling multi-target drug discovery through latent evolutionary optimization and synthesis-aware prioritization (EVOSYNTH). Commun Chem 9, 133 (2026). https://doi.org/10.1038/s42004-026-01945-4
Palavras-chave: projeto de fármacos multitarget, descoberta de fármacos orientada por IA, otimização evolutiva, acessibilidade sintética, polifarmacologia