Clear Sky Science · de
Mehrfachziel-arzneimittelentdeckung ermöglichen durch latente evolutionäre Optimierung und synthese-bewusste Priorisierung (EVOSYNTH)
Warum intelligenteres Wirkstoffdesign wichtig ist
Viele schwere Erkrankungen, von Alzheimer bis Eierstockkrebs, entstehen nicht durch ein einzelnes fehlerhaftes Protein, sondern durch ganze Netze gestörter Signalwege. Solche Erkrankungen mit einem einzelnen Wirkstoff gegen ein Ziel zu behandeln, reicht oft nicht aus, während die Verabreichung mehrerer Medikamente Nebenwirkungen und komplizierte Dosierungspläne erzeugen kann. Diese Studie stellt EVOSYNTH vor, ein rechnerisches Framework, das darauf abzielt, einzelne Moleküle zu entwerfen, die mehrere krankheitsrelevante Ziele sicher und effektiv treffen können — und, was entscheidend ist, die Chemiker*innen tatsächlich im Labor herstellen können.
Von einzelnen Zielen zu vielen Schaltern
Die traditionelle Wirkstoffforschung hat vielfach nach „Magischen Kugeln“ gesucht: Verbindungen, die stark an ein Protein binden und alles andere unberührt lassen. Mittlerweile zeigt sich, dass dieser Ansatz bei komplexen Krankheiten mit zahlreichen Rückkopplungen und Umgehungswegen oft versagt. Mehrere Medikamente (Polypharmazie) können die Abdeckung verbessern, erhöhen aber das Risiko gefährlicher Wechselwirkungen, unvorhersehbarem Verhalten im Körper und belastenden Therapieplänen. Mehrziel-Wirkstoffe bieten einen Mittelweg: ein wohlüberlegtes Molekül, das mehrere Schlüsselorene gleichzeitig moduliert und idealerweise ein ganzes Netzwerk wieder in Richtung Gesundheit lenkt. Die Herausforderung besteht darin, solche Moleküle zu finden und zugleich sicherzustellen, dass sie praktisch synthetisierbar bleiben — eine Aufgabe, die von Hand extrem schwierig ist.
Eine digitale Evolutionseinheit für Moleküle
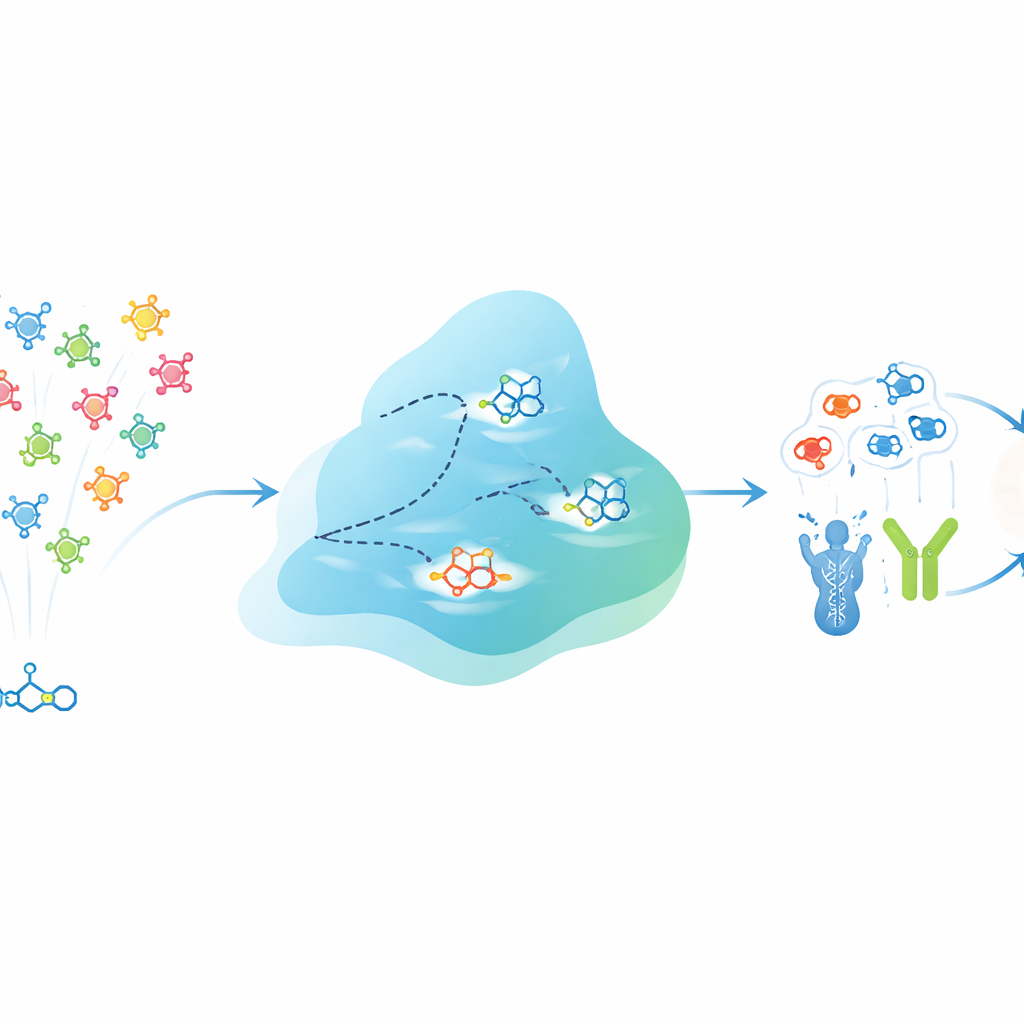
EVOSYNTH geht dieses Problem an, indem potenzielle Wirkstoffe als Population betrachtet werden, die innerhalb eines Computers „evolvieren“ kann. Anstatt reale Moleküle im Reagenzglas zu verändern, arbeitet das System in einem abstrakten, komprimierten Raum, der sowohl die Struktur jedes Moleküls als auch dessen vorhergesenes Verhalten gegenüber verschiedenen Protein-Zielen kodiert. Ein spezialisiertes neuronales Netzwerk erlernt diesen Raum, sodass nahe beieinander liegende Punkte tendenziell Moleküle mit ähnlicher Mehrziel-Aktivität repräsentieren. Ein Diffusionsprozess übernimmt die Rolle der Mutation und verändert diese Punkte sanft, um neue virtuelle Moleküle zu erzeugen. Nach jeder Runde werden Kandidaten dahingehend bewertet, wie stark sie voraussichtlich an mehrere gewählte Proteine binden, während harte Filter alle verworfen, die grundlegende Anforderungen an Wirkstoffähnlichkeit, Toxizität oder — bei Hirnerkrankungen — die Fähigkeit, die Blut-Hirn-Schranke zu überwinden, nicht erfüllen.
Wirkstoffe entwerfen, die tatsächlich herstellbar sind
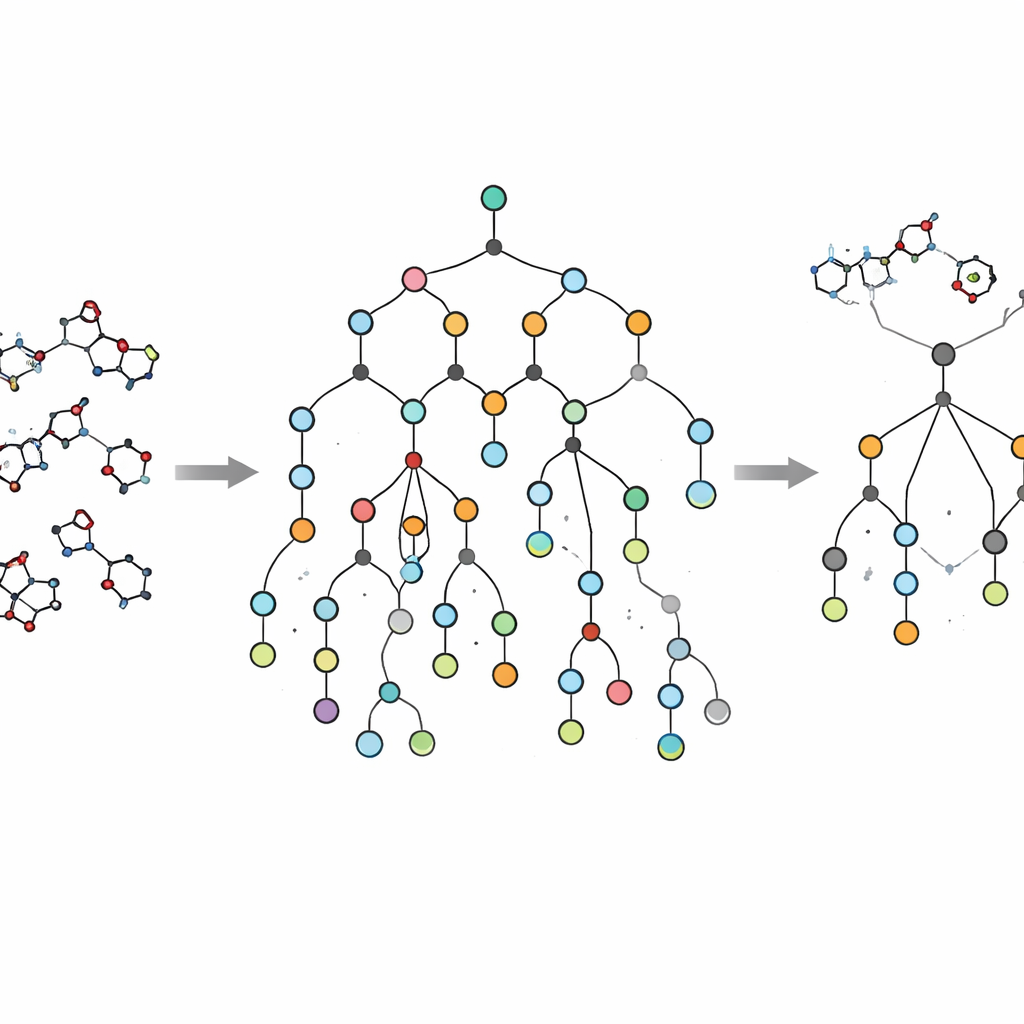
Eine wichtige Innovation von EVOSYNTH ist, dass es nicht bei virtuellen Aktivitätsvorhersagen stehen bleibt. Viele von KI-Modellen vorgeschlagene Moleküle sehen auf dem Bildschirm vielversprechend aus, sind aber in der Praxis prohibitiv schwierig oder teuer zu synthetisieren. Um diese Falle zu vermeiden, integrieren die Autor*innen ein Syntheseplanungs-System namens SPARROW in ihren Workflow. Dieses Werkzeug baut Reaktionsnetzwerke auf, die jedes Kandidatenmolekül mit leicht erhältlichen Ausgangsbausteinen verbinden und dabei Anzahl der Schritte, Kosten der Ausgangsmaterialien und Zuverlässigkeit einzelner Reaktionen abschätzen. Statt unmögliche Moleküle erst nachträglich zu verwerfen, nutzt EVOSYNTH diese netzwerkweiten Berechnungen zur Priorisierung von Kandidaten, die das beste Verhältnis zwischen therapeutischem Potenzial und realer Herstellbarkeit bieten — einschließlich der Möglichkeit, Zwischenprodukte wiederzuverwenden und Schritte über mehrere Spitzenkandidaten zu teilen.
Reale Tests bei Hirnerkrankungen und Krebs
Um zu demonstrieren, was EVOSYNTH leisten kann, wendeten die Forschenden es auf zwei anspruchsvolle Fälle an. Für Alzheimer suchten sie Moleküle, die sowohl JNK3 als auch GSK3β blockieren können — zwei Enzyme, die mit Nervenzellsterben und abnormer Proteinablagerung im Gehirn in Verbindung gebracht werden. Für Eierstockkrebs zielten sie auf ein Paar von Proteinen ab, die an Wachstumssignalen und DNA-Reparatur beteiligt sind, PI3K und PARP1, die sich als besonders wirksam erwiesen haben, wenn sie gemeinsam gehemmt werden. Ausgehend von bekannten Einziel-Wirkstoffen als „Seed“-Gerüste erzeugte EVOSYNTH über viele Generationen neue Strukturen und verfeinerte sie. Im Vergleich zu einer eng verwandten Methode und einem weiteren fortgeschrittenen generativen Modell produzierte EVOSYNTH durchgehend Kandidaten mit stärker vorhergesagter Aktivität gegen beide Ziele, größerer struktureller Vielfalt und geringerer Ähnlichkeit zum Ursprungsgerüst — Hinweise darauf, dass es wirklich neues chemisches Terrain erkundet statt das gleiche Motiv endlos zu modifizieren.
Power, Vielfalt und Kosten ins Gleichgewicht bringen
Als das Team die besten Moleküle durch die Brille der Synthese betrachtete, wurden die Vorteile ihres Ansatzes noch deutlicher. Unter realistischen Beschränkungen — es können nur etwa zehn Verbindungen für experimentelle Tests weiterverfolgt werden — verbanden EVOSYNTHs Top-Auswahlen höhere erwartete therapeutische Erträge mit weniger Reaktionsschritten, weniger unterschiedlichen Ausgangsstoffen und deutlich geringeren geschätzten Materialkosten als die Vorschläge konkurrierender Methoden. Interessanterweise trat diese Kosten-Effektivität auf, obwohl das System nicht explizit darauf trainiert war, die synthetische Schwierigkeit zu minimieren. Stattdessen ermöglichte seine Neigung, Familien verwandter, aber diverser Moleküle zu erzeugen, dem Syntheseplaner, Bausteine und Reaktionsabfolgen wiederzuverwenden und begünstigte so designs, die sich im Labor besser skalieren lassen würden.
Was das für zukünftige Medikamente bedeutet
Für Nicht-Spezialist*innen ist die Kernbotschaft, dass EVOSYNTH einen Weg bietet, intelligent durch den gewaltigen Raum möglicher Moleküle zu suchen — und zwar nicht nur nach solchen, die mehrere Krankheits-Schalter gleichzeitig treffen, sondern auch nach solchen, die Chemiker*innen ohne heldenhaften Aufwand herstellen können. Durch die enge Kopplung von Vorhersagen zur Mehrzielaktivität mit Prüfungen zu Sicherheit, Hirndurchdringung und synthetischer Praktikabilität rückt das Framework die rechnergestützte Wirkstoffentwicklung einen Schritt näher an die Erzeugung realer, testbarer Verbindungen. Während die aktuelle Arbeit sich auf Zielpaare konzentriert und auf computerbasierte Bindungsschätzungen statt vollständiger experimenteller Daten beruht, ist der Ansatz allgemein. Mit weiterer Verfeinerung könnten ähnliche Systeme helfen, eine neue Generation von Mehrzweck-Wirkstoffen zu entwerfen, die biologisch anspruchsvoll und in der Herstellung skalierbar sind.
Zitation: Nguyen, V.T.D., Pham, P. & Hy, TS. Enabling multi-target drug discovery through latent evolutionary optimization and synthesis-aware prioritization (EVOSYNTH). Commun Chem 9, 133 (2026). https://doi.org/10.1038/s42004-026-01945-4
Schlüsselwörter: Mehrziel-Arzneimittel-Design, KI-gestützte Wirkstoffforschung, evolutionäre Optimierung, synthetische Zugänglichkeit, Polypharmakologie