Clear Sky Science · fr
Permettre la découverte de médicaments multi-cibles via l’optimisation évolutive latente et la priorisation consciente de la synthèse (EVOSYNTH)
Pourquoi concevoir des médicaments plus intelligents est important
De nombreuses maladies graves, de la maladie d’Alzheimer au cancer de l’ovaire, ne résultent pas d’une seule protéine défaillante mais d’un réseau entier de voies perturbées. Traiter ces affections avec un médicament unique ciblant une seule cible est souvent insuffisant, tandis que prescrire plusieurs médicaments peut provoquer des effets secondaires toxiques et des protocoles posologiques complexes. Cette étude présente EVOSYNTH, un cadre computationnel visant à concevoir des molécules uniques capables d’atteindre en toute sécurité et efficacement plusieurs cibles liées à la maladie simultanément — et, aspect crucial, que les chimistes peuvent réellement synthétiser en laboratoire.
Des cibles uniques à plusieurs commutateurs
La découverte de médicaments traditionnelle a largement recherché des « balles magiques » qui se lient fortement à une protéine et n’affectent rien d’autre. Avec le temps, il est apparu que cette approche échoue face aux maladies complexes impliquant de multiples boucles de rétroaction et voies de secours. Ajouter des médicaments — la stratégie de polypharmacie — peut améliorer la couverture mais augmente le risque d’interactions médicamenteuses dangereuses, de comportements imprévisibles dans l’organisme et d’un fardeau thérapeutique élevé. Les médicaments multi-cibles offrent une voie intermédiaire : une seule molécule conçue avec soin qui module simultanément plusieurs protéines clés, idéalement en réorientant l’ensemble du réseau vers un état sain. Le défi est que trouver de telles molécules, tout en garantissant qu’elles restent praticables à synthétiser, est extrêmement difficile à réaliser manuellement.
Un moteur d’évolution numérique pour molécules
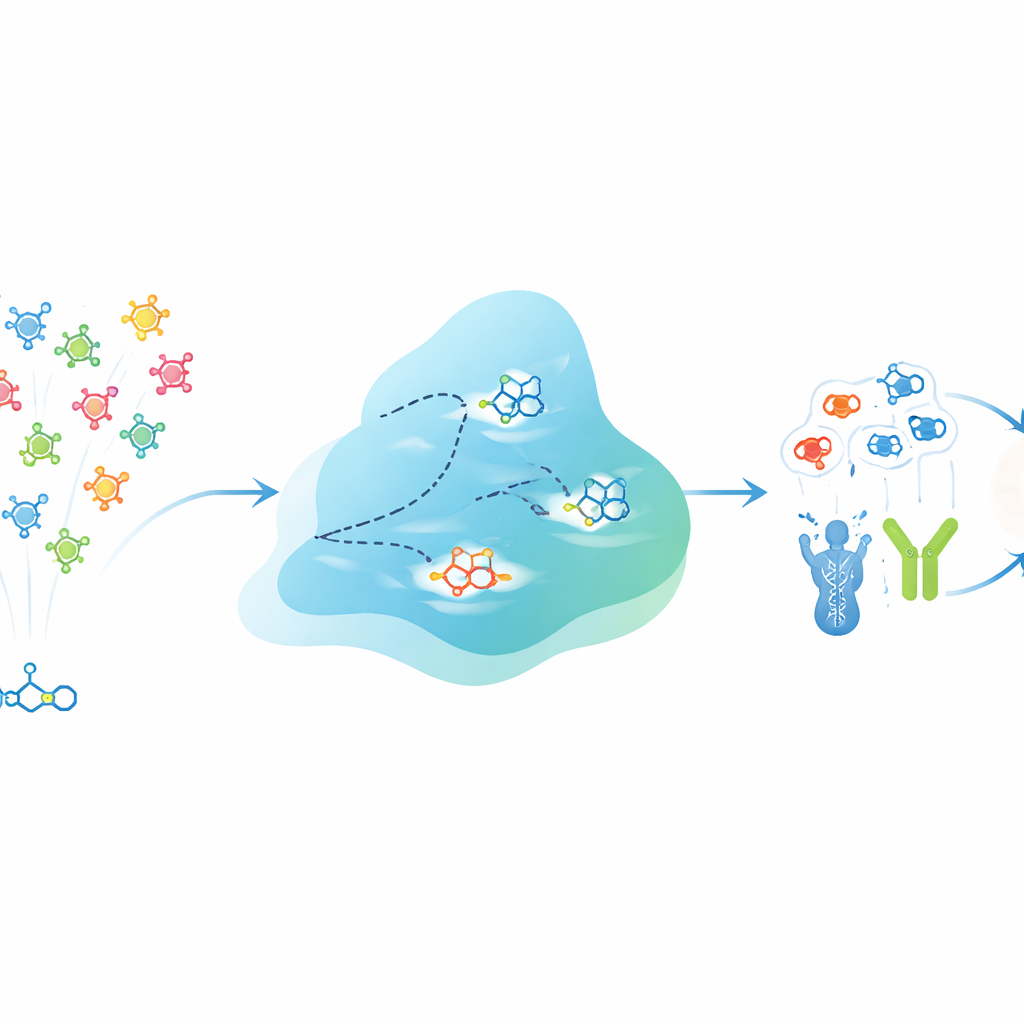
EVOSYNTH relève ce défi en traitant les candidats-médicaments comme une population susceptible « d’évoluer » à l’intérieur d’un ordinateur. Plutôt que d’altérer de véritables molécules dans un tube à essai, le système opère dans un espace abstrait et compressé qui encode à la fois la structure de chaque molécule et son comportement prédit vis‑à‑vis de différentes cibles protéiques. Un réseau de neurones spécialisé apprend cet espace de sorte que des points proches correspondent en général à des molécules ayant des activités multi-cibles similaires. Un processus de diffusion joue ensuite le rôle de mutation, perturbant légèrement ces points pour générer de nouvelles molécules virtuelles. Après chaque cycle, les candidats sont évalués selon la force prédite de leur liaison à plusieurs protéines sélectionnées simultanément, tandis que des filtres stricts écartent ceux qui ne satisfont pas aux exigences de base en matière de propriétés physico-chimiques, de toxicité ou, pour les maladies cérébrales, de capacité à traverser la barrière hémato‑encéphalique.
Concevoir des médicaments qui peuvent réellement être fabriqués
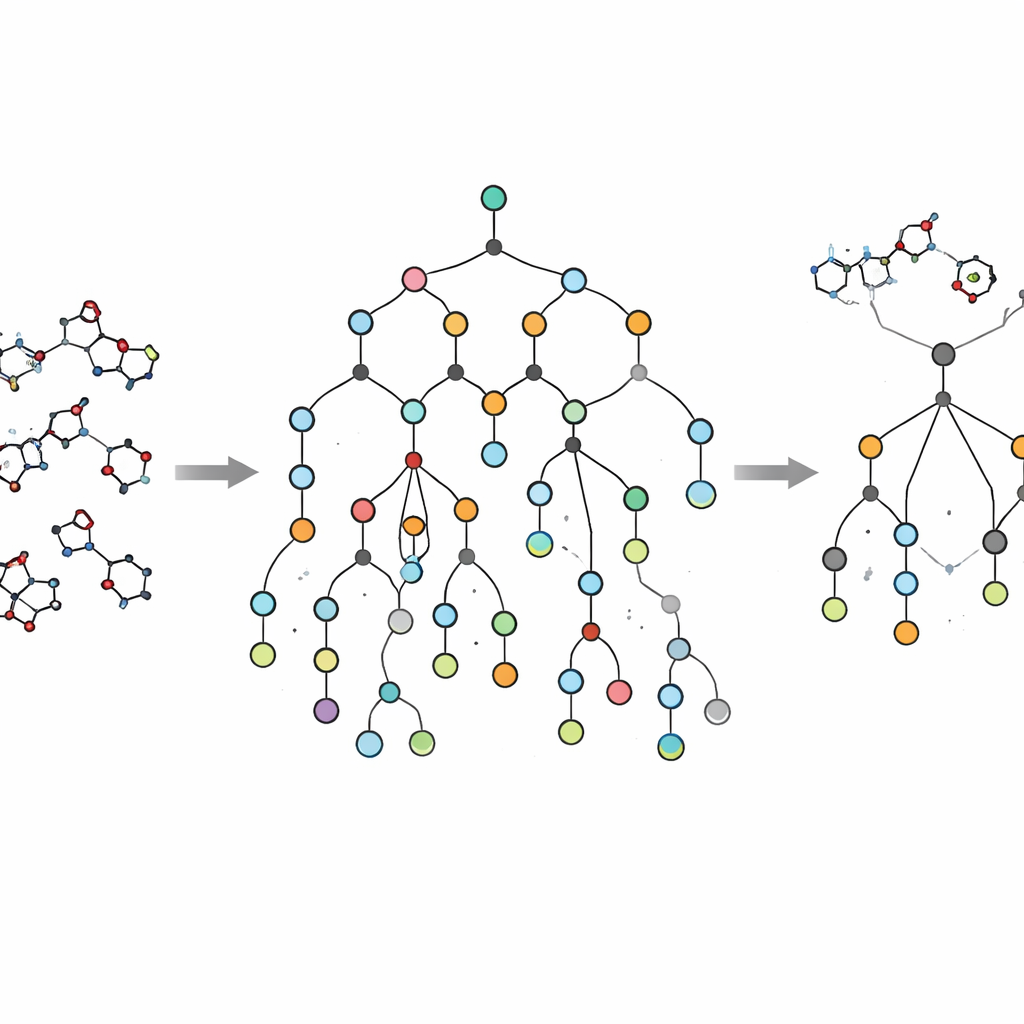
Une innovation importante d’EVOSYNTH est qu’il ne s’arrête pas à l’activité virtuelle. De nombreuses molécules proposées par des modèles d’IA semblent prometteuses à l’écran mais sont prohibitivement difficiles ou coûteuses à synthétiser. Pour éviter cet écueil, les auteurs intègrent dans leur flux de travail un système de planification de synthèse nommé SPARROW. Cet outil construit des réseaux de réactions reliant chaque molécule candidate à des blocs de construction facilement achetables, estimant le nombre d’étapes, le coût des matières premières et la fiabilité de chaque réaction. Plutôt que de rejeter a posteriori les molécules impossibles, EVOSYNTH utilise ces calculs à l’échelle du réseau pour prioriser les candidats offrant le meilleur compromis entre promesse thérapeutique et fabriquabilité réelle, y compris les opportunités de réutiliser des intermédiaires et de partager des étapes entre plusieurs composés en tête de liste.
Tests réalistes en maladies cérébrales et en cancer
Pour démontrer ce dont EVOSYNTH est capable, les chercheurs l’ont appliqué à deux cas-tests exigeants. Pour la maladie d’Alzheimer, ils ont cherché des molécules capables de bloquer à la fois JNK3 et GSK3β, deux enzymes impliquées dans la mort neuronale et l’accumulation anormale de protéines dans le cerveau. Pour le cancer de l’ovaire, ils ont ciblé une paire de protéines impliquées dans la signalisation de croissance et la réparation de l’ADN, PI3K et PARP1, qui ont montré une efficacité particulière lorsqu’elles sont inhibées simultanément. À partir de médicaments connus ciblant une seule protéine comme échafaudages « graines », EVOSYNTH a généré et affiné de nouvelles structures sur de nombreuses générations. Comparé à une méthode étroitement liée et à un autre modèle génératif avancé, EVOSYNTH a constamment produit des candidats avec une activité prédite plus forte sur les deux cibles, une plus grande variété structurelle et une similarité plus faible à l’échafaudage d’origine — autant d’indications qu’il explore de nouveaux territoires chimiques plutôt que d’ajuster indéfiniment le même motif.
Équilibrer puissance, diversité et coût
Lorsque l’équipe a examiné les meilleures molécules sous l’angle de la synthèse, les avantages de leur approche sont devenus encore plus évidents. Dans des limites réalistes — seulement une dizaine de composés peuvent être soumis aux tests expérimentaux — les meilleures sélections d’EVOSYNTH combinaient un rendement thérapeutique attendu plus élevé avec moins d’étapes de réaction, moins de matières premières distinctes et des coûts de matériaux estimés nettement inférieurs à ceux proposés par les méthodes concurrentes. Fait intéressant, cette efficacité en coût est apparue alors même que le système n’avait pas été explicitement entraîné pour minimiser la difficulté synthétique. Au contraire, sa propension à générer des familles de molécules apparentées mais diversifiées a permis au planificateur de synthèse de réutiliser des blocs de construction et des séquences réactionnelles, favorisant naturellement des conceptions mieux extensibles en laboratoire.
Ce que cela signifie pour les médicaments du futur
Pour un non-spécialiste, l’essentiel est que EVOSYNTH offre un moyen de parcourir intelligemment l’immense espace des molécules possibles, en recherchant non seulement celles qui activent plusieurs commutateurs de la maladie simultanément, mais aussi celles que les chimistes peuvent produire sans efforts herculéens. En couplant étroitement les prédictions d’activité multi‑cible à des vérifications de sécurité, de pénétration cérébrale et de praticabilité de synthèse, ce cadre rapproche la conception computationnelle de médicaments de la production de composés réels et testables. Si le travail actuel se concentre sur des paires de cibles et s’appuie sur des estimations informatiques de liaison plutôt que sur des données expérimentales complètes, l’approche est générale. Avec des raffinements supplémentaires, des systèmes similaires pourraient aider à concevoir une nouvelle génération de médicaments polyfonctionnels à la fois biologiquement sophistiqués et manufacturables à grande échelle.
Citation: Nguyen, V.T.D., Pham, P. & Hy, TS. Enabling multi-target drug discovery through latent evolutionary optimization and synthesis-aware prioritization (EVOSYNTH). Commun Chem 9, 133 (2026). https://doi.org/10.1038/s42004-026-01945-4
Mots-clés: conception de médicaments multi-cibles, découverte de médicaments pilotée par IA, optimisation évolutive, accessibilité synthétique, polypharmacologie