Clear Sky Science · es
Habilitar el descubrimiento de fármacos multiobjetivo mediante optimización evolutiva latente y priorización consciente de la síntesis (EVOSYNTH)
Por qué importa diseñar medicinas más inteligentes
Muchas enfermedades graves, desde el Alzheimer hasta el cáncer de ovario, no se deben a una única proteína defectuosa sino a redes enteras de rutas alteradas. Tratar estas condiciones con un solo fármaco dirigido a un objetivo suele ser insuficiente, mientras que administrar múltiples medicamentos puede provocar efectos secundarios tóxicos y regímenes de dosificación complejos. Este estudio presenta EVOSYNTH, un marco computacional que pretende diseñar moléculas únicas capaces de actuar de forma segura y eficaz sobre varios objetivos relacionados con la enfermedad a la vez y, crucialmente, que los químicos puedan realmente sintetizar en el laboratorio.
De objetivos únicos a múltiples interruptores
El descubrimiento tradicional de fármacos ha perseguido en gran medida compuestos “bala mágica” que se unen fuertemente a una proteína y no afectan a las demás. Con el tiempo ha quedado claro que este enfoque tiene dificultades frente a enfermedades complejas que implican múltiples bucles de retroalimentación y rutas de reserva. Añadir más fármacos —la estrategia de polifarmacia— puede mejorar la cobertura, pero aumenta el riesgo de interacciones peligrosas entre medicamentos, comportamientos impredecibles en el organismo y tratamientos gravosos. Los fármacos multiobjetivo ofrecen un camino intermedio: una molécula diseñada con criterio que modula varias proteínas clave a la vez, idealmente orientando una red completa de vuelta hacia la salud. El desafío es que encontrar tales moléculas, y asegurarse de que sigan siendo prácticas de sintetizar, es extremadamente difícil de hacer a mano.
Un motor de evolución digital para moléculas
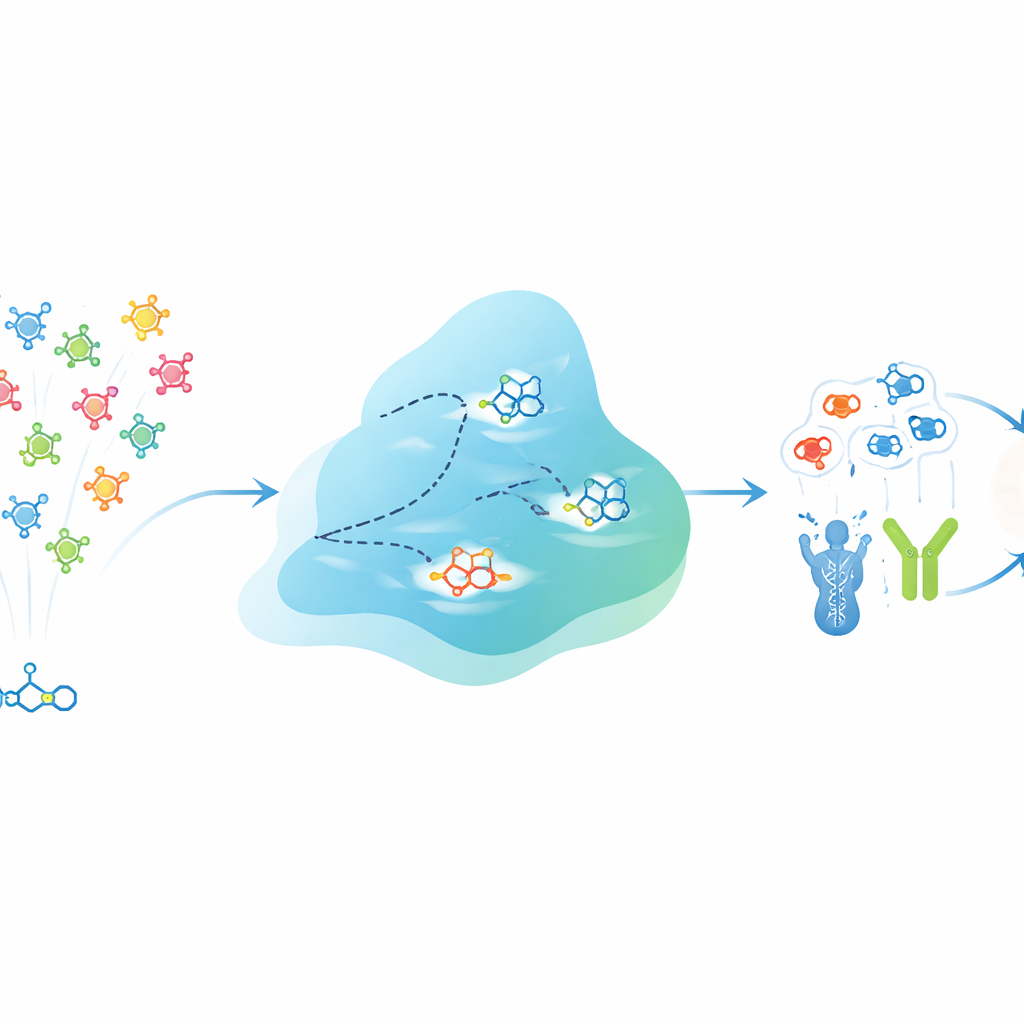
EVOSYNTH aborda este reto tratando a los candidatos a fármaco como una población que puede “evolucionar” dentro de un ordenador. En lugar de alterar moléculas reales en un tubo de ensayo, el sistema trabaja en un espacio abstracto y comprimido que codifica tanto la estructura de cada molécula como su comportamiento predicho frente a distintos objetivos proteicos. Una red neuronal especializada aprende este espacio para que puntos cercanos tiendan a corresponder a moléculas con actividad multiobjetivo similar. Un proceso de difusión hace el papel de mutación, perturbando suavemente estos puntos para generar nuevas moléculas virtuales. Tras cada ronda, los candidatos se evalúan por la fuerza con la que se predice que se unirán a varias proteínas elegidas a la vez, mientras que filtros estrictos descartan aquellos que no cumplen requisitos básicos de semejanza a fármaco, toxicidad o, en enfermedades cerebrales, la capacidad de cruzar la barrera hematoencefálica.
Diseñar fármacos que realmente se puedan fabricar
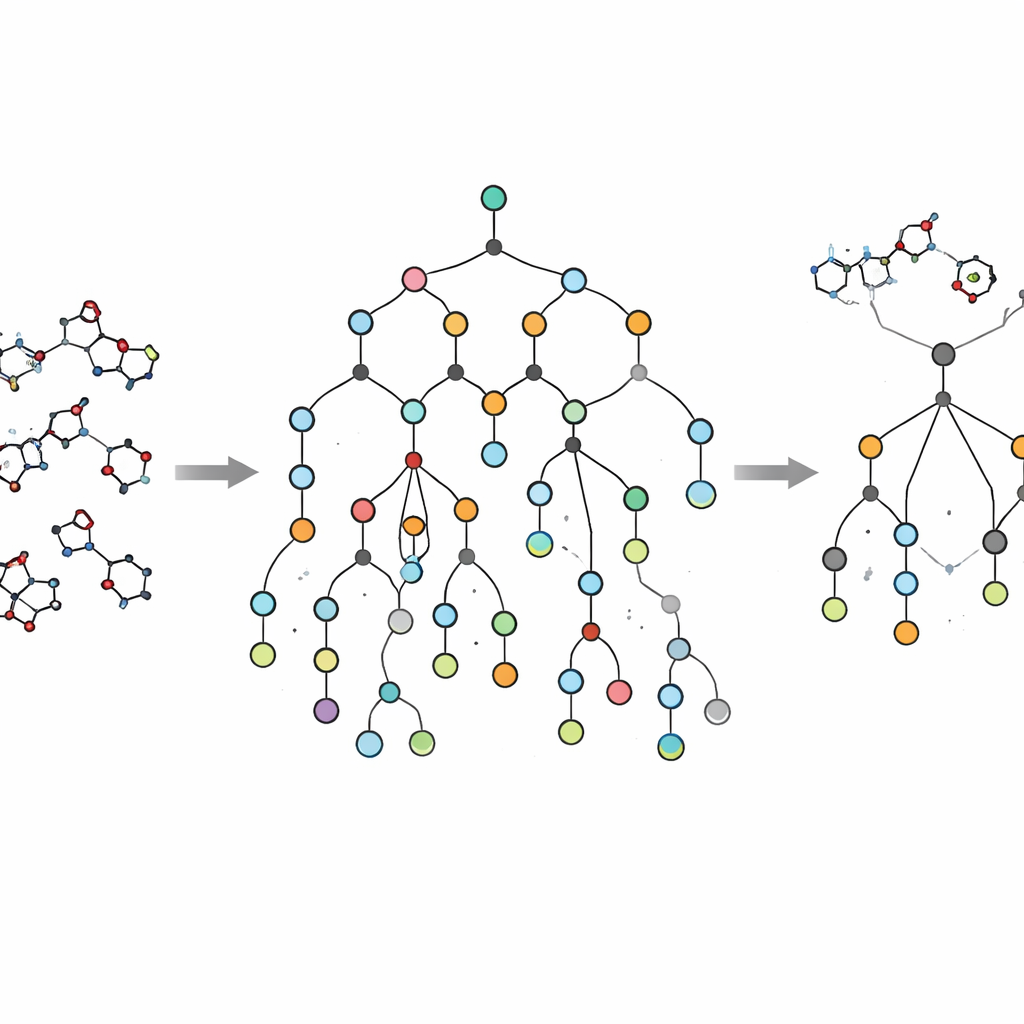
Una innovación importante de EVOSYNTH es que no se queda en la actividad virtual. Muchas moléculas propuestas por modelos de inteligencia artificial parecen prometedoras en pantalla pero son prohibitivamente difíciles o caras de sintetizar. Para evitar esta trampa, los autores integran un sistema de planificación sintética llamado SPARROW en su flujo de trabajo. Esta herramienta construye redes de reacciones que conectan cada molécula candidata con bloques de construcción fácilmente comprables, estimando el número de pasos, el coste de los materiales iniciales y la fiabilidad de cada reacción. En lugar de simplemente rechazar moléculas imposibles a posteriori, EVOSYNTH utiliza estos cálculos en toda la red para priorizar candidatos que ofrecen el mejor equilibrio entre promesa terapéutica y capacidad de fabricación en el mundo real, incluidas oportunidades para reutilizar intermedios y compartir pasos entre varios compuestos principales.
Pruebas realistas en enfermedades cerebrales y cáncer
Para demostrar lo que puede hacer EVOSYNTH, los investigadores lo aplicaron a dos casos de prueba exigentes. Para la enfermedad de Alzheimer, buscaron moléculas que pudieran bloquear tanto JNK3 como GSK3β, dos enzimas implicadas en la muerte neuronal y la acumulación anómala de proteínas en el cerebro. Para el cáncer de ovario, se dirigieron a un par de proteínas implicadas en la señalización de crecimiento y la reparación del ADN, PI3K y PARP1, que han demostrado funcionar especialmente bien cuando se inhiben juntas. Partiendo de fármacos conocidos de objetivo único como andamiajes “semilla”, EVOSYNTH generó y refinó nuevas estructuras a lo largo de muchas generaciones. En comparación con un método estrechamente relacionado y otro modelo generativo avanzado, EVOSYNTH produjo de forma consistente moléculas candidatas con mayor actividad predicha en ambos objetivos, mayor variedad estructural y menor similitud con el andamiaje original —señales de que está explorando territorio químico genuinamente nuevo en lugar de modificar eternamente el mismo motivo.
Equilibrando potencia, diversidad y coste
Cuando el equipo examinó las mejores moléculas desde la perspectiva de la síntesis, las ventajas de su enfoque se hicieron aún más claras. Bajo límites realistas —solo alrededor de diez compuestos pueden avanzar a ensayos experimentales— las selecciones principales de EVOSYNTH combinaron un mayor rendimiento terapéutico esperado con menos pasos de reacción, menos materiales de partida distintos y costes de material estimados sustancialmente más bajos que los propuestos por métodos competidores. Curiosamente, esta rentabilidad surgió aunque el sistema no se entrenó explícitamente para minimizar la dificultad sintética. En su lugar, su tendencia a generar familias de moléculas relacionadas pero diversas permitió al planificador sintético reutilizar bloques de construcción y secuencias de reacción, favoreciendo de forma natural diseños que escalarían mejor en el laboratorio.
Qué significa esto para las medicinas futuras
Para un público no especializado, la idea clave es que EVOSYNTH ofrece una forma de buscar de manera inteligente en el inmenso espacio de moléculas posibles, buscando no solo aquellas que actúen sobre varios interruptores de la enfermedad a la vez, sino también las que los químicos pueden fabricar sin esfuerzos heroicos. Al acoplar estrechamente las predicciones de actividad multiobjetivo con comprobaciones de seguridad, penetración cerebral y practicidad sintética, el marco acerca el diseño computacional de fármacos un paso más a producir compuestos reales y comprobables. Aunque el trabajo actual se centra en pares de objetivos y se basa en estimaciones computacionales de unión más que en datos experimentales completos, el enfoque es general. Con mayor refinamiento, sistemas similares podrían ayudar a diseñar una nueva generación de fármacos polivalentes que sean tanto biológicamente sofisticados como fabricables a escala.
Cita: Nguyen, V.T.D., Pham, P. & Hy, TS. Enabling multi-target drug discovery through latent evolutionary optimization and synthesis-aware prioritization (EVOSYNTH). Commun Chem 9, 133 (2026). https://doi.org/10.1038/s42004-026-01945-4
Palabras clave: diseño de fármacos multiobjetivo, descubrimiento de fármacos impulsado por IA, optimización evolutiva, accesibilidad sintética, polifarmacología