Clear Sky Science · ru
Обеспечение многоматочной разработки препаратов через латентную эволюционную оптимизацию и приоритизацию с учётом синтеза (EVOSYNTH)
Почему важно проектировать более умные лекарства
Многие тяжёлые заболевания, от болезни Альцгеймера до рака яичников, возникают не из‑за одной дефектной белковой цели, а из‑за целых сетей нарушенных путей. Лечение таких состояний одним препаратом, направленным на одну мишень, часто оказывается недостаточным, тогда как назначение пациентам нескольких лекарств приводит к токсическим побочным эффектам и сложным схемам дозирования. В этой работе представлена EVOSYNTH — вычислительная платформа, цель которой — проектировать одиночные молекулы, способные безопасно и эффективно воздействовать сразу на несколько связанных с болезнью мишеней, и, что не менее важно, которые химики реально смогут синтезировать в лаборатории.
От одиночных мишеней к множеству переключателей
Традиционная разработка лекарств в основном стремилась к «волшебным пулям» — соединениям, которые сильно связываются с одним белком и не затрагивают остальное. Со временем выяснилось, что этот подход слабо работает при сложных заболеваниях с множественными петлями обратной связи и запасными путями. Добавление большего числа препаратов — стратегия полифармакотерапии — может улучшить покрытие, но повышает риск опасных взаимодействий между лекарствами, непредсказуемого поведения в организме и обременительных режимов лечения. Многоцелевые препараты предлагают средний путь: одна продуманная молекула, одновременно модулирующая несколько ключевых белков и, в идеале, направляющая всю сеть обратно к нормальному состоянию. Проблема в том, что нахождение таких молекул и обеспечение их практической синтезируемости вручную чрезвычайно затруднительно.
Цифровой двигатель эволюции для молекул
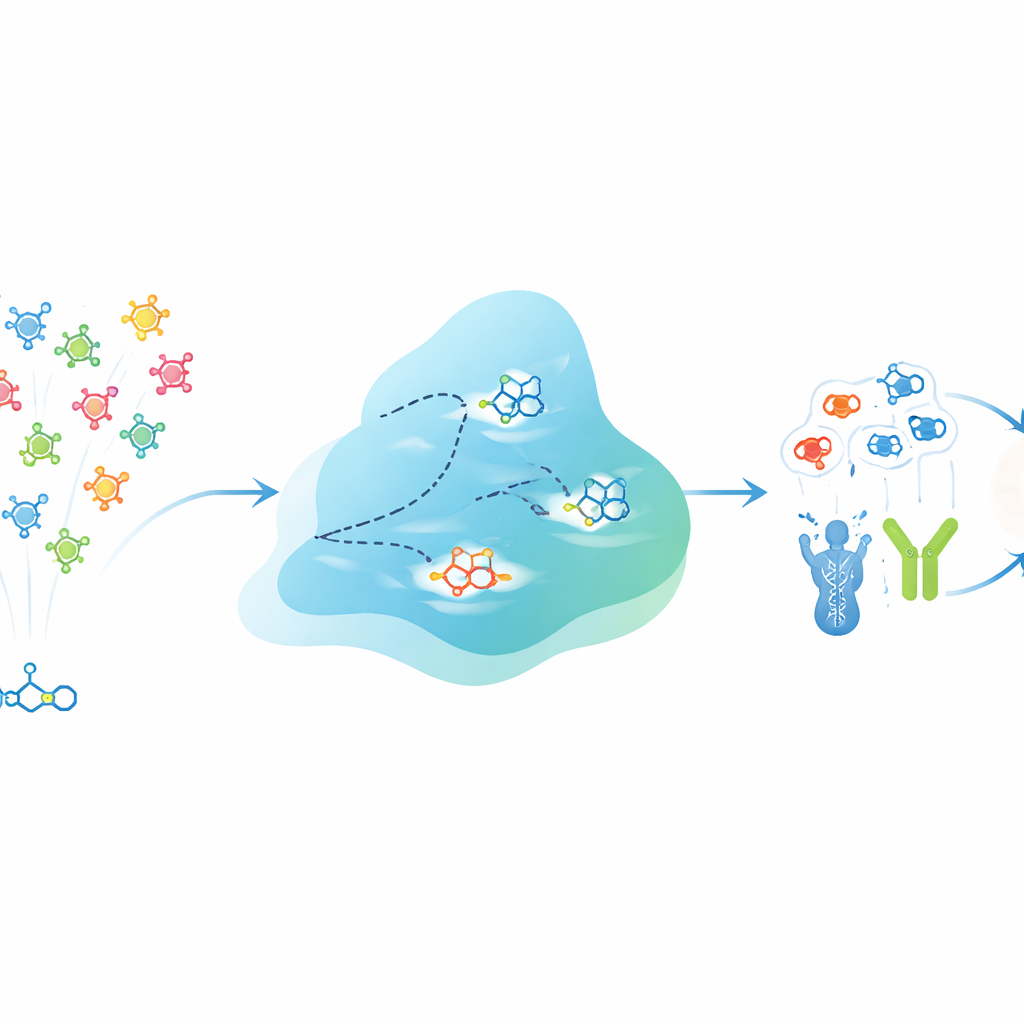
EVOSYNTH решает эту задачу, рассматривая потенциальные препараты как популяцию, которая может «эволюционировать» внутри компьютера. Вместо изменения реальных молекул в пробирке система работает в абстрактном, сжатом пространстве, кодирующем и структуру каждой молекулы, и её предсказанное поведение по отношению к разным белковым мишеням. Специализированная нейронная сеть изучает это пространство так, что близкие точки обычно соответствуют молекулам с похожей многоцелевой активностью. Процесс диффузии выполняет роль мутации, мягко возмущая эти точки для генерации новых виртуальных молекул. После каждого цикла кандидаты оцениваются по тому, насколько сильно они, как ожидается, связываются с несколькими выбранными белками одновременно, а жёсткие фильтры отбрасывают те, которые не соответствуют базовым требованиям лекарственности, токсичности или, для заболеваний мозга, способности пересекать гематоэнцефалический барьер.
Проектирование препаратов, которые реально можно сделать
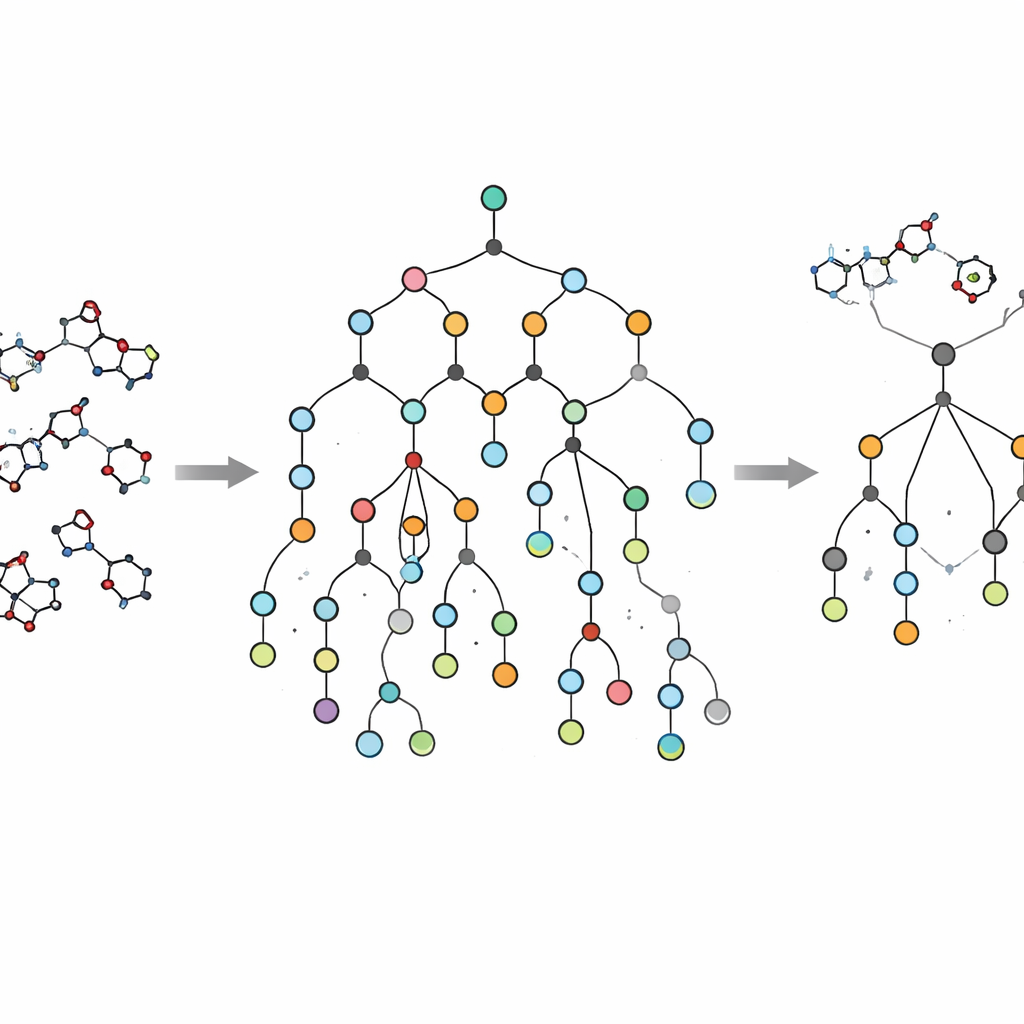
Важное новшество EVOSYNTH — то, что система не останавливается на виртуальной активности. Многие предложенные ИИ‑моделями молекулы выглядят перспективно на экране, но оказались бы чрезмерно сложны или дороги для синтеза. Чтобы избежать этой ловушки, авторы интегрировали в рабочий процесс систему планирования синтеза SPARROW. Этот инструмент строит сети реакций, связывая каждую кандидат‑молекулу с легко приобретаемыми исходными блоками, оценивая число шагов, стоимость стартовых материалов и надёжность каждой реакции. Вместо того чтобы просто отбрасывать невозможные в синтезе молекулы постфактум, EVOSYNTH использует эти расчёты по всей сети для приоритизации кандидатов, предлагающих лучшую компромисс между терапевтическим потенциалом и реальной производительностью, включая возможности повторного использования промежуточных соединений и объединения этапов для нескольких ведущих соединений.
Реалистичные испытания в заболеваниях мозга и раке
Чтобы продемонстрировать возможности EVOSYNTH, исследователи применили её к двум требовательным кейсам. Для болезни Альцгеймера они искали молекулы, способные блокировать как JNK3, так и GSK3β — два фермента, связанные со смертью нервных клеток и аномальным накоплением белков в мозге. Для рака яичников целью стали пара белков, вовлечённых в сигналы роста и репарацию ДНК, PI3K и PARP1, которые показали особенно хорошую совместную эффективность при их ингибировании. Начиная с известных препаратов, нацеленных на одну мишень, в качестве «сидовых» каркасов, EVOSYNTH генерировала и оттачивала новые структуры в течение многих поколений. По сравнению с близким по принципу методом и ещё одной продвинутой генеративной моделью, EVOSYNTH последовательно давала кандидаты с более сильной предсказанной активностью по обеим мишеням, большим структурным разнообразием и меньшим сходством с исходным каркасом — признаки того, что система исследует действительно новую химическую территорию, а не бесконечно подгоняет один и тот же мотив.
Баланс силы, разнообразия и стоимости
Когда команда проанализировала лучшие молекулы с точки зрения синтеза, преимущества их подхода стали ещё очевиднее. В рамках реалистичных ограничений — в экспериментальную проверку можно отправить всего около десяти соединений — лучшие подборки EVOSYNTH сочетали более высокий ожидаемый терапевтический эффект с меньшим числом реакционных шагов, меньшим количеством различных исходных материалов и значительно более низкой оценочной стоимостью материалов по сравнению с предложениями конкурентов. Примечательно, что эта экономичность проявилась несмотря на то, что система явно не обучалась минимизировать сложность синтеза. Скорее, её склонность генерировать семейства родственных, но разнообразных молекул позволяла планировщику синтеза переиспользовать блоки и последовательности реакций, естественным образом предпочитая конструкции, которые лучше масштабируются в лаборатории.
Что это значит для будущих лекарств
Для неспециалиста главный вывод таков: EVOSYNTH предоставляет способ разумно исследовать огромное пространство возможных молекул, искать не только те, что одновременно переключают несколько болезненных узлов, но и те, которые химики смогут синтезировать без героических усилий. Плотно связывая предсказания многоцелевой активности с проверками безопасности, проникновения в мозг и практичности синтеза, эта платформа приближает вычислительную разработку лекарств к созданию реальных, тестируемых соединений. Хотя текущая работа сосредоточена на парах мишеней и опирается на вычислительные оценки связывания, а не на полные экспериментальные данные, подход является общим. При дальнейшем совершенствовании подобные системы могут помочь спроектировать новое поколение многофункциональных препаратов, которые одновременно биологически изощрённы и производимы в масштабе.
Цитирование: Nguyen, V.T.D., Pham, P. & Hy, TS. Enabling multi-target drug discovery through latent evolutionary optimization and synthesis-aware prioritization (EVOSYNTH). Commun Chem 9, 133 (2026). https://doi.org/10.1038/s42004-026-01945-4
Ключевые слова: разработка многоцелевых лекарств, поиск лекарств с помощью ИИ, эволюционная оптимизация, синтетическая доступность, полифармакология