Clear Sky Science · sv
Metaheuristisk optimering av djupa CNN:er för flerkategori-diagnostik av livmoderhalscancer och lymfom
Smartare verktyg för att upptäcka cancer tidigt
För många kommer en cancerdiagnos fortfarande för sent, när behandlingen är svårare och överlevnadschanserna minskar. Läkare använder redan mikroskop och datorer för att granska vävnadsprover, men att lära maskiner att skilja åt cancersorter som ser lika ut är förvånansvärt svårt. Denna studie undersöker hur konstgjord intelligens kan göras mycket mer pålitlig för att upptäcka två allvarliga sjukdomar, livmoderhalscancer och lymfom, genom att låta naturinspirerade sökstrategier automatiskt finjustera ett kraftfullt bildanalysnätverk.
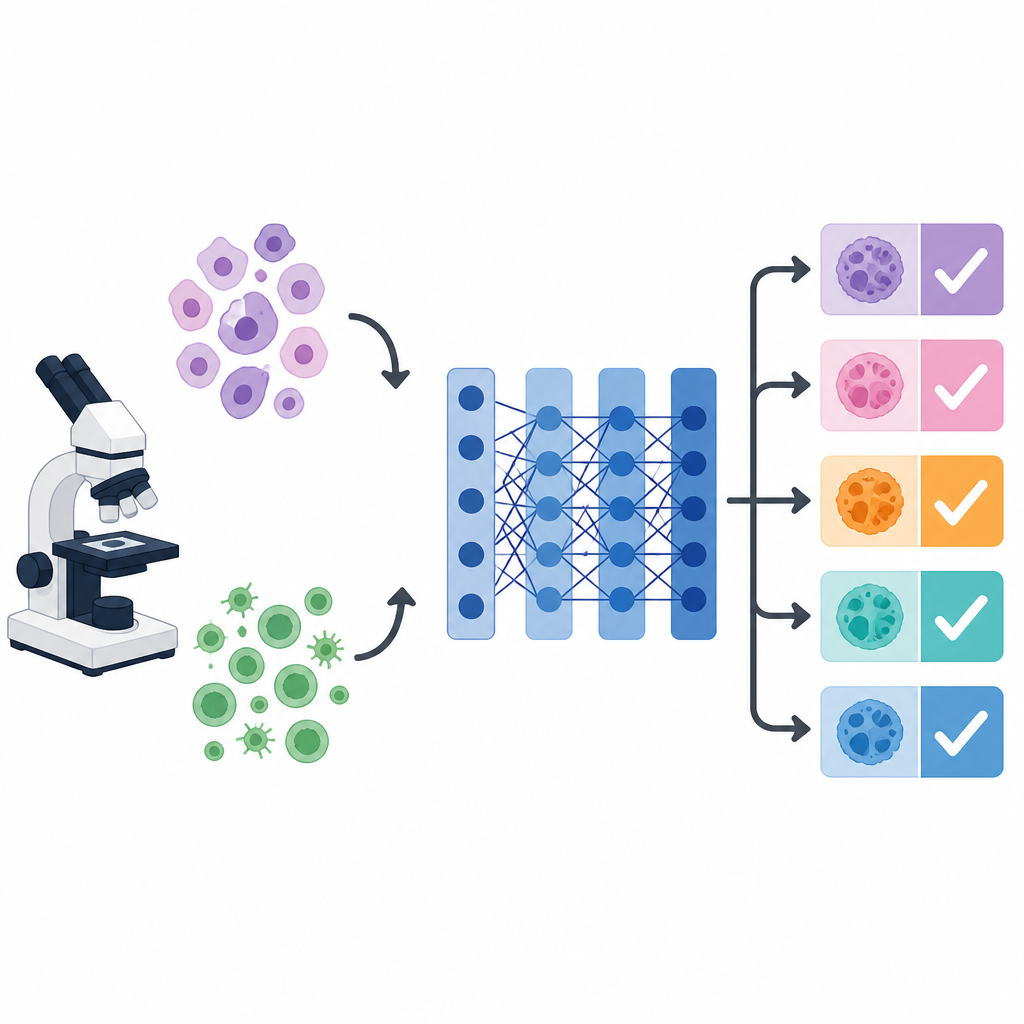
Varför cancerbilder förvirrar datorer
Under mikroskopet kan celler från olika cancerformer likna varandra, samtidigt som celler från samma cancer kan variera kraftigt i form, färg och textur. Detta visuella kaos gör det svårt för både människor och maskiner att ge konsekventa diagnoser. Djupinlärningssystem, särskilt ett populärt bildnätverk kallat VGG 16, kan lära sig att upptäcka användbara visuella mönster. Men deras prestanda beror starkt på många dolda inställningar, såsom inlärningshastighet, batchstorlek och hur starkt modellen regulariseras. Dessa inställningar, kallade hyperparametrar, väljs oftast manuellt eller lämnas på standardvärden, vilket kan begränsa noggrannheten, särskilt när målet är att skilja mellan flera cancertyper samtidigt.
Låna styrka från stora data utan att behöva dem
Medicinska bilddatamängder är ofta små eftersom högkvalitativa märkta prover är svåra och kostsamma att samla in. För att komma runt detta förlitade sig forskarna på transfer learning. De utgick från ett VGG 16-nätverk som tränats på en mycket stor allmän bildsamling och återanvände dess tidiga lager som en funktions-extraktör för cellbilder. De la sedan till anpassade lager för den nya uppgiften. Teamet arbetade med två publika samlingar: en dataset för livmoderhalscancer med fem cellkategorier och en för lymfom med tre undertyper. Varje ursprunglig datamängd hade under tusen bilder, så författarna utökade dem genom noggrann augmentation, såsom små rotationer, förskjutningar, zoom, ljusstyrkeändringar och speglingar, för att skapa tiotusentals varierade träningsexempel.
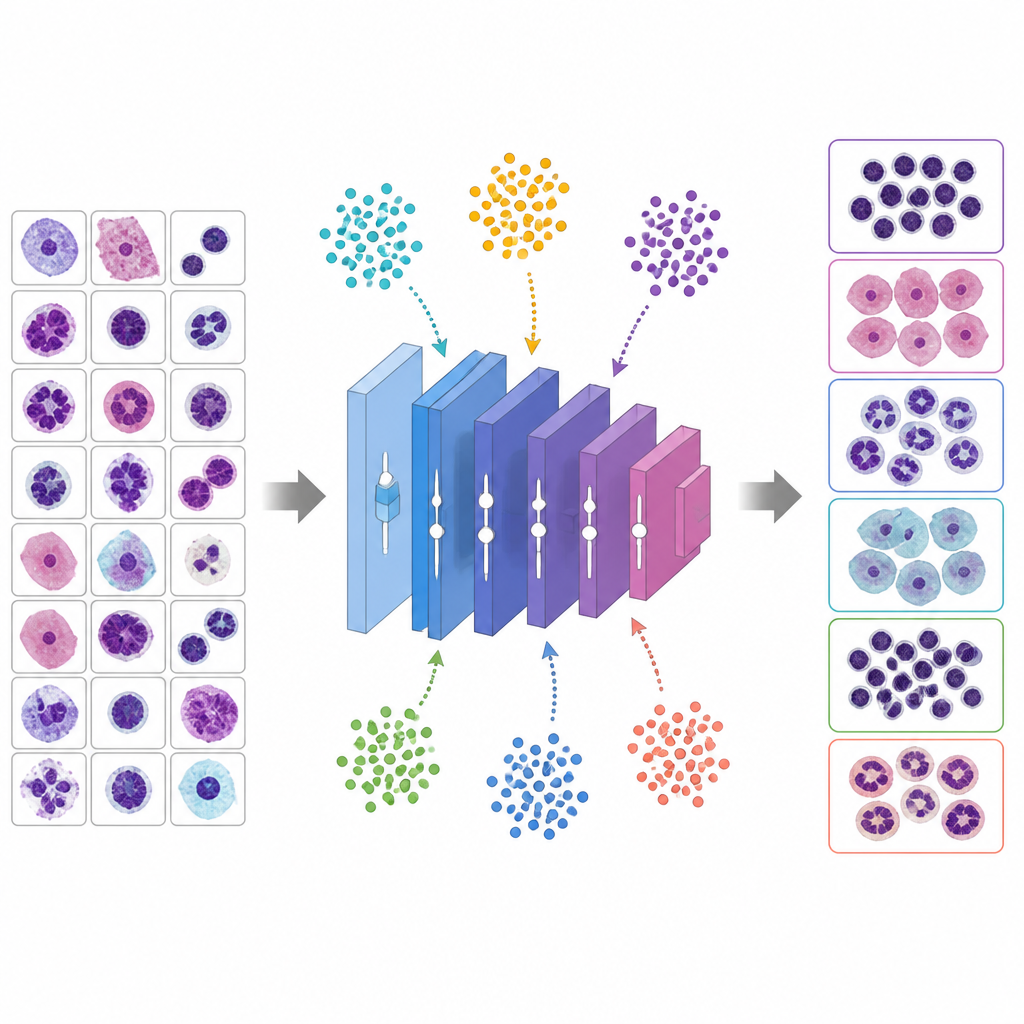
Låta virtuella djur ställa in rattarna
I stället för att gissa bra hyperparametrar använder studien sex metaheuristiska algoritmer inspirerade av djurbeteende och evolution för att söka efter de bästa inställningarna. I dessa metoder är varje kandidatlösning som ett väsen som utforskar ett landskap av möjligheter. Whale Optimization Algorithm härmar hur knölvalar spiralar runt sitt byte, Grey Wolf Optimizer modellerar vargar som omsluter och spårar ett mål, Particle Swarm Optimization behandlar lösningar som fåglar i en flock, Genetic Algorithm rekombinerar och muterar lösningar likt gener, Ant Colony Optimization följer virtuella feromonspår, och en modifierad PSO-variant arbetar för att undvika att fastna för tidigt. Varje kandidat definierar ett komplett träningsrecept för VGG 16; nätverket tränas kort, dess valideringsnoggrannhet mäts, och metaheuristiken justerar sin population för att gynna bättre recept över flera rundor.
Från inställningsrecept till finpolering av nätverket
Ramen körs i två faser. Först används den förtränade VGG 16 som en fryst funktions-extraktör medan algoritmerna söker efter starka hyperparameterset. Därefter, när det bästa setet har hittats, låses de översta lagren i VGG 16 upp och finjusteras på cancerdata med de optimerade inställningarna, vilket tillåter nätverket att anpassa sina interna filter till de specifika vävnadsmönstren. Trots att man använde mycket små sökbudgetar — bara fem agenter och tre iterationer — och måttliga antal tränings-epoker, gav denna tvåfasstrategi dramatiska förbättringar. På lymfomdatasetet nådde exempelvis en grundläggande VGG 16 utan optimering cirka 83 procent noggrannhet, medan optimerade modeller klättrade upp i höga nittiofemprocentnivåer. Liknande hopp sågs för livmoderhalscancer, där fininställda system överträffade 99 procent noggrannhet även med bara fem tränings-epoker.
Vilken strategi fungerade bäst och varför det spelar roll
Över båda cancerformerna och i upprepade körningar utmärkte sig Whale Optimization Algorithm. När den kombinerades med den förtränade VGG 16 uppnådde den perfekta poäng på testseten för noggrannhet, precision, recall och specificitet, och den konvergerade pålitligt inom bara några steg. Andra algoritmer, såsom Ant Colony Optimization och Particle Swarm Optimization, visade sin styrka särskilt när finjustering av de djupa lagren möjliggjordes, och närmade sig eller översteg också 99 procent noggrannhet. Statistiska tester bekräftade att förbättringarna från val-baserad tuning över de andra metoderna inte berodde på slumpen. Medan sådana nästan perfekta resultat fortfarande måste kontrolleras på bredare och mer varierade data, visar studien att väl valda sökstrategier kan frigöra betydligt mer prestanda ur befintliga nätverk än vad standardinställningar tillåter.
Vad detta betyder för framtidens cancervård
För icke-specialister är huvudpoängen att studien erbjuder ett smartare sätt att justera ett befintligt djupinlärningssystem så att det kan skilja flera, liknande cancerformer med mycket hög tillförlitlighet, med begränsade träningsdata och rimliga beräkningsresurser. I stället för att ersätta läkare kan sådana system fungera som konsekventa assistenter, flagga misstänkta preparat och hjälpa till att minska missade eller felaktiga diagnoser. Författarna noterar att större och mer mångfaldiga datamängder, lättare nätverksdesigner och verktyg som förklarar vad modellen ser kommer att behövas innan införande i kliniker. Ändå antyder detta arbete att låta virtuella valar, vargar och svärmar finjustera våra cancerupptäckande nätverk kan göra automatiserad diagnostik skarpare, snabbare och mer pålitlig.
Citering: Abdelhay, E.H., Elgamily, K.M. & Badr, W.O.EF. Metaheuristic optimization of deep CNNs for multi-class diagnosis of cervical cancer and lymphoma. Sci Rep 16, 15110 (2026). https://doi.org/10.1038/s41598-026-51619-3
Nyckelord: avbildning av livmoderhalscancer, klassificering av lymfom, djupinlärningsdiagnostik, hyperparameteroptimering, metaheuristiska algoritmer