Clear Sky Science · pt
Otimização metaheurística de CNNs profundas para diagnóstico multiclasse de câncer cervical e linfoma
Ferramentas mais inteligentes para detectar o câncer precocemente
Para muitas pessoas, o diagnóstico de câncer ainda aparece tarde demais, quando o tratamento é mais difícil e as chances de sobrevivência diminuem. Médicos já utilizam microscópios e computadores para inspecionar amostras de tecido, mas ensinar máquinas a distinguir cânceres de aparência similar é surpreendentemente difícil. Este estudo explora como tornar a inteligência artificial muito mais confiável na detecção de duas doenças graves, câncer cervical e linfoma, permitindo que estratégias de busca inspiradas na natureza ajustem automaticamente uma poderosa rede de análise de imagens.
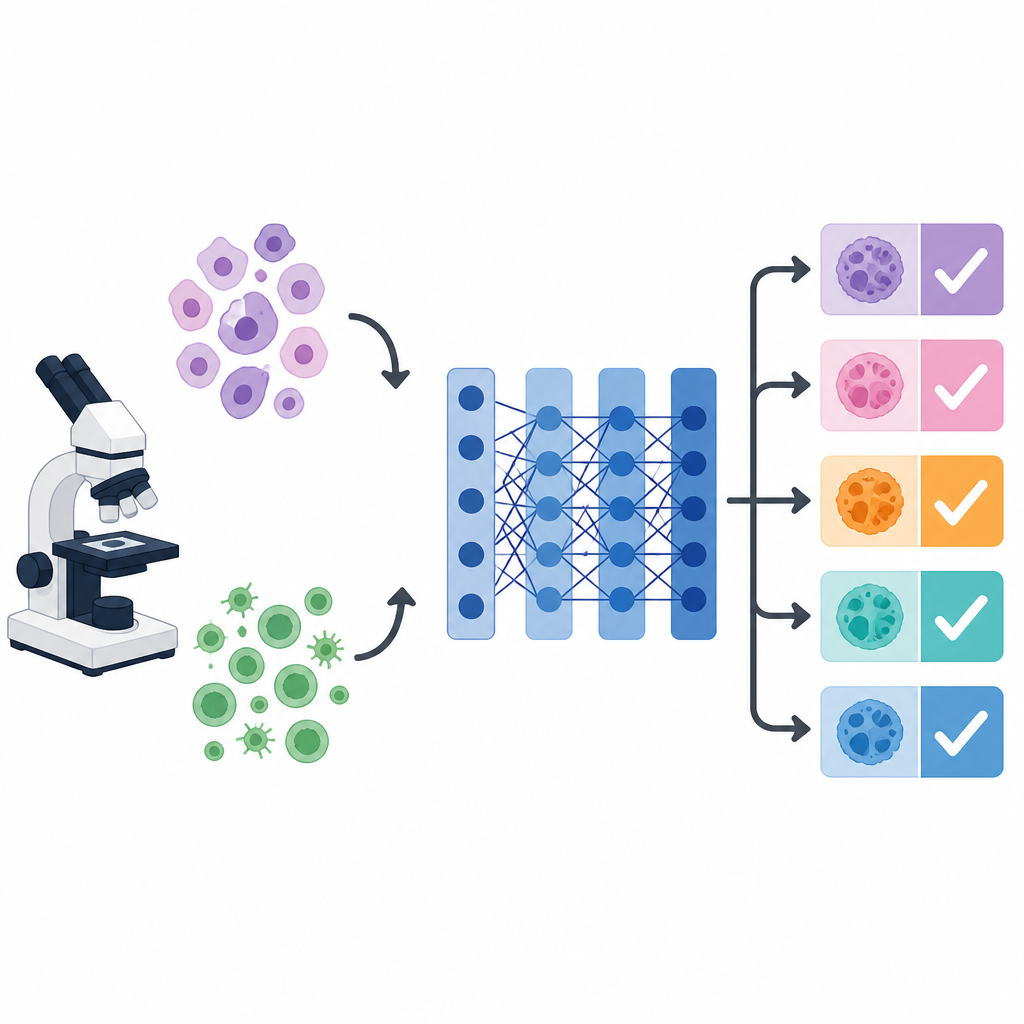
Por que imagens de câncer confundem os computadores
Ao microscópio, células de diferentes cânceres podem se assemelhar, enquanto células do mesmo câncer podem variar amplamente em forma, cor e textura. Essa bagunça visual dificulta diagnósticos consistentes tanto para humanos quanto para máquinas. Sistemas de aprendizado profundo, especialmente uma rede de imagens popular chamada VGG-16, podem aprender padrões visuais úteis. Contudo, seu desempenho depende fortemente de muitos parâmetros ocultos, como taxa de aprendizado, tamanho do lote e o grau de regularização do modelo. Esses parâmetros, chamados hiperparâmetros, geralmente são escolhidos manualmente ou mantidos em valores padrão, o que pode limitar a acurácia, especialmente quando o objetivo é distinguir múltiplos tipos de câncer ao mesmo tempo.
Aproveitando força de grandes bases sem precisá-las
Conjuntos de imagens médicas costumam ser pequenos, porque amostras rotuladas de alta qualidade são difíceis e caras de obter. Para contornar isso, os pesquisadores usam transferência de aprendizado. Eles partem de uma rede VGG-16 treinada em uma enorme coleção de imagens gerais e reaproveitam suas camadas iniciais como extrator de características para imagens de células. Em seguida, acrescentam camadas personalizadas adaptadas à nova tarefa. A equipe trabalha com duas coleções públicas: um conjunto de câncer cervical com cinco categorias celulares e um conjunto de linfoma com três subtipos. Cada conjunto original tinha menos de mil imagens, então os autores os ampliaram por meio de aumento de dados cuidadoso, como pequenas rotações, deslocamentos, zooms, alterações de brilho e espelhamentos, para criar dezenas de milhares de exemplos de treinamento variados.
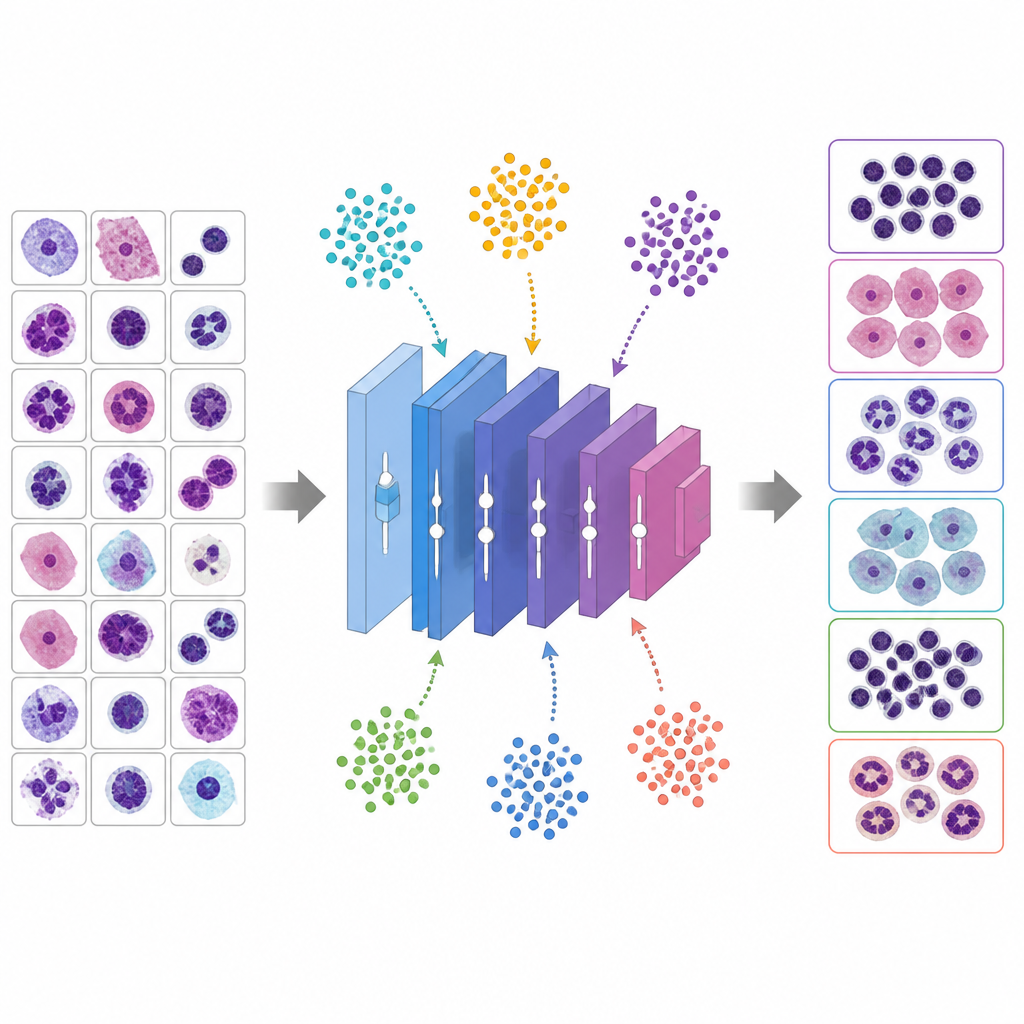
Deixando animais virtuais ajustar os botões
Em vez de adivinhar bons hiperparâmetros, o estudo usa seis algoritmos metaheurísticos inspirados no comportamento animal e na evolução para buscar as melhores configurações. Nesses métodos, cada solução candidata é como uma criatura explorando uma paisagem de possibilidades. O Whale Optimization Algorithm imita como jubartes espiralam ao redor da presa, o Grey Wolf Optimizer modela lobos cercando e rastreando um alvo, o Particle Swarm Optimization trata as soluções como pássaros em um bando, o Genetic Algorithm recombina e muta soluções como genes, o Ant Colony Optimization segue trilhas de feromônio virtuais, e uma variante modificada do PSO trabalha para evitar ficar presa cedo demais. Cada candidato define uma receita completa de treinamento para o VGG-16; a rede é treinada brevemente, sua acurácia de validação é medida, e a metaheurística ajusta sua população para favorecer melhores receitas ao longo de várias rodadas.
Das receitas de ajuste ao polimento fino da rede
O framework roda em duas fases. Primeiro, o VGG-16 pré-treinado é usado como um extrator de características congelado enquanto os algoritmos buscam conjuntos fortes de hiperparâmetros. Segundo, uma vez encontrado o melhor conjunto, as camadas superiores do VGG-16 são descongeladas e afinadas nos dados de câncer usando essas configurações otimizadas, permitindo que a rede adapte seus filtros internos aos padrões específicos do tecido. Apesar de usar orçamentos de busca muito pequenos — apenas cinco agentes e três iterações — e números modestos de épocas de treinamento, essa estratégia dupla produziu ganhos impressionantes. No conjunto de linfoma, por exemplo, um VGG-16 padrão sem otimização alcançou cerca de 83% de acurácia, enquanto modelos otimizados subiram para a casa dos noventa e poucos por cento. Saltos semelhantes foram observados para câncer cervical, onde sistemas afinados ultrapassaram 99% de acurácia mesmo com apenas cinco épocas de treinamento.
Qual estratégia funcionou melhor e por que isso importa
Ao longo de ambos os tipos de câncer e em execuções repetidas, o Whale Optimization Algorithm se destacou. Quando combinado com o VGG-16 pré-treinado, alcançou pontuações perfeitas nos conjuntos de teste para acurácia, precisão, recall e especificidade, e convergiu de forma confiável em apenas alguns passos. Outros algoritmos, como Ant Colony Optimization e Particle Swarm Optimization, mostraram sua força especialmente depois que o ajuste fino das camadas profundas foi habilitado, também se aproximando ou ultrapassando 99% de acurácia. Testes estatísticos confirmaram que os ganhos do ajuste baseado em whale sobre os outros métodos não foram fruto do acaso. Embora resultados quase perfeitos devam ainda ser verificados em dados mais amplos e diversos, o estudo demonstra que estratégias de busca cuidadosamente escolhidas podem desbloquear muito mais desempenho de redes existentes do que os valores padrão permitem.
O que isso significa para o futuro do cuidado com o câncer
Para não especialistas, a principal conclusão é que o estudo oferece uma maneira mais inteligente de ajustar um sistema de aprendizado profundo existente para que ele consiga separar múltiplos cânceres de aparência similar com alta confiabilidade, usando dados de treinamento limitados e recursos computacionais razoáveis. Em vez de substituir médicos, tais sistemas podem servir como assistentes consistentes, sinalizando lâminas suspeitas e ajudando a reduzir diagnósticos perdidos ou equivocados. Os autores observam que conjuntos de dados maiores e mais diversos, projetos de redes mais leves e ferramentas que expliquem o que o modelo enxerga serão necessários antes do uso em clínicas. Ainda assim, este trabalho sugere que deixar baleias, lobos e enxames virtuais ajustarem nossas redes de detecção de câncer pode tornar o diagnóstico automatizado mais preciso, rápido e confiável.
Citação: Abdelhay, E.H., Elgamily, K.M. & Badr, W.O.EF. Metaheuristic optimization of deep CNNs for multi-class diagnosis of cervical cancer and lymphoma. Sci Rep 16, 15110 (2026). https://doi.org/10.1038/s41598-026-51619-3
Palavras-chave: imagens de câncer cervical, classificação de linfoma, diagnóstico por aprendizado profundo, otimização de hiperparâmetros, algoritmos metaheurísticos