Clear Sky Science · ru
Метаэвристическая оптимизация глубоких CNN для многоклассовой диагностики рака шейки матки и лимфомы
Более умные инструменты для раннего выявления рака
Для многих людей диагноз «рак» всё ещё устанавливают слишком поздно, когда лечение сложнее, а шансы на выживание ниже. Врачи уже используют микроскопы и компьютеры для анализа образцов тканей, но научить машины различать визуально похожие виды рака оказывается неожиданно трудно. В этом исследовании изучается, как сделать искусственный интеллект гораздо более надёжным в обнаружении двух серьёзных заболеваний — рака шейки матки и лимфомы — позволяя стратегиям поиска, вдохновлённым природой, автоматически тонко настраивать мощную сеть для анализа изображений.
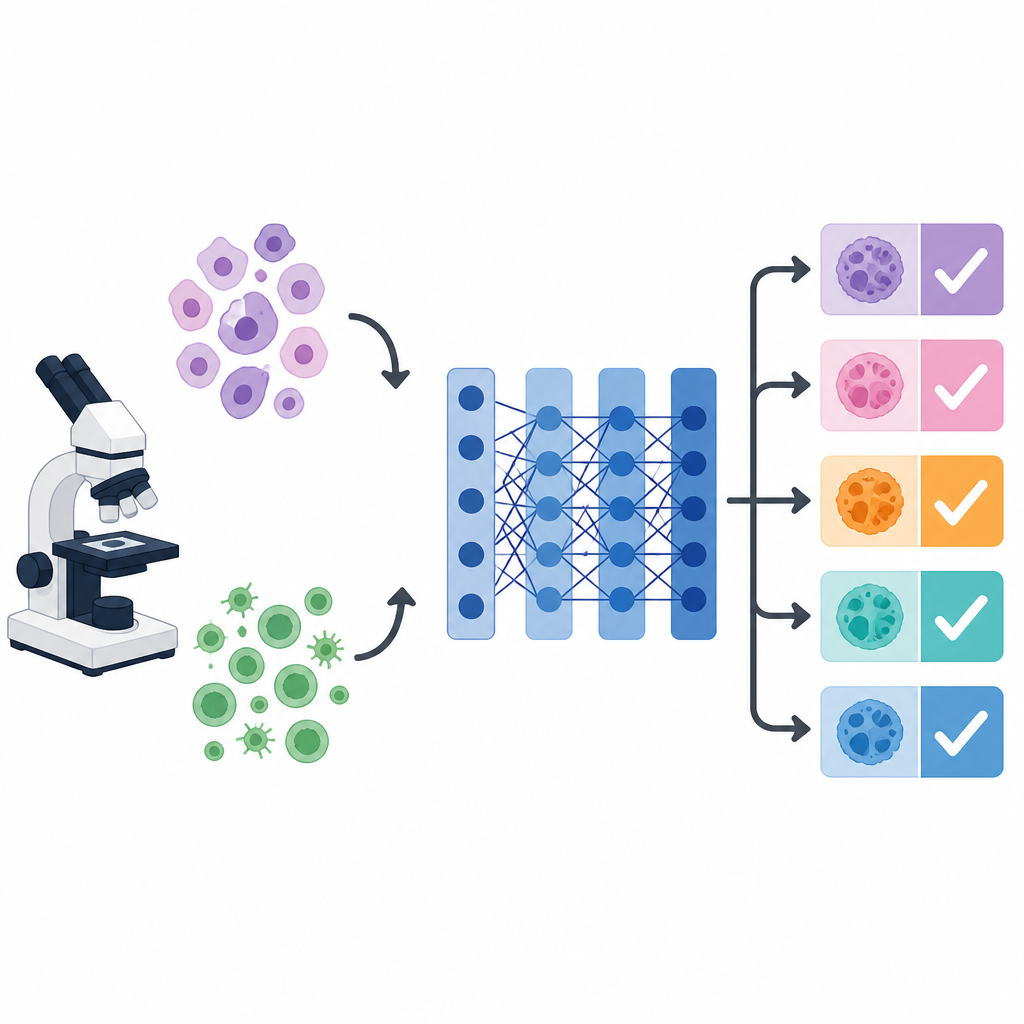
Почему изображения рака сбивают с толку компьютеры
Под микроскопом клетки разных видов рака могут имитировать друг друга, в то время как клетки одного и того же рака сильно различаются по форме, цвету и текстуре. Этот визуальный хаос затрудняет получение согласованных диагнозов как людьми, так и машинами. Системы глубокого обучения, особенно популярная сеть для изображений VGG 16, способны выучивать полезные визуальные паттерны. Однако их эффективность сильно зависит от множества скрытых настроек, таких как скорость обучения, размер батча и степень регуляризации. Эти настройки, называемые гиперпараметрами, обычно выбирают вручную или оставляют по умолчанию, что может ограничивать точность, особенно когда цель — различать несколько типов рака одновременно.
Заимствуя силу больших данных, не имея их в избытке
Медицинские наборы изображений часто малы, поскольку качественные размеченные образцы трудно и дорого собрать. Чтобы обойти это, исследователи опираются на перенос обучения. Они начинают с VGG 16, обученной на огромной коллекции общих изображений, и повторно используют её ранние слои как извлекатель признаков для изображений клеток. Затем добавляют собственные слои, адаптированные к новой задаче. Команда работает с двумя публичными коллекциями: набором по раку шейки матки с пятью категориями клеток и набором по лимфоме с тремя подтипами. В каждом исходном наборе было менее тысячи изображений, поэтому авторы расширили их с помощью аккуратного увеличения данных — небольших поворотов, сдвигов, масштабирования, изменений яркости и зеркалирования — чтобы получить десятки тысяч разнообразных обучающих примеров.
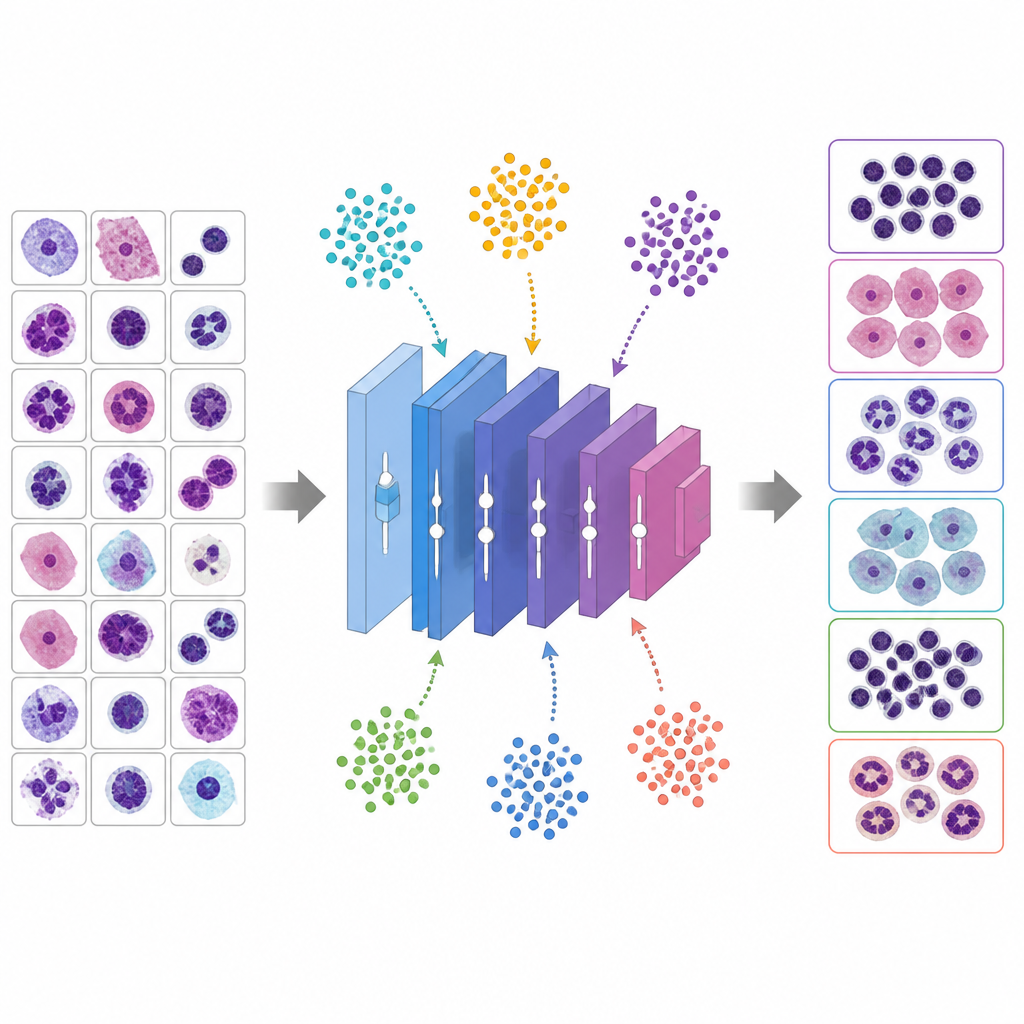
Пускаем виртуальных животных настраивать регуляторы
Вместо того чтобы угадывать хорошие гиперпараметры, в исследовании используют шесть метаэвристических алгоритмов, вдохновлённых поведением животных и эволюцией, чтобы искать лучшие настройки. В этих методах каждая кандидатная конфигурация подобна существу, исследующему ландшафт возможностей. Алгоритм оптимизации китов имитирует, как горбатые киты закручиваются вокруг добычи, Grey Wolf Optimizer моделирует волков, окружающих и отслеживающих цель, Particle Swarm Optimization рассматривает решения как птиц в стае, генетический алгоритм рекомбинирует и мутирует решения, как гены, Ant Colony Optimization следует виртуальным феромоновым тропам, а модифицированный вариант PSO старается избежать преждевременной сходимости. Каждая кандидатная точка задаёт полный рецепт обучения VGG 16; сеть обучают недолго, измеряют точность на валидации, а метаэвристика корректирует популяцию, чтобы в последующих раундах отдавать предпочтение лучшим рецептам.
От подбора рецептов к тонкой доводке сети
Фреймворк работает в два этапа. Сначала предобученная VGG 16 используется в замороженном виде как извлекатель признаков, пока алгоритмы ищут сильные наборы гиперпараметров. Затем, после нахождения лучшего набора, верхние слои VGG 16 размораживают и дообучают на данных по раку с использованием оптимизированных настроек, что позволяет сети адаптировать внутренние фильтры к специфике тканевых образцов. Несмотря на очень скромные бюджеты поиска — всего пять агентов и три итерации — и умеренное число эпох обучения, эта двухэтапная стратегия дала впечатляющие улучшения. Например, на наборе по лимфоме базовая VGG 16 без оптимизации достигала примерно 83 процентов точности, тогда как оптимизированные модели поднялись до высоких девяностых процентов. Похожие скачки наблюдались и для рака шейки матки, где настроенные системы превысили 99 процентов точности даже при всего пяти эпохах обучения.
Какая стратегия сработала лучше и почему это важно
Во всех экспериментах и повторных запусках выделился алгоритм оптимизации китов. В паре с предобученной VGG 16 он достигал идеальных показателей на тестовых наборах по точности, точности положительных срабатываний (precision), полноте (recall) и специфичности, и сходился стабильно всего за несколько шагов. Другие алгоритмы, такие как Ant Colony Optimization и Particle Swarm Optimization, показали свою силу особенно после включения дообучения глубоких слоёв, также приближаясь или превосходя 99 процентов точности. Статистические тесты подтвердили, что преимущества китовой оптимизации перед другими методами не объясняются случайностью. Хотя столь близкие к идеалу результаты нужно ещё проверять на более широких и разнообразных данных, исследование демонстрирует, что тщательно подобранные стратегии поиска могут раскрыть гораздо большую производительность существующих сетей, чем позволяют настройки по умолчанию.
Что это значит для будущей онкологической помощи
Для неспециалистов главный вывод в том, что исследование предложило более умный способ настроить существующую систему глубокого обучения, чтобы она с очень высокой надёжностью разделяла несколько визуально похожих видов рака, используя ограниченные обучающие данные и разумные вычислительные ресурсы. Такие системы не заменяют врачей, но могут служить надёжными помощниками, отмечая подозрительные слайды и помогая уменьшить количество пропущенных или ошибочных диагнозов. Авторы отмечают, что перед внедрением в клинику потребуются большие и более разнообразные наборы данных, более лёгкие архитектуры сетей и инструменты, поясняющие, что именно видит модель. Тем не менее работа показывает, что позволяя виртуальным китам, волкам и роям настраивать наши сети для обнаружения рака, можно сделать автоматизированную диагностику острее, быстрее и надёжнее.
Цитирование: Abdelhay, E.H., Elgamily, K.M. & Badr, W.O.EF. Metaheuristic optimization of deep CNNs for multi-class diagnosis of cervical cancer and lymphoma. Sci Rep 16, 15110 (2026). https://doi.org/10.1038/s41598-026-51619-3
Ключевые слова: визуализация рака шейки матки, классификация лимфомы, диагностика с помощью глубокого обучения, оптимизация гиперпараметров, метаэвристические алгоритмы