Clear Sky Science · pl
Metaheurystyczna optymalizacja głębokich CNN dla wieloklasowej diagnozy raka szyjki macicy i chłoniaka
Mądrzejsze narzędzia do wczesnego wykrywania raka
Dla wielu osób diagnoza nowotworu wciąż pojawia się zbyt późno, gdy leczenie jest trudniejsze, a szanse przeżycia maleją. Lekarze już korzystają z mikroskopów i komputerów do analizy próbek tkankowych, lecz nauczanie maszyn rozróżniania podobnie wyglądających nowotworów okazuje się zaskakująco trudne. W tym badaniu autorzy badają, jak uczynić sztuczną inteligencję znacznie bardziej niezawodną w rozpoznawaniu dwóch poważnych chorób — raka szyjki macicy i chłoniaka — pozwalając strategiom wyszukiwania inspirowanym naturą automatycznie dopracować potężną sieć do analizy obrazów.
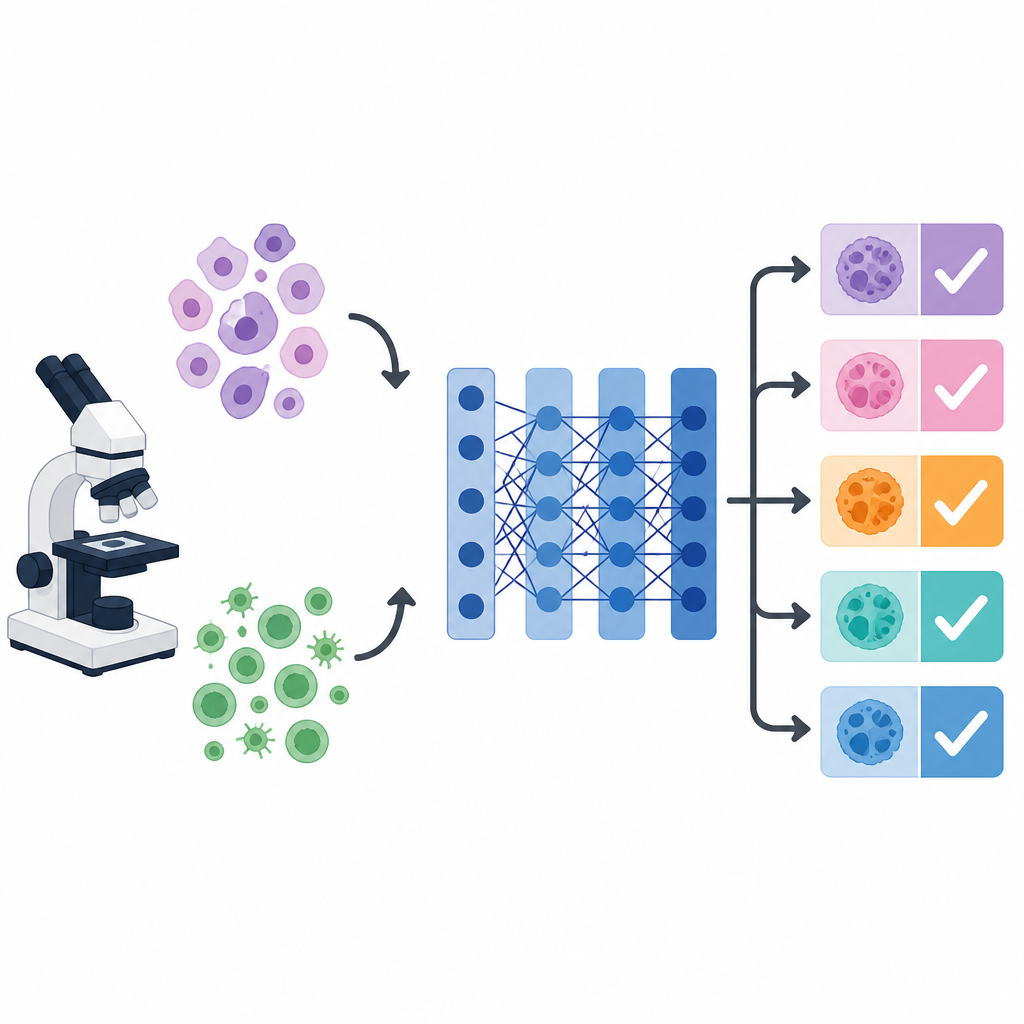
Dlaczego obrazy nowotworów wprowadzają komputery w błąd
Pod mikroskopem komórki pochodzące z różnych nowotworów mogą się wzajemnie upodabniać, podczas gdy komórki tego samego nowotworu mogą znacznie różnić się kształtem, kolorem i strukturą. Ten wizualny bałagan utrudnia zarówno ludziom, jak i maszynom dostarczanie spójnych diagnoz. Systemy głębokiego uczenia, zwłaszcza popularna sieć obrazowa VGG 16, potrafią wychwytywać użyteczne wzorce wizualne. Ich wydajność zależy jednak w dużej mierze od wielu ukrytych ustawień, takich jak szybkość uczenia, rozmiar partii czy siła regularyzacji. Te ustawienia, zwane hiperparametrami, zwykle wybiera się ręcznie lub pozostawia domyślne, co może ograniczać dokładność, szczególnie gdy celem jest jednoczesne rozróżnienie wielu typów nowotworów.
Wykorzystywanie siły dużych zbiorów danych bez konieczności ich posiadania
Zbiory medycznych obrazów często są małe, ponieważ wysokiej jakości oznakowane próbki są trudne i kosztowne w pozyskaniu. Aby to obejść, badacze stosują transfer learning. Rozpoczynają od sieci VGG 16 wytrenowanej na ogromnym ogólnym zbiorze obrazów i ponownie wykorzystują jej wczesne warstwy jako ekstraktor cech dla obrazów komórek. Następnie dodają niestandardowe warstwy dostosowane do nowego zadania. Zespół pracował na dwóch publicznych zbiorach: zestawie raka szyjki macicy z pięcioma kategoriami komórek oraz zbiorze chłoniaka z trzema podtypami. Każdy oryginalny zbiór miał poniżej tysiąca obrazów, więc autorzy powiększyli je przez staranną augmentację, taką jak niewielkie obroty, przesunięcia, skalowanie, zmiany jasności i odbicia, aby utworzyć dziesiątki tysięcy zróżnicowanych przykładów treningowych.
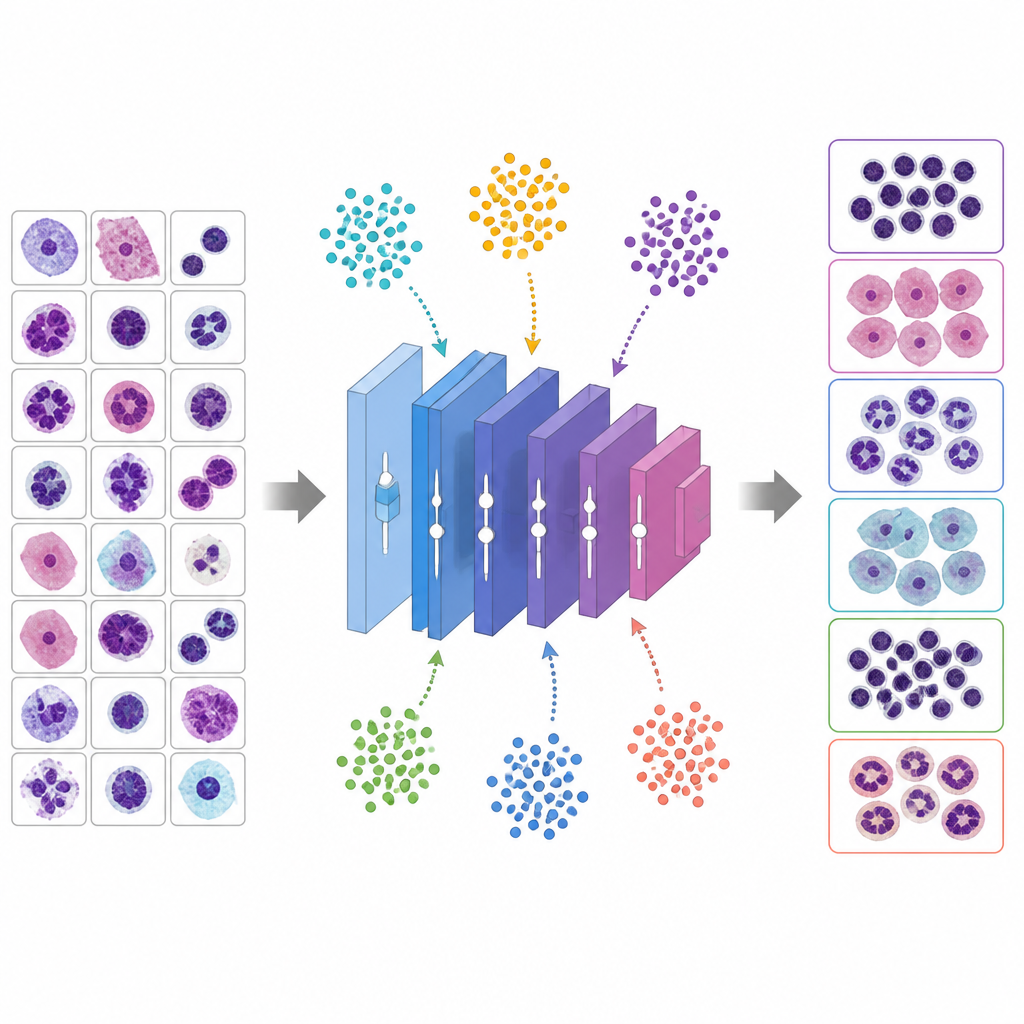
Pozwalając wirtualnym zwierzętom regulować pokrętła
Zamiast zgadywać dobre hiperparametry, badanie wykorzystuje sześć metaheurystycznych algorytmów zainspirowanych zachowaniami zwierząt i ewolucją do poszukiwania najlepszych ustawień. W tych metodach każdy kandydat rozwiązania jest jak stworzenie eksplorujące przestrzeń możliwości. Algorytm optymalizacji wielorybów (Whale Optimization Algorithm) naśladuje sposób, w jaki humbaki spiralnie obławiają zdobycz, Grey Wolf Optimizer modeluje wilki okrążające i śledzące cel, Particle Swarm Optimization traktuje rozwiązania jak ptaki w stadzie, algorytm genetyczny rekombinuje i mutuje rozwiązania jak geny, Ant Colony Optimization podąża za wirtualnymi śladami feromonowymi, a zmodyfikowana odmiana PSO stara się uniknąć przedwczesnego utknięcia. Każdy kandydat definiuje pełny przepis treningowy dla VGG 16; sieć jest trenowana krótko, mierzona jest jej dokładność na walidacji, a metaheurystyka dostosowuje populację, uprzywilejowując lepsze przepisy przez kilka rund.
Od strojenia przepisów do drobnego polerowania sieci
Ramowy schemat działa w dwóch fazach. Najpierw wstępnie wytrenowana VGG 16 jest używana jako zamrożony ekstraktor cech, podczas gdy algorytmy poszukują silnych zestawów hiperparametrów. Po drugie, gdy najlepszy zestaw zostanie znaleziony, najwyższe warstwy VGG 16 zostają odmrożone i dopracowane na danych nowotworowych z użyciem tych zoptymalizowanych ustawień, co pozwala sieci dopasować wewnętrzne filtry do specyficznych wzorców tkankowych. Pomimo bardzo małego budżetu poszukiwań — zaledwie pięciu agentów i trzech iteracji — oraz umiarkowanej liczby epok treningowych, ta dwuetapowa strategia przyniosła uderzające korzyści. Na zbiorze chłoniaka, na przykład, bazowa VGG 16 bez optymalizacji osiągała około 83 procent trafności, podczas gdy zoptymalizowane modele wspięły się do wysokich dziewięćdziesiątek. Podobne skoki zaobserwowano dla raka szyjki macicy, gdzie dostrojone systemy przekroczyły 99 procent dokładności nawet przy zaledwie pięciu epokach treningu.
Która strategia sprawdziła się najlepiej i dlaczego to ważne
We wszystkich analizowanych typach nowotworów i przy powtarzanych uruchomieniach wyróżniał się algorytm optymalizacji wielorybów. W połączeniu z wstępnie wytrenowaną VGG 16 osiągał on perfekcyjne wyniki na zestawach testowych pod względem dokładności, precyzji, czułości i specyficzności, i zbiegał się niezawodnie w zaledwie kilku krokach. Inne algorytmy, takie jak Ant Colony Optimization czy Particle Swarm Optimization, wykazywały swoją siłę zwłaszcza po włączeniu finetuningu głębokich warstw, także zbliżając się do lub przekraczając 99 procent dokładności. Testy statystyczne potwierdziły, że zyski wynikające z strojenia opartego na algorytmie wielorybów w porównaniu z innymi metodami nie były dziełem przypadku. Chociaż tak bliskie perfekcji wyniki należy jeszcze zweryfikować na szerszych, bardziej zróżnicowanych danych, badanie pokazuje, że starannie dobrane strategie poszukiwania potrafią wydobyć znacznie więcej z istniejących sieci niż pozwalają na to ustawienia domyślne.
Co to oznacza dla przyszłej opieki onkologicznej
Dla osób niebędących specjalistami główny wniosek jest taki, że badanie proponuje mądrzejszy sposób dostosowania istniejącego systemu głębokiego uczenia, dzięki któremu potrafi on rozdzielać wiele, podobnie wyglądających nowotworów z bardzo wysoką niezawodnością, używając ograniczonych danych treningowych i rozsądnych zasobów obliczeniowych. Zamiast zastępować lekarzy, takie systemy mogłyby służyć jako spójni asystenci, wskazując podejrzane preparaty i pomagając zmniejszyć liczbę pominiętych lub błędnych diagnoz. Autorzy zauważają, że przed wdrożeniem w klinikach potrzebne będą większe i bardziej zróżnicowane zbiory danych, lżejsze architektury sieci oraz narzędzia wyjaśniające, co model widzi. Mimo to praca ta sugeruje, że pozwalanie wirtualnym wielorybom, wilkom i rojom dostrajać nasze sieci wykrywające raka może uczynić automatyczną diagnostykę ostrzejszą, szybszą i bardziej wiarygodną.
Cytowanie: Abdelhay, E.H., Elgamily, K.M. & Badr, W.O.EF. Metaheuristic optimization of deep CNNs for multi-class diagnosis of cervical cancer and lymphoma. Sci Rep 16, 15110 (2026). https://doi.org/10.1038/s41598-026-51619-3
Słowa kluczowe: obrazowanie raka szyjki macicy, klasyfikacja chłoniaka, diagnoza z użyciem głębokiego uczenia, optymalizacja hiperparametrów, algorytmy metaheurystyczne