Clear Sky Science · it
Ottimizzazione metaeuristica di CNN profonde per la diagnosi multiclasse di cancro cervicale e linfoma
Strumenti più intelligenti per individuare il cancro precocemente
Per molte persone, una diagnosi di cancro arriva ancora troppo tardi, quando le cure sono più difficili e le probabilità di sopravvivenza diminuiscono. I medici già usano microscopi e computer per esaminare campioni di tessuto, ma addestrare macchine a distinguere tumori dall’aspetto simile è sorprendentemente difficile. Questo studio esplora come rendere l’intelligenza artificiale molto più affidabile nell’individuare due malattie gravi, cancro cervicale e linfoma, lasciando che strategie di ricerca ispirate alla natura ottimizzino automaticamente una potente rete di analisi delle immagini.
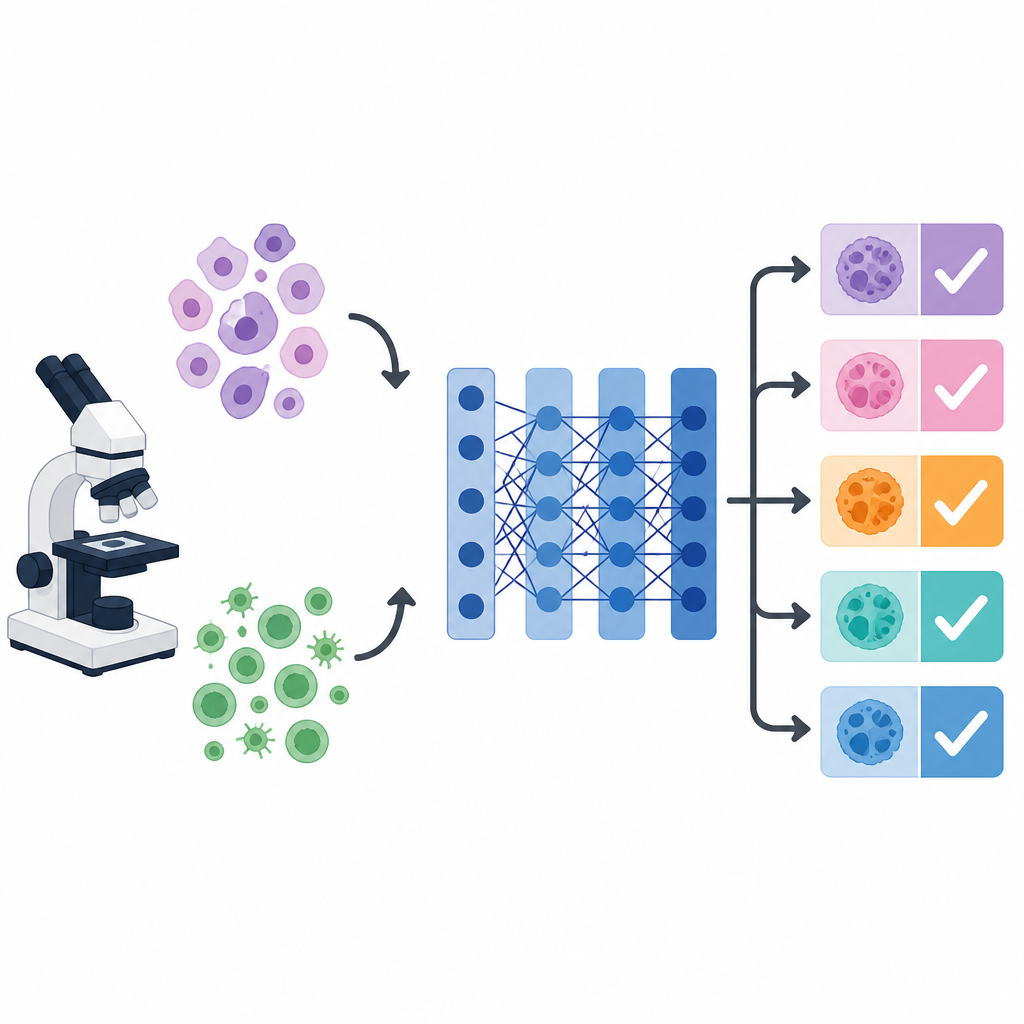
Perché le immagini tumorali confondono i computer
Al microscopio, cellule provenienti da diversi tumori possono imitarsi a vicenda, mentre cellule dello stesso tumore possono variare notevolmente in forma, colore e trama. Questo disordine visivo rende difficile per esseri umani e macchine fornire diagnosi coerenti. I sistemi di deep learning, in particolare una rete di immagini popolare chiamata VGG 16, possono apprendere pattern visivi utili. Tuttavia, le loro prestazioni dipendono fortemente da numerose impostazioni nascoste, come il tasso di apprendimento, la dimensione del batch e l’intensità della regolarizzazione. Queste impostazioni, chiamate iperparametri, sono solitamente scelte a mano o lasciate ai valori predefiniti, il che può limitare l’accuratezza, soprattutto quando l’obiettivo è distinguere più tipi di cancro contemporaneamente.
Prendere forza dai big data senza averne bisogno
I dataset di immagini mediche sono spesso piccoli, perché campioni etichettati di alta qualità sono difficili e costosi da raccogliere. Per ovviare a questo, i ricercatori si affidano al transfer learning. Partono da una rete VGG 16 addestrata su un’enorme raccolta di immagini generiche e riutilizzano i suoi strati iniziali come estrattore di caratteristiche per immagini di cellule. Poi aggiungono strati personalizzati adattati al nuovo compito. Il team lavora con due collezioni pubbliche: un set di cancro cervicale con cinque categorie cellulari e un set di linfoma con tre sottotipi. Ciascun dataset originale conteneva meno di mille immagini, quindi gli autori li hanno ampliati tramite augmentazione mirata, come piccole rotazioni, traslazioni, zoom, variazioni di luminosità e ribaltamenti, per creare decine di migliaia di esempi di addestramento variati.
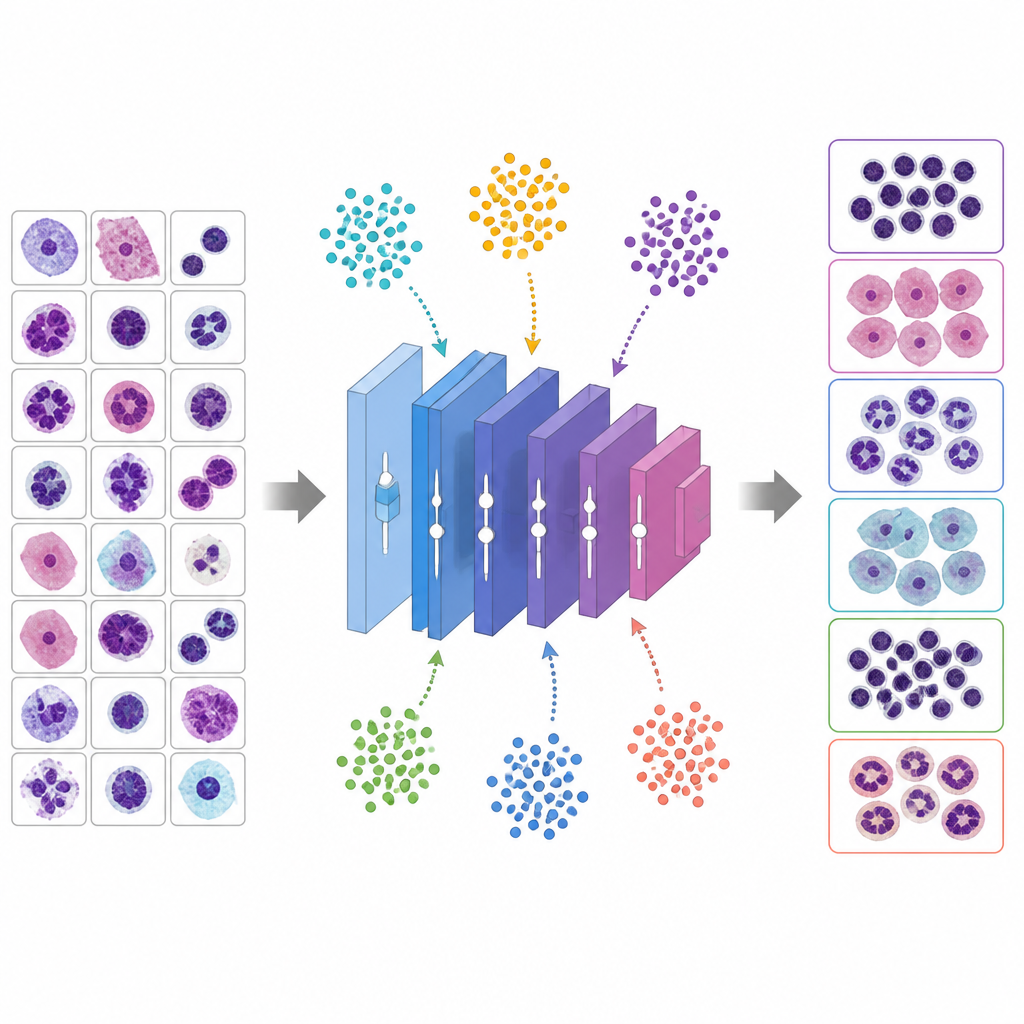
Lasciare che animali virtuali regolino le manopole
Invece di indovinare buoni iperparametri, lo studio utilizza sei algoritmi metaeuristici ispirati al comportamento animale e all’evoluzione per cercare le migliori impostazioni. In questi metodi, ogni soluzione candidata è come una creatura che esplora un paesaggio di possibilità. Il Whale Optimization Algorithm imita come le balene megattere spiraleggiano intorno alla preda, il Grey Wolf Optimizer modella i lupi che circondano e inseguono un bersaglio, il Particle Swarm Optimization tratta le soluzioni come uccelli in uno stormo, il Genetic Algorithm ricombina e muta le soluzioni come geni, l’Ant Colony Optimization segue piste di feromoni virtuali e una variante modificata del PSO lavora per evitare di restare bloccata prematuramente. Ogni candidato definisce una ricetta di addestramento completa per VGG 16; la rete viene addestrata brevemente, si misura l’accuratezza di validazione e la metaeuristica aggiusta la popolazione per favorire le ricette migliori attraverso più iterazioni.
Dalla ricerca di ricette alla rifinitura della rete
Il framework opera in due fasi. Prima, la VGG 16 preaddestrata è usata come estrattore di caratteristiche congelato mentre gli algoritmi cercano set di iperparametri efficaci. Secondo, una volta trovato il miglior set, gli strati superiori della VGG 16 vengono sbloccati e ottimizzati sul dato tumorale usando quelle impostazioni ottimizzate, permettendo alla rete di adattare i suoi filtri interni ai pattern tissutali specifici. Nonostante l’uso di budget di ricerca molto contenuti — appena cinque agenti e tre iterazioni — e di un numero modesto di epoche di addestramento, questa strategia duplice ha prodotto guadagni sorprendenti. Sul dataset di linfoma, per esempio, una VGG 16 di base senza ottimizzazione raggiungeva circa l’83% di accuratezza, mentre i modelli ottimizzati saliva fino a valori negli alti novanta. Salti simili sono stati osservati per il cancro cervicale, dove i sistemi sintonizzati hanno superato il 99% di accuratezza anche con sole cinque epoche di addestramento.
Quale strategia ha funzionato meglio e perché importa
Su entrambi i tipi di cancro e in esecuzioni ripetute, il Whale Optimization Algorithm si è distinto. Abbinato alla VGG 16 preaddestrata, ha raggiunto punteggi perfetti nei set di test per accuratezza, precisione, richiamo e specificità, convergendo in modo affidabile in appena pochi passi. Altri algoritmi, come l’Ant Colony Optimization e il Particle Swarm Optimization, hanno mostrato forza soprattutto una volta abilitata la messa a punto degli strati profondi, avvicinandosi anch’essi o superando il 99% di accuratezza. Test statistici hanno confermato che i miglioramenti dovuti alla sintonizzazione basata sulle “balene” rispetto agli altri metodi non erano dovuti al caso. Pur richiedendo ulteriori verifiche su dati più ampi e vari, lo studio dimostra che strategie di ricerca scelte con cura possono liberare molto più potenziale dalle reti esistenti rispetto ai valori predefiniti.
Cosa significa per la cura del cancro futura
Per i non specialisti, la conclusione principale è che lo studio propone un modo più intelligente di adattare un sistema di deep learning esistente affinché separi in modo molto affidabile più tipi di tumori dall’aspetto simile, usando dati di addestramento limitati e risorse di calcolo ragionevoli. Piuttosto che sostituire i medici, tali sistemi potrebbero fungere da assistenti coerenti, segnalando vetrini sospetti e aiutando a ridurre diagnosi mancate o errate. Gli autori osservano che saranno necessari dataset più grandi e diversificati, architetture di rete più leggere e strumenti che spieghino ciò che il modello vede prima di un impiego clinico. Tuttavia, questo lavoro suggerisce che lasciare che balene, lupi e sciami virtuali sintonizzino le nostre reti per individuare il cancro può rendere la diagnosi automatizzata più precisa, veloce e affidabile.
Citazione: Abdelhay, E.H., Elgamily, K.M. & Badr, W.O.EF. Metaheuristic optimization of deep CNNs for multi-class diagnosis of cervical cancer and lymphoma. Sci Rep 16, 15110 (2026). https://doi.org/10.1038/s41598-026-51619-3
Parole chiave: imaging del cancro cervicale, classificazione del linfoma, diagnosi con deep learning, ottimizzazione degli iperparametri, algoritmi metaeuristici