Clear Sky Science · de
Metaheuristische Optimierung tiefer CNNs für die Mehrklassen-Diagnose von Gebärmutterhalskrebs und Lymphom
Klügere Werkzeuge zum frühzeitigen Erkennen von Krebs
Für viele Menschen kommt eine Krebsdiagnose noch zu spät, wenn die Behandlung schwieriger ist und die Überlebenschancen sinken. Ärztinnen und Ärzte nutzen bereits Mikroskope und Computer, um Gewebeproben zu untersuchen, doch Maschinen beizubringen, sich ähnlich aussehende Krebsarten zu unterscheiden, ist überraschend schwierig. Diese Studie untersucht, wie künstliche Intelligenz deutlich zuverlässiger darin werden kann, zwei ernsthafte Erkrankungen – Gebärmutterhalskrebs und Lymphome – zu erkennen, indem naturinspirierte Suchstrategien automatisch ein leistungsfähiges Bildanalyse-Netzwerk feinabstimmen.
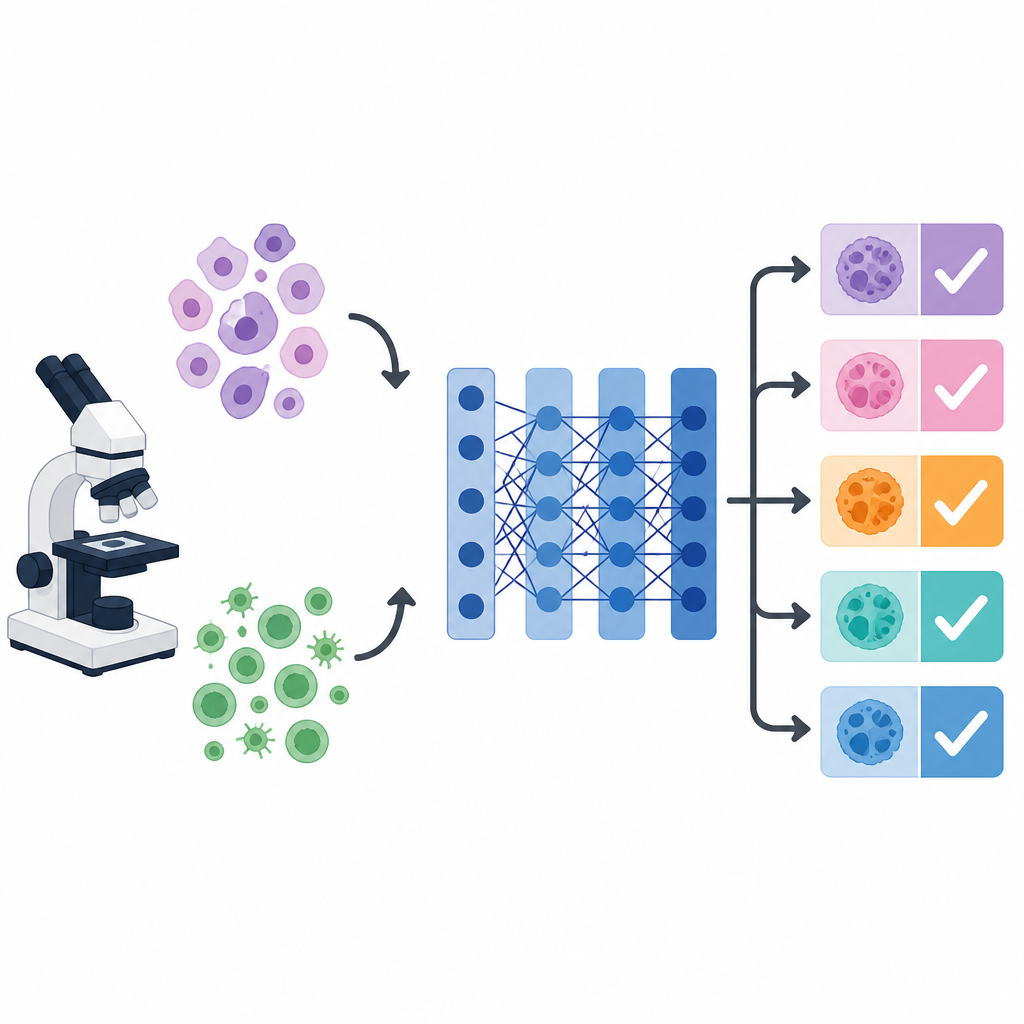
Warum Krebsbilder Computer verwirren
Unter dem Mikroskop können Zellen verschiedener Krebsarten einander ähneln, während Zellen derselben Krebsart stark in Form, Farbe und Textur variieren. Dieses visuelle Durcheinander erschwert sowohl Menschen als auch Maschinen konsistente Diagnosen. Deep-Learning-Systeme, insbesondere ein populäres Bildnetzwerk namens VGG-16, können nützliche visuelle Muster erlernen. Ihre Leistung hängt jedoch stark von zahlreichen verborgenen Einstellungen ab, wie Lernrate, Batch-Größe und Stärke der Regularisierung. Diese Einstellungen, Hyperparameter genannt, werden meist manuell gewählt oder auf Standardwerte belassen, was die Genauigkeit einschränken kann, besonders wenn mehrere Krebsarten gleichzeitig unterschieden werden sollen.
Von der Stärke großer Daten profitieren, ohne sie zu benötigen
Medizinische Bilddatensätze sind oft klein, weil hochwertige, gelabelte Proben schwer und teuer zu sammeln sind. Um dies zu umgehen, nutzen die Forschenden Transfer Learning. Sie beginnen mit einem auf einer großen allgemeinen Bildsammlung trainierten VGG-16-Netzwerk und verwenden dessen frühe Schichten wieder als Merkmalextraktor für Zellbilder. Anschließend fügen sie angepasste Schichten für die neue Aufgabe hinzu. Das Team arbeitet mit zwei öffentlichen Sammlungen: einem Gebärmutterhals-Datensatz mit fünf Zellkategorien und einem Lymphom-Datensatz mit drei Subtypen. Jeder Originaldatensatz enthielt weniger als tausend Bilder, daher vergrößerten die Autorinnen und Autoren sie durch gezielte Augmentierung wie kleine Drehungen, Verschiebungen, Zooms, Helligkeitsänderungen und Spiegelungen, um Zehntausende variierter Trainingsbeispiele zu erzeugen.
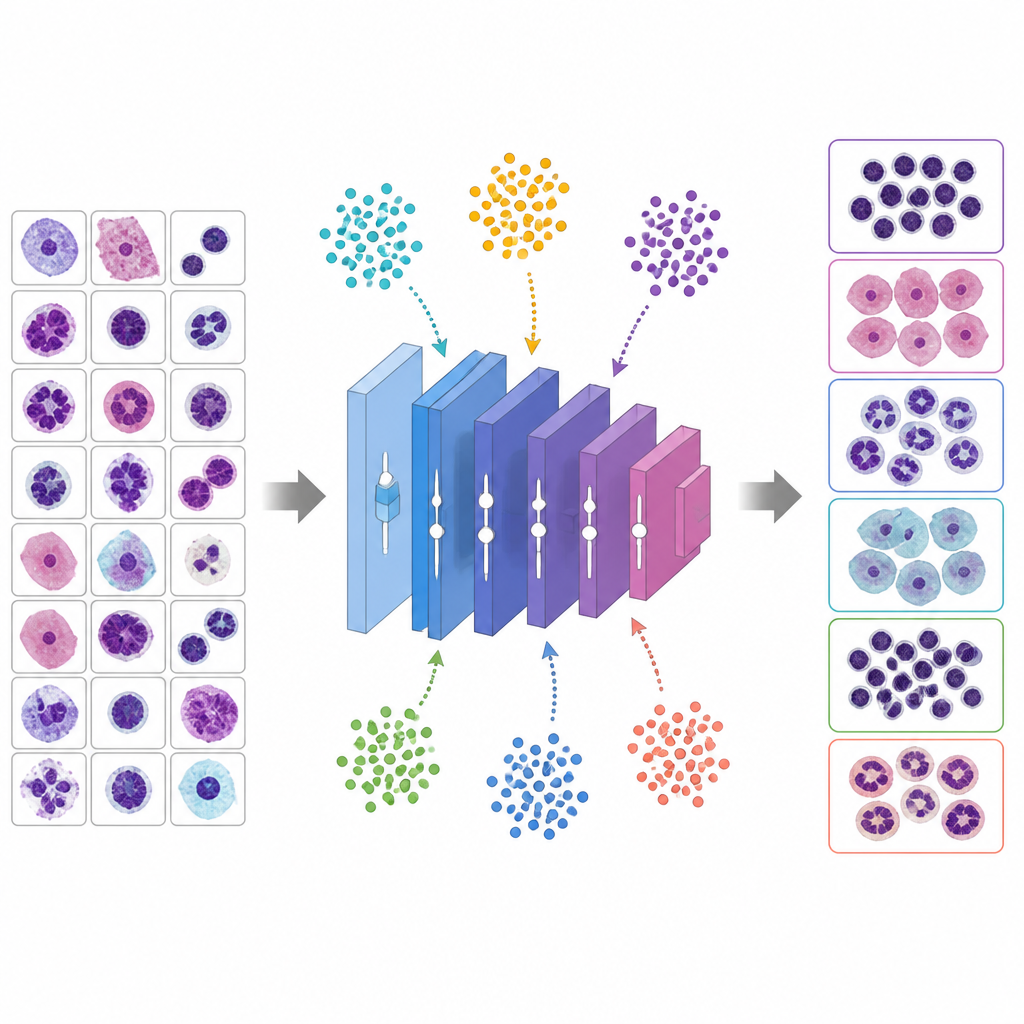
Virtuelle Tiere drehen an den Reglern
Anstatt Hyperparameter zu raten, verwendet die Studie sechs metaheuristische Algorithmen, die sich an Tierverhalten und Evolution orientieren, um die besten Einstellungen zu suchen. In diesen Methoden ist jede Kandidatenlösung wie ein Lebewesen, das eine Landschaft von Möglichkeiten erkundet. Der Whale Optimization Algorithm imitiert, wie Buckelwale in Spiralbahnen um Beute kreisen, der Grey Wolf Optimizer modelliert Wölfe beim Einkreisen und Verfolgen eines Ziels, Particle Swarm Optimization behandelt Lösungen wie Vögel in einem Schwarm, der Genetic Algorithm rekombiniert und mutiert Lösungen wie Gene, Ant Colony Optimization folgt virtuellen Pheromonspuren, und eine modifizierte PSO-Variante arbeitet darauf hin, frühes Festfahren zu vermeiden. Jede Kandidatenkonfiguration definiert ein vollständiges Trainingsrezept für VGG-16; das Netzwerk wird kurz trainiert, seine Validierungsgenauigkeit gemessen, und die Metaheuristik passt ihre Population an, um bessere Rezepte über mehrere Runden zu bevorzugen.
Vom Abstimmen der Rezepte bis zum Feinschliff des Netzwerks
Das Framework läuft in zwei Phasen. Zuerst wird das vortrainierte VGG-16 als eingefrorener Merkmalextraktor verwendet, während die Algorithmen nach starken Hyperparameter-Sets suchen. Zweitens, sobald das beste Set gefunden ist, werden die oberen Schichten von VGG-16 aufgetaut und mit diesen optimierten Einstellungen an den Krebsdaten feinabgestimmt, wodurch das Netzwerk seine internen Filter an die spezifischen Gewebemuster anpassen kann. Trotz sehr kleiner Suchbudgets – nur fünf Agenten und drei Iterationen – und moderater Anzahl an Trainings-Epochen erzielte diese zweistufige Strategie beeindruckende Verbesserungen. Auf dem Lymphom-Datensatz erreichte ein unoptimiertes VGG-16 etwa 83 Prozent Genauigkeit, während optimierte Modelle in die hohen Neunziger stiegen. Ähnliche Sprünge zeigten sich beim Gebärmutterhalskrebs, wo abgestimmte Systeme über 99 Prozent Genauigkeit erreichten, selbst bei nur fünf Trainings-Epochen.
Welche Strategie am besten funktionierte und warum das wichtig ist
Über beide Krebsarten und in wiederholten Läufen stach der Whale Optimization Algorithm hervor. In Kombination mit dem vortrainierten VGG-16 erzielte er perfekte Werte in den Testsets für Genauigkeit, Präzision, Recall und Spezifität und konvergierte zuverlässig innerhalb weniger Schritte. Andere Algorithmen wie Ant Colony Optimization und Particle Swarm Optimization zeigten ihre Stärke insbesondere, nachdem das Fine-Tuning der tiefen Schichten aktiviert war, und näherten sich ebenfalls oder übertrafen 99 Prozent Genauigkeit. Statistische Tests bestätigten, dass die Verbesserungen durch die walbasierte Abstimmung gegenüber den anderen Methoden nicht zufällig waren. Obwohl solche nahezu perfekten Ergebnisse noch an größeren, vielfältigeren Daten geprüft werden müssen, zeigt die Studie, dass sorgfältig gewählte Suchstrategien deutlich mehr Leistung aus bestehenden Netzwerken herausholen können als Standardwerte.
Was das für die zukünftige Krebsversorgung bedeutet
Für Nichtfachleute lautet die Kernbotschaft: Die Studie bietet eine klügere Methode, ein vorhandenes Deep-Learning-System so anzupassen, dass es mehrere, ähnlich aussehende Krebsarten mit sehr hoher Zuverlässigkeit trennen kann, wobei begrenzte Trainingsdaten und vernünftige Rechenressourcen ausreichen. Anstatt Ärztinnen und Ärzte zu ersetzen, könnten solche Systeme als konsistente Assistenten dienen, verdächtige Präparate kennzeichnen und helfen, verpasste oder falsche Diagnosen zu reduzieren. Die Autorinnen und Autoren betonen, dass vor einer klinischen Anwendung größere und vielfältigere Datensätze, leichtere Netzarchitekturen und Werkzeuge nötig sind, die erklären, was das Modell erkennt. Dennoch deutet diese Arbeit darauf hin, dass virtuelle Wale, Wölfe und Schwärme, die unsere Krebsdetektionsnetzwerke abstimmen, automatisierte Diagnosen schärfer, schneller und vertrauenswürdiger machen können.
Zitation: Abdelhay, E.H., Elgamily, K.M. & Badr, W.O.EF. Metaheuristic optimization of deep CNNs for multi-class diagnosis of cervical cancer and lymphoma. Sci Rep 16, 15110 (2026). https://doi.org/10.1038/s41598-026-51619-3
Schlüsselwörter: Bildgebung Gebärmutterhalskrebs, Lymphom-Klassifikation, Deep-Learning-Diagnose, Hyperparameter-Optimierung, Metaheuristische Algorithmen