Clear Sky Science · es
Optimización metaheurística de CNN profundas para el diagnóstico multiclase de cáncer cervical y linfoma
Herramientas más inteligentes para detectar el cáncer temprano
Para muchas personas, el diagnóstico de cáncer sigue llegando demasiado tarde, cuando el tratamiento es más difícil y las probabilidades de supervivencia disminuyen. Los médicos ya usan microscopios y ordenadores para inspeccionar muestras de tejido, pero enseñar a las máquinas a distinguir cánceres de aspecto similar resulta sorprendentemente complicado. Este estudio explora cómo hacer que la inteligencia artificial sea mucho más fiable a la hora de detectar dos enfermedades graves, cáncer cervical y linfoma, permitiendo que estrategias de búsqueda inspiradas en la naturaleza ajusten automáticamente una potente red de análisis de imágenes.
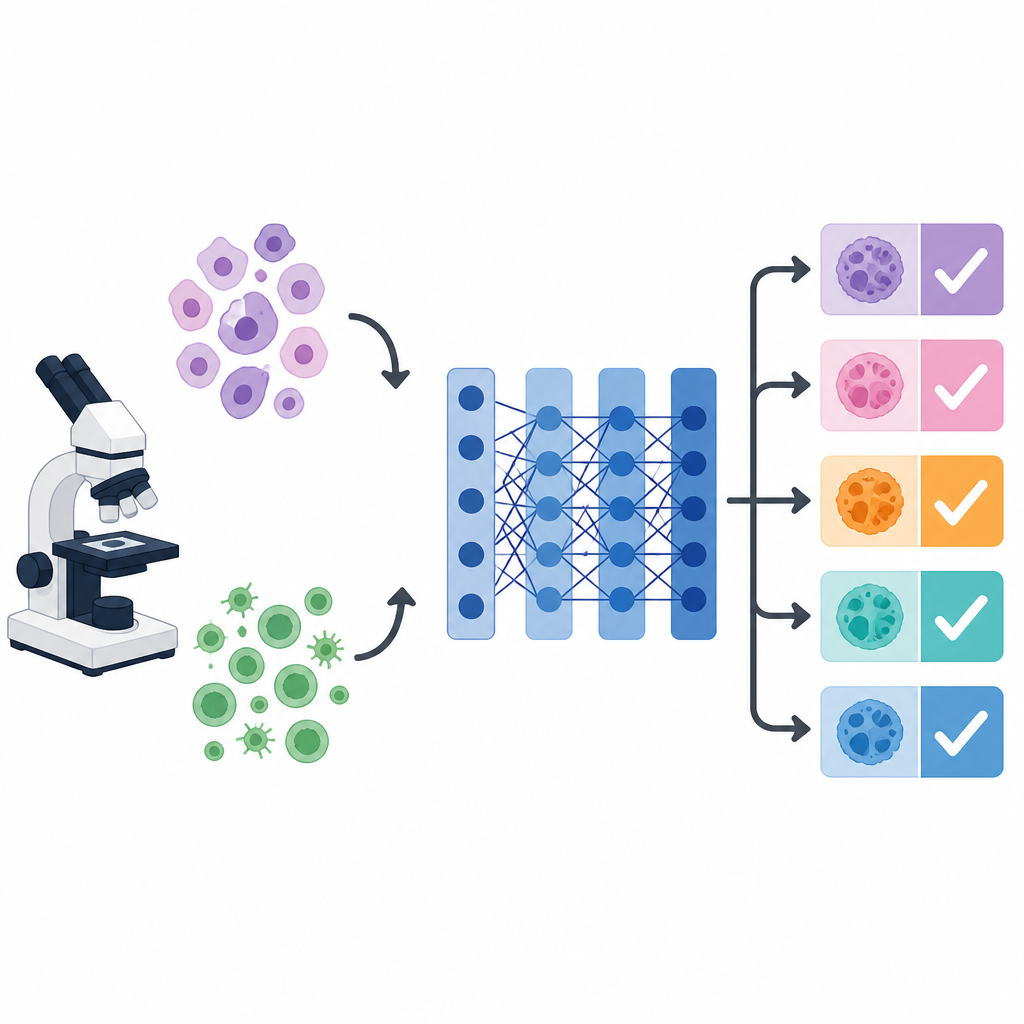
Por qué las imágenes de cáncer confunden a los ordenadores
Bajo el microscopio, las células de distintos cánceres pueden imitarse entre sí, mientras que las células del mismo cáncer pueden variar enormemente en forma, color y textura. Este desorden visual dificulta que tanto humanos como máquinas ofrezcan diagnósticos consistentes. Los sistemas de aprendizaje profundo, en especial una red de imágenes popular llamada VGG 16, pueden aprender a captar patrones visuales útiles. Sin embargo, su rendimiento depende en gran medida de muchos ajustes ocultos, como la tasa de aprendizaje, el tamaño del lote y la intensidad de la regularización. Estos ajustes, llamados hiperparámetros, suelen elegirse a mano o dejarse en valores por defecto, lo que puede limitar la precisión, especialmente cuando el objetivo es distinguir múltiples tipos de cáncer a la vez.
Tomar prestada la fuerza de los datos masivos sin necesitarlos
Los conjuntos de imágenes médicas suelen ser pequeños, porque obtener muestras etiquetadas de alta calidad es difícil y caro. Para sortear esto, los investigadores recurren al aprendizaje por transferencia. Parten de una red VGG 16 entrenada en una enorme colección de imágenes generales y reutilizan sus capas iniciales como extractor de características para las imágenes celulares. Luego añaden capas personalizadas adaptadas a la nueva tarea. El equipo trabaja con dos colecciones públicas: un conjunto de cáncer cervical con cinco categorías celulares y un conjunto de linfoma con tres subtipos. Cada conjunto original tenía menos de mil imágenes, por lo que los autores los ampliaron mediante aumentos controlados, como rotaciones pequeñas, desplazamientos, zooms, variaciones de brillo y volteos, para crear decenas de miles de ejemplos de entrenamiento variados.
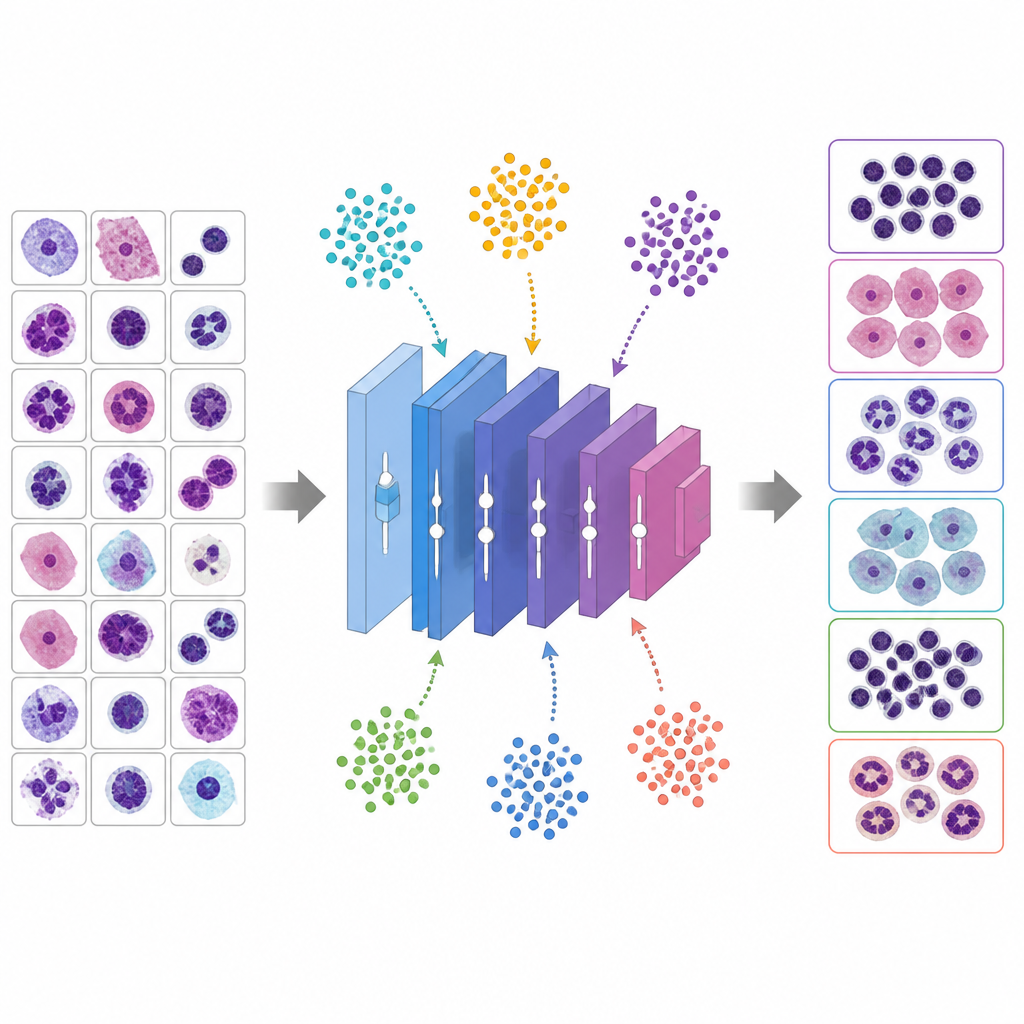
Dejar que animales virtuales ajusten los mandos
En lugar de adivinar buenos hiperparámetros, el estudio utiliza seis algoritmos metaheurísticos inspirados en el comportamiento animal y la evolución para buscar los mejores ajustes. En estos métodos, cada solución candidata es como una criatura que explora un paisaje de posibilidades. El Algoritmo de Optimización de Ballenas imita cómo las ballenas jorobadas espiralizan alrededor de sus presas, el Optimizador de Lobos Grises modela a lobos rodeando y siguiendo un objetivo, la Optimización por Enjambre de Partículas trata las soluciones como aves en una bandada, el Algoritmo Genético recombina y muta soluciones como genes, la Optimización por Colonia de Hormigas sigue rastros virtuales de feromonas, y una variante modificada de PSO trabaja para evitar quedarse atascada prematuramente. Cada candidato define una receta completa de entrenamiento para VGG 16; la red se entrena brevemente, se mide su precisión en validación y la metaheurística ajusta su población para favorecer mejores recetas a lo largo de varias rondas.
De afinar recetas a pulir la red
El marco se ejecuta en dos fases. Primero, la VGG 16 preentrenada se usa como extractor de características congelado mientras los algoritmos buscan conjuntos de hiperparámetros potentes. Segundo, una vez encontrado el mejor conjunto, se descongelan las capas superiores de VGG 16 y se realiza un afinado fino en los datos de cáncer usando esos ajustes optimizados, permitiendo que la red adapte sus filtros internos a los patrones tisulares específicos. A pesar de usar presupuestos de búsqueda muy pequeños —solo cinco agentes y tres iteraciones— y números modestos de épocas de entrenamiento, esta estrategia dual produjo ganancias notables. En el conjunto de linfoma, por ejemplo, una VGG 16 base sin optimización alcanzó alrededor del 83 por ciento de precisión, mientras que los modelos optimizados escalaron hasta niveles de los noventa altos. Se observaron saltos similares para el cáncer cervical, donde los sistemas afinados superaron el 99 por ciento de precisión incluso con solo cinco épocas de entrenamiento.
Qué estrategia funcionó mejor y por qué importa
En ambos tipos de cáncer y en ejecuciones repetidas, el Algoritmo de Optimización de Ballenas destacó. Al combinarse con la VGG 16 preentrenada, alcanzó puntuaciones perfectas en los conjuntos de prueba para precisión, precisión (precision), recall y especificidad, y convergió de forma fiable en apenas unos pasos. Otros algoritmos, como la Optimización por Colonia de Hormigas y la Optimización por Enjambre de Partículas, mostraron su fortaleza especialmente una vez que se permitió el afinado fino de las capas profundas, acercándose también o superando el 99 por ciento de precisión. Las pruebas estadísticas confirmaron que las mejoras del ajuste basado en ballenas sobre los otros métodos no se debieron al azar. Aunque resultados tan próximos a la perfección deben verificarse aún en datos más amplios y variados, el estudio demuestra que estrategias de búsqueda bien elegidas pueden desbloquear mucho más rendimiento de redes existentes que los valores por defecto permiten.
Qué significa esto para la atención oncológica futura
Para los no especialistas, la conclusión principal es que el estudio ofrece una forma más inteligente de ajustar un sistema de aprendizaje profundo existente para que pueda separar múltiples cánceres de aspecto similar con muy alta fiabilidad, usando datos de entrenamiento limitados y recursos computacionales razonables. En lugar de reemplazar a los médicos, estos sistemas podrían servir como asistentes consistentes, señalando portaobjetos sospechosos y ayudando a reducir diagnósticos perdidos o erróneos. Los autores señalan que serán necesarios conjuntos de datos más grandes y diversos, diseños de redes más ligeros y herramientas que expliquen lo que el modelo ve antes de su implantación en clínicas. Aun así, este trabajo sugiere que dejar que ballenas, lobos y enjambres virtuales ajusten nuestras redes detectoras de cáncer puede hacer que el diagnóstico automatizado sea más preciso, rápido y fiable.
Cita: Abdelhay, E.H., Elgamily, K.M. & Badr, W.O.EF. Metaheuristic optimization of deep CNNs for multi-class diagnosis of cervical cancer and lymphoma. Sci Rep 16, 15110 (2026). https://doi.org/10.1038/s41598-026-51619-3
Palabras clave: imagenología del cáncer cervical, clasificación de linfoma, diagnóstico mediante aprendizaje profundo, optimización de hiperparámetros, algoritmos metaheurísticos