Clear Sky Science · he
אופטימיזציה מטאהיוריסטית של רשתות CNN עמוקות לאבחון רב-מעמדי של סרטן צוואר רחם ולימפומה
כלים חכמים יותר לגילוי מוקדם של סרטן
עבור רבים, אבחנת סרטן עדיין מתבצעת מאוחר מדי, כשהטיפול מסובך יותר וסיכויי ההישרדות יורדים. רופאים כבר משתמשים במיקרוסקופים ומחשבים כדי לבחון דגימות רקמה, אבל ללמד מכונות להבחין בין סוגי סרטן שנראים דומים הוא משימה מפתיעה וקשה. המחקר הזה בוחן כיצד להפוך בינה מלאכותית לאמינה הרבה יותר בזיהוי שתי מחלות קשות — סרטן צוואר הרחם ולימפומה — על ידי שימוש באסטרטגיות חיפוש בהשראת הטבע כדי לכוונן באופן אוטומטי רשת חזקה לניתוח תמונות.
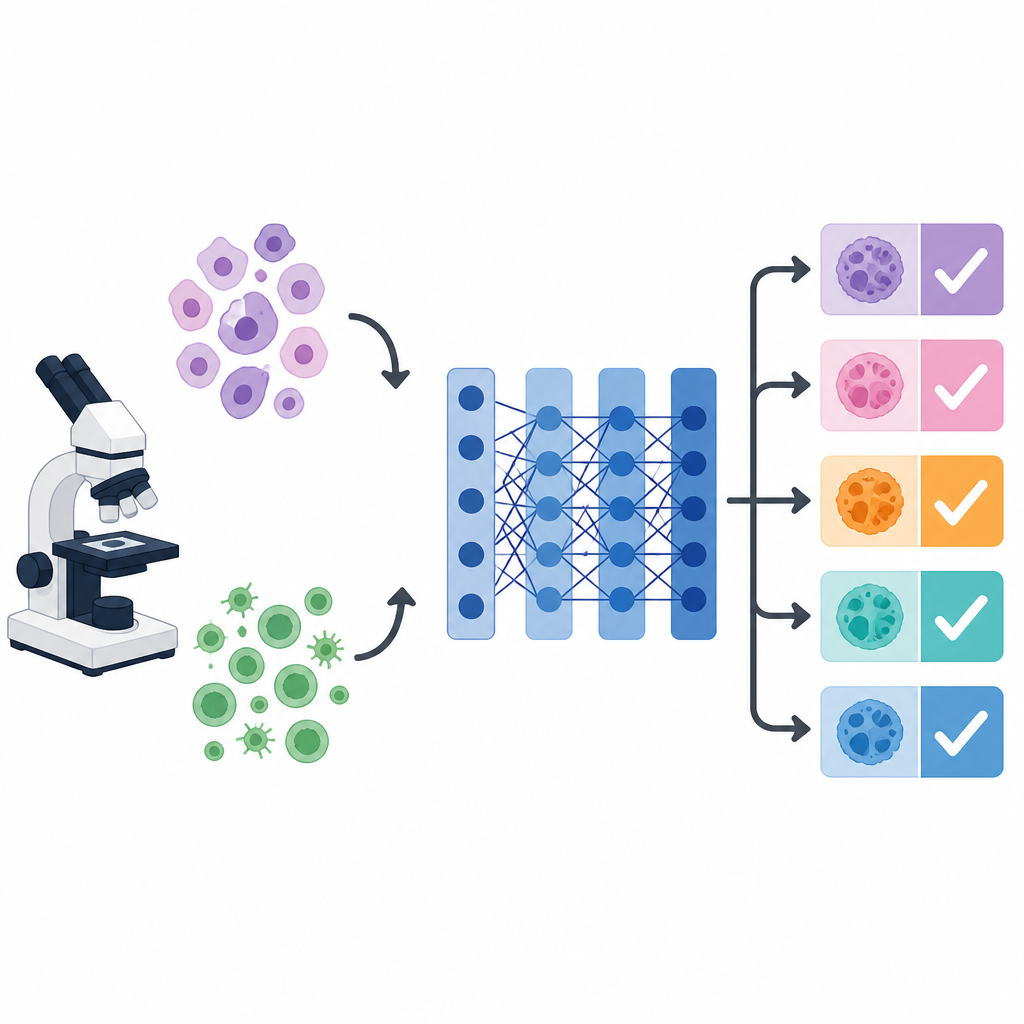
מדוע תמונות של סרטן מבלבלות מחשבים
מתחת למיקרוסקופ, תאים מסוגי סרטן שונים יכולים לחקות זה את זה, בעוד שתאים מאותו סוג סרטן עלולים להשתנות באופן קיצוני בצורה, בצבע ובמרקם. הבלאגן הוויזואלי הזה מקשה על בני אדם ומכונות לספק אבחנות עקביות. מערכות למידה עמוקה, במיוחד רשת תמונה פופולרית בשם VGG 16, יכולות ללמוד לזהות דפוסים ויזואליים שימושיים. עם זאת, ביצועיהן תלויים רבות בהגדרות נסתרות רבות, כגון שיעור הלמידה, גודל האצווה ועוצמת הרגולריזציה של המודל. הגדרות אלה, שנקראות היפרפרמטרים, נבחרות בדרך כלל ביד או נשארות בערכי ברירת מחדל, מה שעלול להגביל את הדיוק, במיוחד כאשר המטרה היא להבחין בין מספר סוגי סרטן בו־זמנית.
להשען על נתונים גדולים בלי להידרש להם
מערכי נתונים רפואיים של תמונות הם לעיתים קרובות קטנים, כי דגימות מסומנות באיכות גבוהה קשות ויקרות לאיסוף. כדי לעקוף זאת, החוקרים נשענים על למידת העברה (transfer learning). הם מתחילים מרשת VGG 16 שאומנה על אוסף גדול כללי של תמונות ומשתמשים בשכבותיה המוקדמות כמוציאת תכונות לתמונות התאים. לאחר מכן מוסיפים שכבות מותאמות למשימה החדשה. הצוות עובד עם שני אוספים ציבוריים: מערך סרטן צוואר הרחם עם חמש קטגוריות תאים ומערך לימפומה עם שלושה תת־סוגים. כל מאגר מקורי כלל פחות מאלף תמונות, לכן המחברים הרחיבו אותם באמצעות הגדלה זהירה (augmentation), כגון סיבובים קטנים, הזזות, זום, שינויים בהירות והיפוכים, כדי ליצור עשרות אלפי דוגמאות אימון מגוונות.
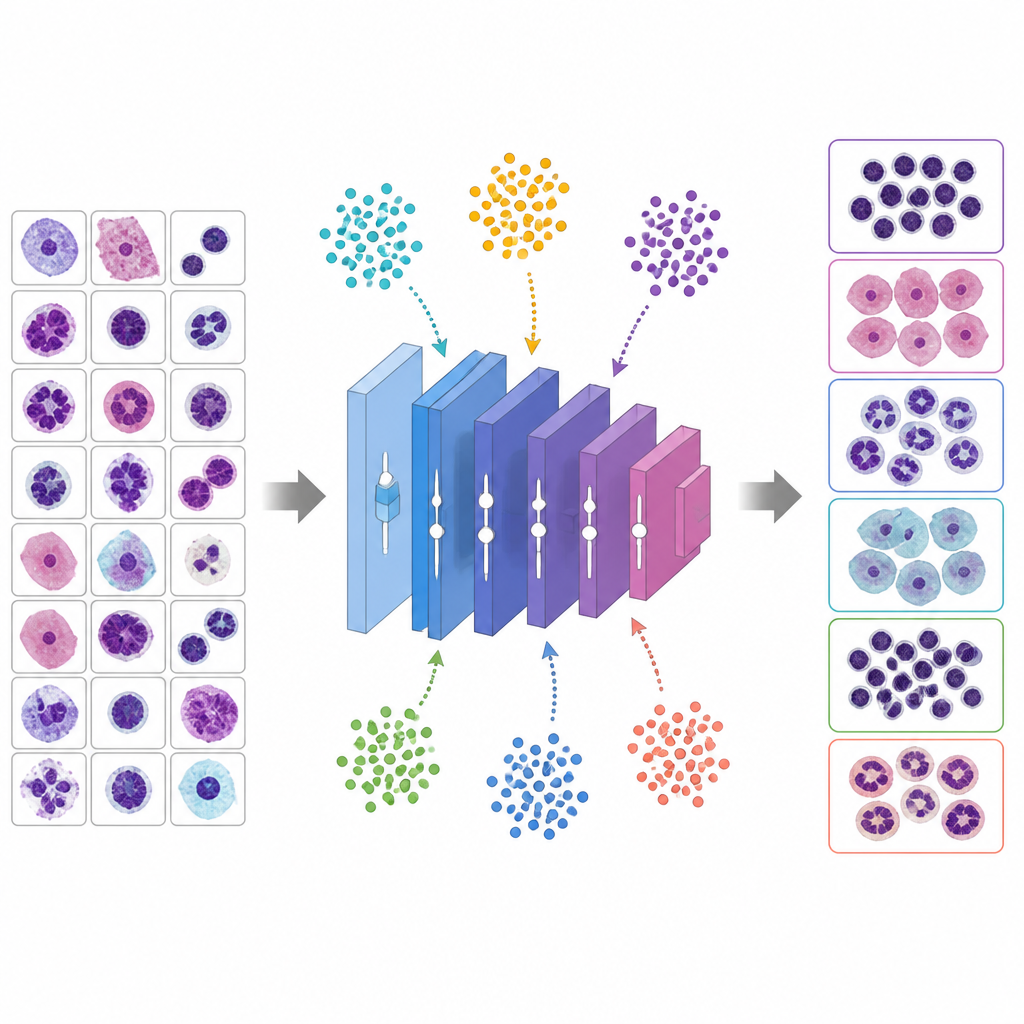
לתת לחיות וירטואליות לכוון את הכפתורים
במקום לנחש היפרפרמטרים טובים, המחקר משתמש בשש אלגוריתמים מטאהיוריסטיים בהשראת התנהגות בעלי חיים ואבולוציה כדי לחפש את ההגדרות הטובות ביותר. בשיטות אלה, כל פתרון מועמד הוא כמו יצור הסוקר נוף של אפשרויות. אלגוריתם האופטימיזציה של הלווייתן (Whale Optimization Algorithm) מדמה את האופן שבו לווייתני גב־אדום סורגים סביב הטרף, Grey Wolf Optimizer מדמה זאבים המסיטים ומתחקים אחרי מטרה, Particle Swarm Optimization רואה בפתרונות ציפורים בעדר, האלגוריתם הגנטי (Genetic Algorithm) משלב ומוטט פתרונות כמו גנים, Ant Colony Optimization עוקב אחרי שבילי פרומונים וגרסה מותאמת של PSO מנסה להימנע מהיתקעות מוקדמת. כל מועמד קובע מתכון אימון מלא ל־VGG 16; הרשת מאומנת בקצרה, נמדדת דיוק האימות שלה, והמטאהיוריסטיקה מעדכנת את האוכלוסייה כדי להעדיף מתכונים טובים יותר במספר סבבים.
ממתכונים לכוונון עדין של הרשת
המסגרת פועלת בשני שלבים. קודם כל, ה־VGG 16 המאומן מראש משמש כמוציאת תכונות קפואה בזמן שהאלגוריתמים מחפשים מערכי היפרפרמטר חזקים. שנית, לאחר שהמערך הטוב ביותר נמצא, השכבות העליונות של VGG 16 משוחררות ומכווננות בעדינות על נתוני הסרטן באמצעות ההגדרות האופטימליות שנמצאו, כך שהרשת תוכל להתאים את המסננים הפנימיים לדפוסי הרקמה הספציפיים. למרות שימוש בתקציבי חיפוש קטנים מאוד — רק חמש סוכנים ושלוש איטרציות — וכן במספר מתונים של אפוקי אימון, האסטרטגיה הכפולה הזו הניבה שיפורים מרשימים. למשל, במערך הלימפומה, VGG 16 בסיסי ללא אופטימיזציה הגיע למשך כ־83 אחוז דיוק, בעוד שמודלים אופטימיזציה טיפסו לאחוזים גבוהים מאוד. עליות דומות נצפו בסרטן צוואר הרחם, שם מערכות מכוונות עברו את 99 אחוז הדיוק אף כאשר אומנו רק חמש אפוקים.
איזו אסטרטגיה עבדה הכי טוב ולמה זה חשוב
בכלל סוגי הסרטן ובריצות חוזרות, אלגוריתם האופטימיזציה של הלווייתן בלט. כשהוא משולב עם VGG 16 המאומן מראש, הוא הגיע לתוצאות מושלמות במערכי המבחן מבחינת דיוק, דיוק חיובי סגולי (precision), אחזור (recall) וספציפיות, והתכנס מהימן תוך מספר צעדים מועט. אלגוריתמים אחרים, כגון Ant Colony Optimization ו־Particle Swarm Optimization, הראו חוזק במיוחד ברגע שאפשרו כוונון עדין של השכבות העמוקות, גם הם התקרבו או עלו על 99 אחוז דיוק. מבחנים סטטיסטיים איששו שהרווחים מכיוון כוונון מבוסס לווייתן על פני שיטות אחרות לא נבעו במקרה. אף שעל תוצאות כמעט מושלמות כאלה יש לבדוק אותן על נתונים רחבים ומגוונים יותר, המחקר מראה שאסטרטגיות חיפוש שנבחרו בקפידה יכולות לשחרר ביצועים גבוהים בהרבה מרשתות קיימות לעומת ערכי ברירת מחדל.
מה משמעות הדבר לטיפול בסרטן בעתיד
עבור ציבור לא מומחה, המסקנה העיקרית היא שהמחקר מציע דרך חכמה יותר לכוונן מערכת למידה עמוקה קיימת כך שהיא תוכל להפריד בין כמה סוגי סרטן דומים במראה באמינות גבוהה מאוד, תוך שימוש בנתוני אימון מוגבלים ומשאבי מחשוב סבירים. במקום להחליף רופאים, מערכות כאלה יכולות לשמש כעוזרות עקביות, לסמן פרוסות חשודות ולעזור להפחית אבחונים חסרים או שגויים. המחברים מדגישים שיהיו נחוצים מערכי נתונים גדולים ומגוונים יותר, ארכיטקטורות רשת קלות יותר וכלים שמסבירים מה המודל רואה לפני הפריסה בקליניקות. עם זאת, עבודה זו מרמזת שלהשאיר ללווייתנים, זאבים ועדרים וירטואליים לכוונן את הרשתות לגילוי סרטן יכול להפוך את האבחון האוטומטי לחד יותר, מהיר יותר ואמין יותר.
ציטוט: Abdelhay, E.H., Elgamily, K.M. & Badr, W.O.EF. Metaheuristic optimization of deep CNNs for multi-class diagnosis of cervical cancer and lymphoma. Sci Rep 16, 15110 (2026). https://doi.org/10.1038/s41598-026-51619-3
מילות מפתח: הדמיה של סרטן צוואר הרחם, מיון לימפומה, אבחון בלמידה עמוקה, אופטימיזציה של היפרפרמטרים, אלגוריתמים מטאהיוריסטיים