Clear Sky Science · ja
子宮頸がんとリンパ腫の多クラス診断に対する深層CNNのメタヒューリスティック最適化
早期発見のための賢いツール
多くの人にとって、がんの診断は依然として手遅れに近い段階で下されることがあり、そのときには治療が難しく生存率が下がります。医師は既に顕微鏡とコンピュータを使って組織標本を調べていますが、見た目が似ているがんを機械に識別させるのは意外に難しい。本研究は、自然に着想を得た探索戦略を用いて強力な画像解析ネットワークを自動で微調整することで、子宮頸がんとリンパ腫という二つの深刻な疾患をAIがより信頼できる形で検出できるようにする方法を探るものです。
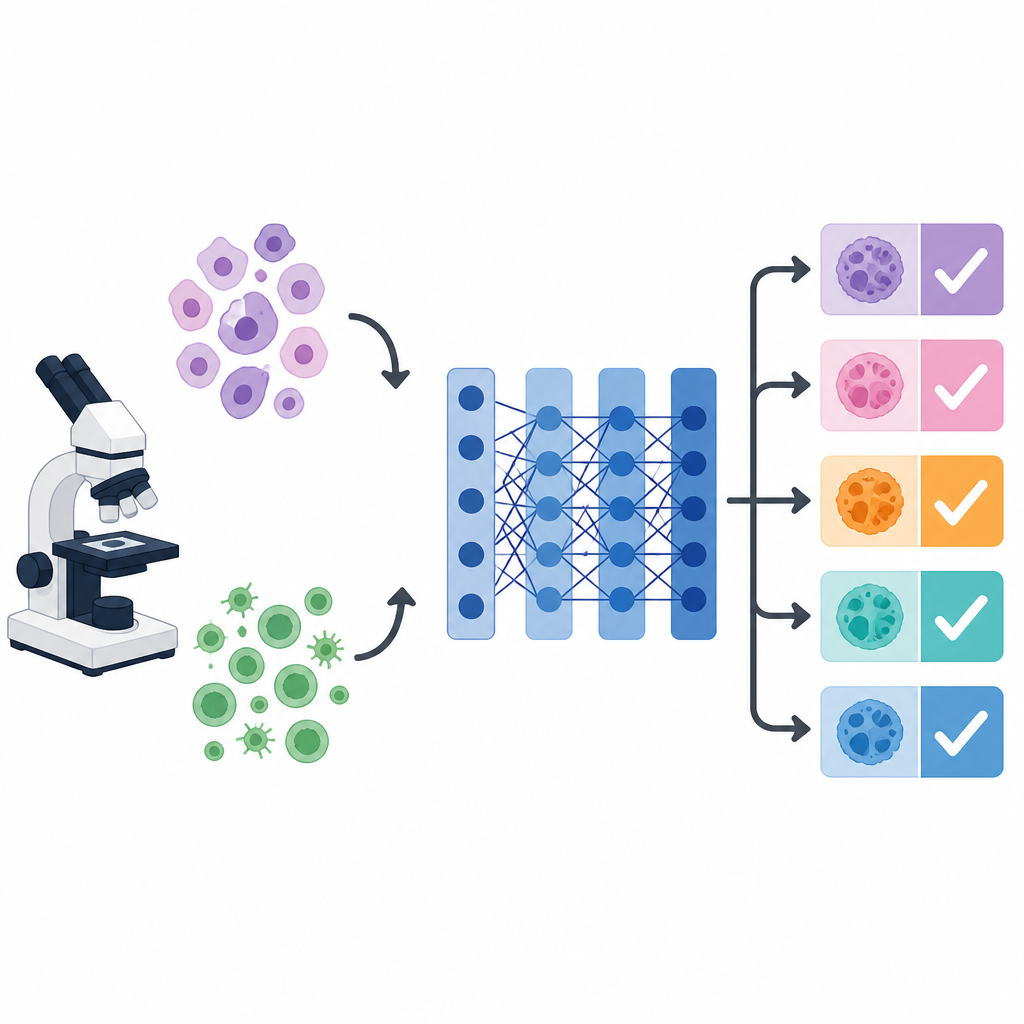
なぜがん画像はコンピュータを混乱させるのか
顕微鏡下では、異なるがんの細胞が互いに似通って見えることがあり、同じがんの細胞でも形状、色、質感が大きくばらつくことがあります。この視覚的な混乱が、人間にも機械にも一貫した診断を難しくします。深層学習システム、特に広く使われる画像ネットワークであるVGG-16は、有用な視覚パターンを学習できます。しかし、その性能は学習率、バッチサイズ、正則化の強さなど多数の隠れた設定に大きく依存します。これらの設定(ハイパーパラメータ)は通常手動で選ばれるかデフォルトのままにされがちで、特に複数のがん種を同時に区別することが目標の場合、精度の足かせになります。
大量データに頼らずビッグデータの利点を借りる
医療画像データセットは高品質なラベル付きサンプルの収集が困難かつ高価なため、小規模になりがちです。これを克服するために研究者らは転移学習を活用します。大規模な一般画像コレクションで学習済みのVGG-16の初期層を特徴抽出器として再利用し、細胞画像に対して有用な表現を取り出します。その上に新しいタスクに合わせたカスタム層を追加します。研究チームは二つの公開コレクションを用いました:5つの細胞カテゴリを含む子宮頸がんセットと、3つのサブタイプを含むリンパ腫セットです。各元データセットは千枚未満の画像だったため、回転や平行移動、ズーム、明るさの変更、反転などの慎重なデータ拡張を行い、何万もの多様な学習例を生成しました。
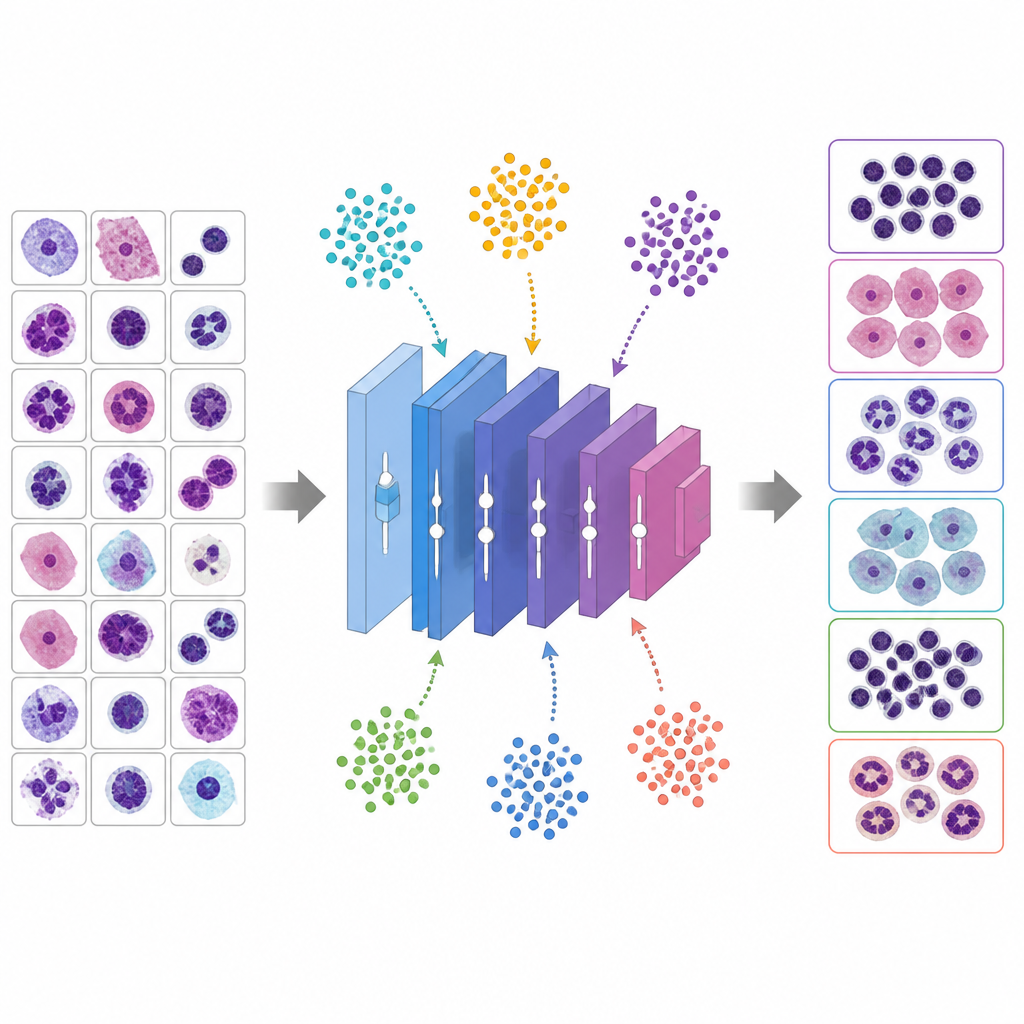
仮想の動物たちにノブを調整させる
良いハイパーパラメータを勘で決める代わりに、本研究では動物の行動や進化に着想を得た6つのメタヒューリスティックアルゴリズムを使って最適な設定を探索します。これらの手法では、各候補解が可能性の風景を探索する生き物のように振る舞います。ホエールオプティマイゼーションアルゴリズムはザトウクジラが獲物の周りでらせん運動をする様子を模し、グレイウルフオプティマイザはオオカミが標的を包囲して追跡する行動をモデル化します。パーティクルスウォーム最適化は候補解を群れをなす鳥のように扱い、遺伝的アルゴリズムは解を遺伝子のように組み替え変異させます。アントコロニー最適化は仮想フェロモントレイルを辿り、改良型PSOは早期収束を避ける工夫を加えます。各候補はVGG-16用の完全な学習レシピを定義し、ネットワークを短時間学習させ検証精度を測定、メタヒューリスティックはより良いレシピを優先するように集団を調整していきます。
レシピの調整からネットワークの微細な仕上げへ
このフレームワークは二段階で動きます。まず学習済みのVGG-16を凍結した特徴抽出器として使い、アルゴリズムが有望なハイパーパラメータ群を探索します。次に最良のセットが見つかったら、VGG-16の上位層の凍結を解除して、最適化された設定でがんデータに対して微調整(ファインチューニング)を行い、ネットワークが特定の組織パターンに内部フィルタを適応させられるようにします。非常に小さな探索予算(たとえばエージェント5体、反復3回)と控えめなエポック数しか使わなかったにもかかわらず、この二段構えの戦略は顕著な改善をもたらしました。例えばリンパ腫データセットでは、最適化なしのベースラインVGG-16が約83%の精度だったのに対し、最適化モデルは90%台後半に達しました。子宮頸がんでも同様の飛躍が見られ、調整されたシステムはわずか5エポックの学習でも99%を超える精度を記録しました。
どの戦略が最も効果的だったか、そしてそれが重要な理由
両方のがん種および繰り返し実験において、ホエールオプティマイゼーションアルゴリズムが際立ちました。学習済みVGG-16と組み合わせると、テストセットで精度、適合率、再現率、特異度のいずれも満点を達成し、わずかなステップで安定的に収束しました。アントコロニー最適化やパーティクルスウォーム最適化などの他の手法も、深層層のファインチューニングを有効にした段階で力を発揮し、99%前後の精度に到達またはそれを超えました。統計検定により、ホエールベースの調整が他の手法よりも優れていたのは偶然ではないことが確認されました。こうしたほぼ完璧な結果はより広範で多様なデータ上での検証が必要ですが、本研究は慎重に選ばれた探索戦略が既存のネットワークからデフォルト設定よりもはるかに高い性能を引き出せることを示しています。
将来のがん医療にとっての意味
非専門家にとっての主要な結論は、この研究が限られた学習データと合理的な計算資源で、既存の深層学習システムをより賢く調整して、見た目が似た複数のがんを非常に高い信頼性で区別できるようにする方法を提示しているということです。こうしたシステムは医師を置き換えるのではなく、疑わしいスライドにフラグを立て見落としや誤診を減らす一貫したアシスタントとして機能し得ます。著者らは、臨床導入の前により大きく多様なデータセット、軽量化されたネットワーク設計、モデルが何を見ているかを説明するツールが必要だと述べています。それでも、仮想のクジラやオオカミ、群れにネットワークの調整を任せることで、自動診断はより鋭く、速く、信頼できるものになる可能性があることを示しています。
引用: Abdelhay, E.H., Elgamily, K.M. & Badr, W.O.EF. Metaheuristic optimization of deep CNNs for multi-class diagnosis of cervical cancer and lymphoma. Sci Rep 16, 15110 (2026). https://doi.org/10.1038/s41598-026-51619-3
キーワード: 子宮頸がん画像, リンパ腫分類, 深層学習による診断, ハイパーパラメータ最適化, メタヒューリスティックアルゴリズム