Clear Sky Science · nl
Metaheuristische optimalisatie van diepe CNN's voor multiclass-diagnose van baarmoederhalskanker en lymfoom
Slimmere instrumenten voor vroege detectie van kanker
Voor veel mensen komt een kankerdiagnose nog steeds te laat, wanneer behandeling moeilijker is en de overlevingskansen afnemen. Artsen gebruiken al microscopen en computers om weefselmonsters te onderzoeken, maar machines leren om elkaar sterk gelijkende kankers uit elkaar te houden blijkt verrassend lastig. Deze studie onderzoekt hoe kunstmatige intelligentie veel betrouwbaarder kan worden in het herkennen van twee ernstige ziekten, baarmoederhalskanker en lymfoom, door door de natuur geïnspireerde zoekstrategieën automatisch een krachtig beeldanalysetewerk te laten fijnafstellen.
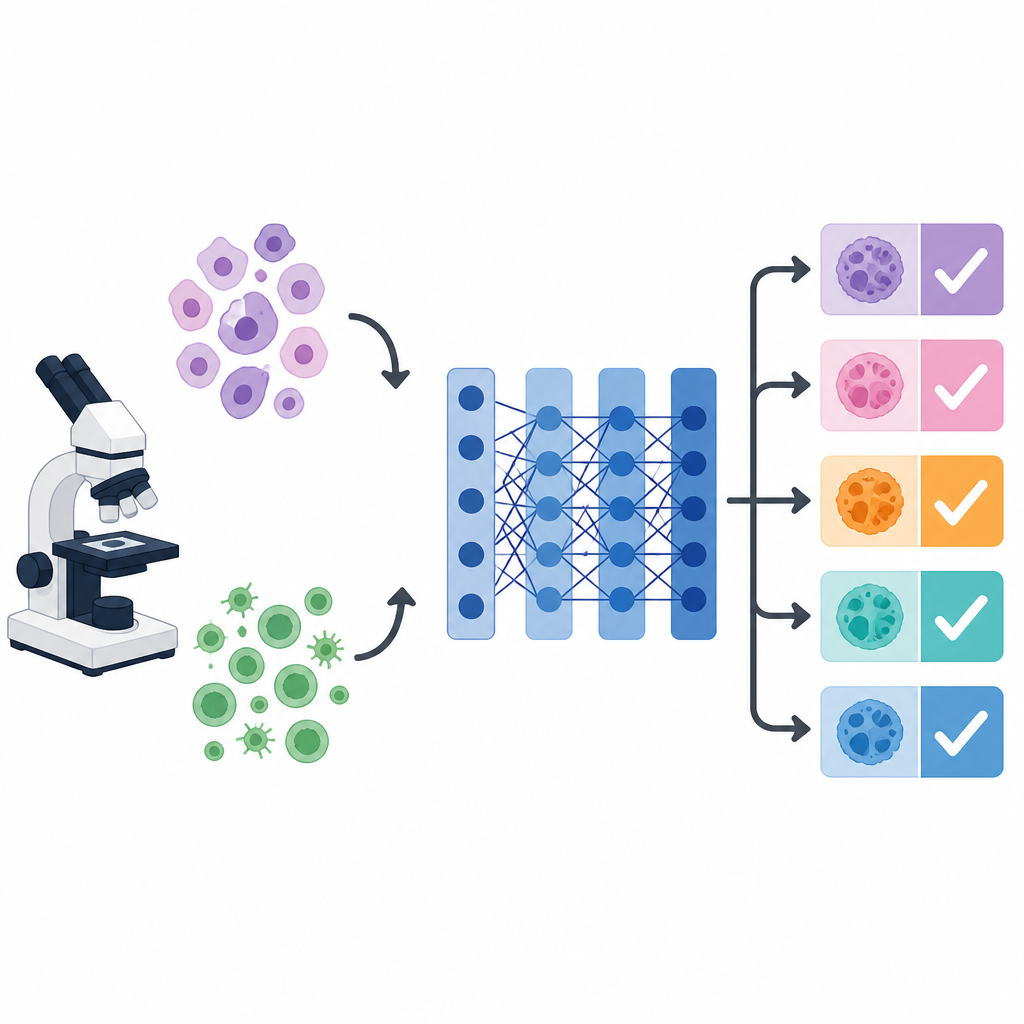
Waarom kankergezichten computers in de war brengen
Onder de microscoop kunnen cellen van verschillende kankers elkaar nabootsen, terwijl cellen van dezelfde kanker sterk kunnen variëren in vorm, kleur en textuur. Deze visuele wirwar maakt het moeilijk voor zowel mensen als machines om consistente diagnoses te geven. Deep learning-systemen, met name een populair beeldnetwerk genaamd VGG 16, kunnen nuttige visuele patronen leren herkennen. Hun prestaties hangen echter sterk af van vele verborgen instellingen, zoals leersnelheid, batchgrootte en hoe sterk het model wordt geregulariseerd. Deze instellingen, hyperparameters genoemd, worden meestal met de hand gekozen of op standaardwaarden gelaten, wat de nauwkeurigheid kan beperken, vooral wanneer het doel is meerdere kankertypen tegelijk te onderscheiden.
Kracht lenen uit grote data zonder die te hoeven hebben
Medische beelddatasets zijn vaak klein, omdat hoogwaardige gelabelde monsters moeilijk en duur zijn om te verzamelen. Om dit te omzeilen vertrouwen de onderzoekers op transfer learning. Ze starten met een VGG 16-netwerk dat is getraind op een enorme algemene beeldverzameling en hergebruiken de vroege lagen als kenmerkextractor voor celbeelden. Daarna voegen ze aangepaste lagen toe die zijn toegespitst op de nieuwe taak. Het team werkt met twee publieke verzamelingen: een dataset voor baarmoederhalskanker met vijf cellen categorieën en een lymfoomset met drie subtypes. Elke oorspronkelijke dataset bevatte minder dan duizend beelden, dus de auteurs vergrootten ze door zorgvuldige augmentatie, zoals kleine rotaties, verschuivingen, zooms, helderheidswijzigingen en spiegelen, om tienduizenden gevarieerde trainingsvoorbeelden te creëren.
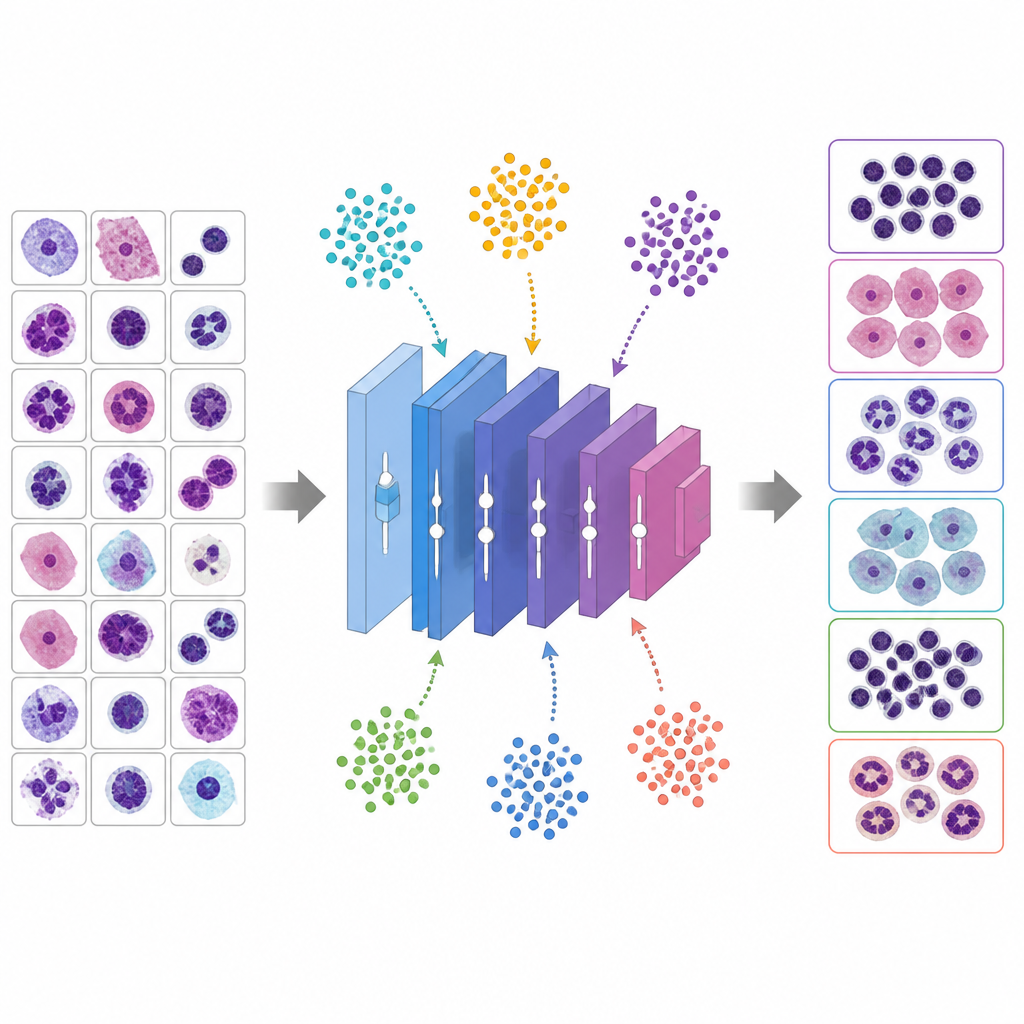
Virtuele dieren laten de knoppen afstellen
In plaats van goede hyperparameters te raden, gebruikt de studie zes metaheuristische algoritmen die zijn geïnspireerd door dierlijk gedrag en evolutie om naar de beste instellingen te zoeken. In deze methoden is elke kandidaat-oplossing als een wezen dat een landschap van mogelijkheden verkent. Het Whale Optimization Algorithm bootst na hoe bultruggen in een spiraal rond prooien bewegen, Grey Wolf Optimizer modelleert wolven die omcirkelen en een doel volgen, Particle Swarm Optimization behandelt oplossingen als vogels in een zwerm, Genetic Algorithm recombineert en muteert oplossingen als genen, Ant Colony Optimization volgt virtuele feromoonsporen, en een gemodificeerde PSO-variant werkt om voortijdig vastlopen te voorkomen. Elke kandidaat definieert een volledig trainingsrecept voor VGG 16; het netwerk wordt kort getraind, de validatienauwkeurigheid wordt gemeten en de metaheuristiek past zijn populatie aan om betere recepten over meerdere ronden te bevoordelen.
Van afstemmingsrecepten naar het verfijnen van het netwerk
Het kader werkt in twee fasen. Eerst wordt de voorgetrainde VGG 16 gebruikt als een bevroren kenmerkextractor terwijl de algoritmen zoeken naar sterke hyperparametersets. Ten tweede, zodra de beste set is gevonden, worden de bovenste lagen van VGG 16 gedemonteerd en fijn afgesteld op de kankerdata met die geoptimaliseerde instellingen, zodat het netwerk zijn interne filters kan aanpassen aan de specifieke weefselpatronen. Ondanks het gebruik van zeer kleine zoekbudgetten — slechts vijf agenten en drie iteraties — en een bescheiden aantal trainingsepochs, leverde deze dubbele strategie indrukwekkende verbeteringen op. Op de lymfoomdataset bereikte een baseline VGG 16 zonder optimalisatie bijvoorbeeld ongeveer 83 procent nauwkeurigheid, terwijl geoptimaliseerde modellen naar de hoge negentiger jaren klommen. Vergelijkbare sprongen werden gezien voor baarmoederhalskanker, waar afgestemde systemen meer dan 99 procent nauwkeurigheid behaalden, zelfs met slechts vijf trainingsepochs.
Welke strategie werkte het beste en waarom dat telt
Over beide kankertypen en in herhaalde runs viel het Whale Optimization Algorithm op. In combinatie met de voorgetrainde VGG 16 behaalde het perfecte scores op de testsets voor nauwkeurigheid, precisie, recall en specificiteit, en het convergeerde betrouwbaar binnen slechts een paar stappen. Andere algoritmen, zoals Ant Colony Optimization en Particle Swarm Optimization, toonden vooral hun kracht zodra het fijn afstellen van de diepe lagen werd ingeschakeld, en benaderden of overschreden ook 99 procent nauwkeurigheid. Statistische toetsen bevestigden dat de winst door op walvis-gebaseerde afstemming ten opzichte van de andere methoden niet op toeval berustte. Hoewel zulke bijna perfecte resultaten nog gecontroleerd moeten worden op bredere, meer gevarieerde data, toont de studie aan dat zorgvuldig gekozen zoekstrategieën veel meer prestatie uit bestaande netwerken kunnen halen dan standaardinstellingen toelaten.
Wat dit betekent voor toekomstige kankerzorg
Voor niet-specialisten is de belangrijkste conclusie dat de studie een slimmere manier biedt om een bestaand deep learning-systeem aan te passen zodat het meerdere, sterk gelijkende kankers met zeer hoge betrouwbaarheid kan onderscheiden, met beperkte trainingsdata en redelijke computerbronnen. In plaats van artsen te vervangen, zouden zulke systemen als consistente assistenten kunnen dienen, verdachte preparaten markeren en helpen gemiste of verkeerde diagnoses te verminderen. De auteurs merken op dat grotere en meer diverse datasets, lichtere netwerkontwerpen en hulpmiddelen die uitleg geven over wat het model ziet, nodig zullen zijn voordat inzet in klinieken mogelijk is. Toch suggereert dit werk dat het laten afstemmen van onze kanker-detecterende netwerken door virtuele walvissen, wolven en zwermen de automatische diagnose scherper, sneller en betrouwbaarder kan maken.
Bronvermelding: Abdelhay, E.H., Elgamily, K.M. & Badr, W.O.EF. Metaheuristic optimization of deep CNNs for multi-class diagnosis of cervical cancer and lymphoma. Sci Rep 16, 15110 (2026). https://doi.org/10.1038/s41598-026-51619-3
Trefwoorden: beeldvorming baarmoederhalskanker, classificatie van lymfoom, deep learning diagnose, hyperparameteroptimalisatie, metaheuristische algoritmen