Clear Sky Science · sv
AmvAR-effluxsystemets roll i patogenesen hos Acinetobacter baumannii
Varför denna sjukhusbakterie är viktig
Acinetobacter baumannii är en svårutrotad sjukhusbakterie som kan orsaka pneumoni, blodförgiftning samt svåra sår- och urinvägsinfektioner, särskilt hos mycket svårt sjuka patienter. Den är ökänd för att stå emot många antibiotika och till och med vissa desinfektionsmedel, vilket gör den till ett stort problem på Världshälsoorganisationens lista över kritiska hot. Denna studie ställer en central fråga: utöver att hjälpa bakterien att pumpa ut giftiga ämnen, gör ett av dess försvarssystem den också bättre på att fästa vid ytor, bilda slemmiga samhällen och orsaka sjukdom?
Ett dubbelt verktyg för överlevnad
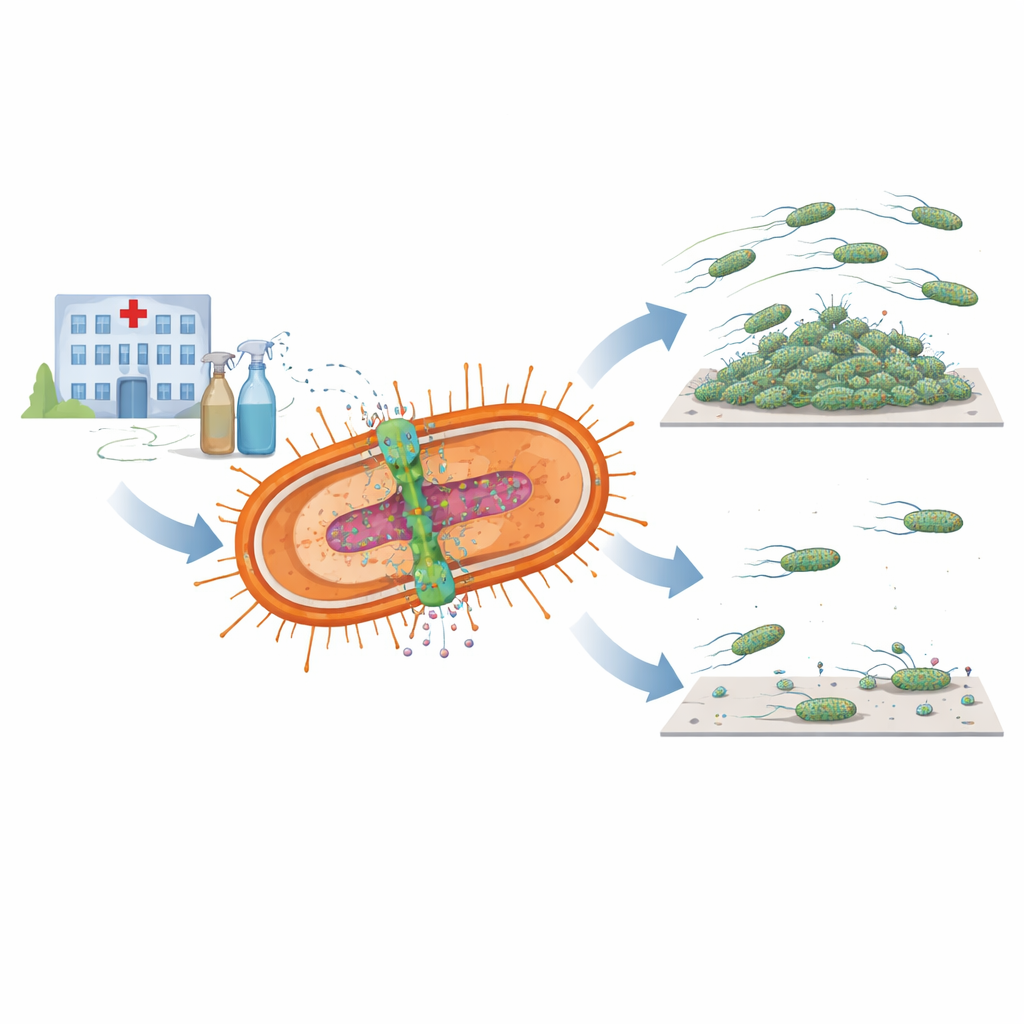
Forskarna fokuserade på ett par nära sammankopplade bakteriella komponenter som tillsammans kallas AmvAR-systemet. Den ena delen, AmvA, sitter i cellmembranet och fungerar som en mikroskopisk pump som skjuter desinfektionsmedel och andra skadliga molekyler ut ur cellen. Den andra delen, AmvR, agerar som en genetisk av/på-brytare som normalt håller pumpen i schack. Genom att skanna hundratals bakteriella genom hittade teamet versioner av båda delarna i nästan alla tillgängliga A. baumannii-stammar, vilket antyder att detta system är centralt för hur bakterien överlever hårda förhållanden på sjukhus, inklusive frekvent kontakt med desinfektionsmedel som klorhexidin.
Hur förändring av systemet påverkar rörelse och slem
För att förstå vad AmvAR gör utöver läkemedelsresistens skapade forskarna mutanter som saknade antingen pumpen eller dess regulator och jämförde dem med den normala stammen. De såg att borttagning av AmvR, regulatorn, gjorde bakterien mindre förmögen att sprida sig över en mjuk yta, vilket visade nedsatt rörlighet. Båda mutanterna, som saknade antingen pumpen eller regulatorn, bildade mycket svagare biofilmer: de klibbiga, lager-på-lager-samhällena på plast och glas som hjälper bakterier att fästa vid medicinska implantat och motstå rengöring. När forskarna återinförde de saknade generna kunde de återställa eller till och med öka biofilmbildningen, vilket tyder på att rätt balans i detta system är avgörande för att bygga stabila ytsamfund.
Hur bakterien greppar värdceller
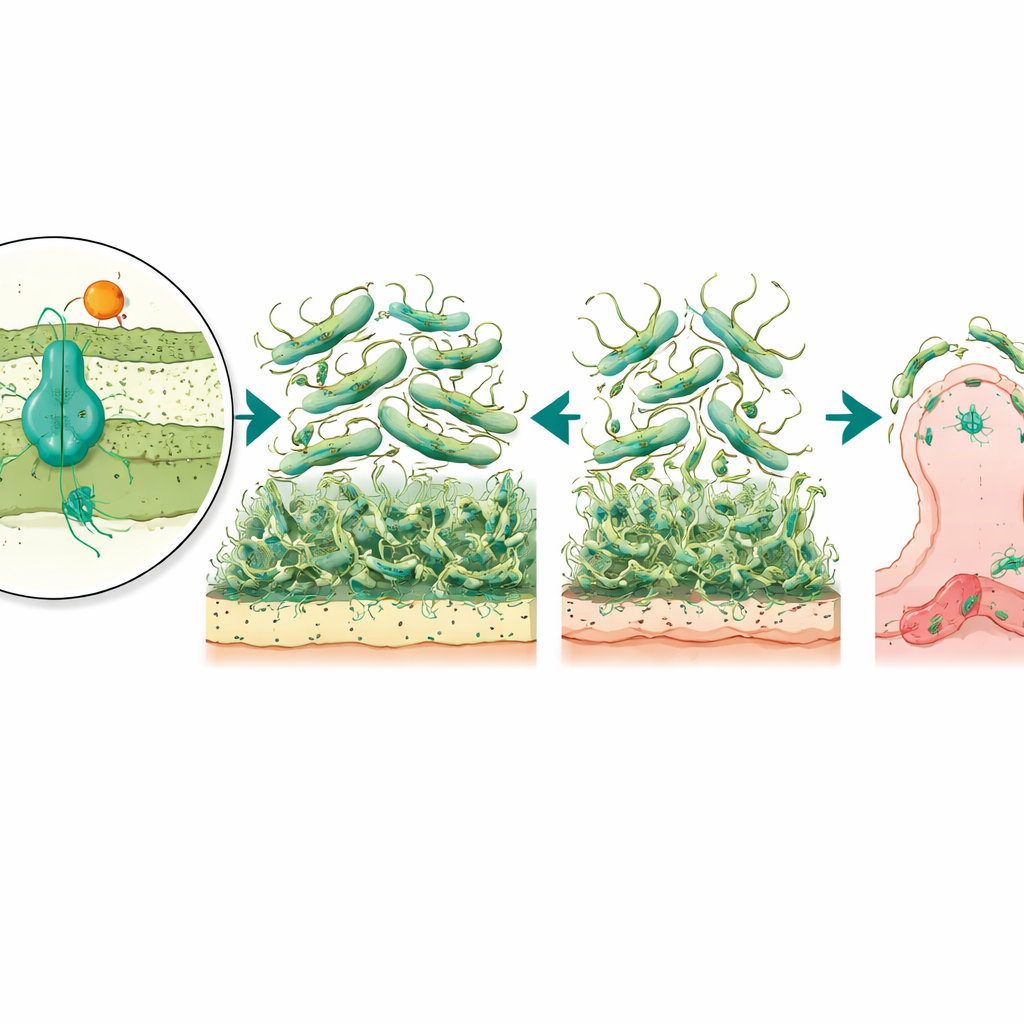
Eftersom biofilmer och yttre strukturer hjälper bakterier att greppa mänsklig vävnad testade teamet next hur väl mutanterna kunde fästa vid blåsceller odlade i laboratoriet, en modell för urinvägsinfektioner. Båda mutanterna fäste mycket sämre än den normala stammen, där varianten utan pumpen visade den största minskningen i vidhäftning. Detta tyder på att AmvAR-systemet inte bara hjälper bakterien att stå emot desinfektionsmedel utan också finjusterar dess yttre yta så att den kan haka fast vid våra celler. Som stöd för denna idé visade regulator-mutanten en dramatisk överproduktion av en pilussubunit, en byggsten i hår-liknande fibrer som medierar ytfästning. Paradoxalt nog kopplades denna överproduktion till sämre biofilmer och rörelse, vilket antyder att för många eller dåligt koordinerade fibrer faktiskt kan störa normalt ytbeteende.
Från vaxmalar till sjukdomsgrad
För att knyta dessa laboratoriefynd till verkliga infektioner vände sig forskarna till en levande modell: larver av vaxmott Galleria mellonella, en etablerad modell för att studera bakteriers virulens. När de infekterades med den normala A. baumannii-stammen dog många larver, men de som infekterades med regulatorn saknande mutant överlevde i mycket högre grad. I kontrast påverkade borttagning av endast pumpen inte den totala sjukdomsgraden. Detta mönster tyder på att AmvR, regulatorn, spelar en bredare koordinerande roll i kontrollen av egenskaper som rörlighet, biofilmbildning och celladhesion, som tillsammans avgör hur väl bakterien kan invadera och kvarstå i en värd.
Vad detta betyder för framtida behandlingar
Enkelt uttryckt visar detta arbete att AmvAR-systemet hos A. baumannii är mer än en kemisk pump: det hjälper till att forma bakteriens yttre hölje, dess förmåga att röra sig, att fästa vid ytor, att bygga skyddande slemlager och i slutändan att orsaka sjukdom. Att störa endast pumpen kan därför inte räcka för att tygla infektionen, men att störa regulatorn eller dess kopplade vägar kan försvaga flera viktiga överlevnadstrick samtidigt. Det gör AmvAR, och liknande kontrollsystem, till lovande mål för nya strategier som syftar till både att övervinna antibiotikaresistens och dämpa virulensen hos denna envisa sjukhusbakterie.
Citering: Gaona, M., Corral, J., Sánchez-Osuna, M. et al. Role of the AmvAR efflux system on the pathogenesis of Acinetobacter baumannii. Sci Rep 16, 10753 (2026). https://doi.org/10.1038/s41598-026-46007-w
Nyckelord: Acinetobacter baumannii, effluxpumpar, biofilm, antimikrobiell resistens, bakteriell virulens