Clear Sky Science · pt
Papel do sistema de efluxo AmvAR na patogênese de Acinetobacter baumannii
Por que esse microrganismo hospitalar importa
Acinetobacter baumannii é um microrganismo hospitalar de difícil erradicação que pode causar pneumonia, infecções sanguíneas e infecções graves em feridas e no trato urinário, especialmente em pacientes muito doentes. É notório por resistir a muitos antibióticos e até a certos desinfetantes, o que o coloca como uma das maiores ameaças na lista de preocupação crítica da Organização Mundial da Saúde. Este estudo faz uma pergunta central: além de ajudar a bactéria a expulsar substâncias tóxicas, um de seus sistemas de defesa também a torna melhor em aderir a superfícies, formar comunidades viscosas e causar doença?
Uma dupla ferramenta para a sobrevivência
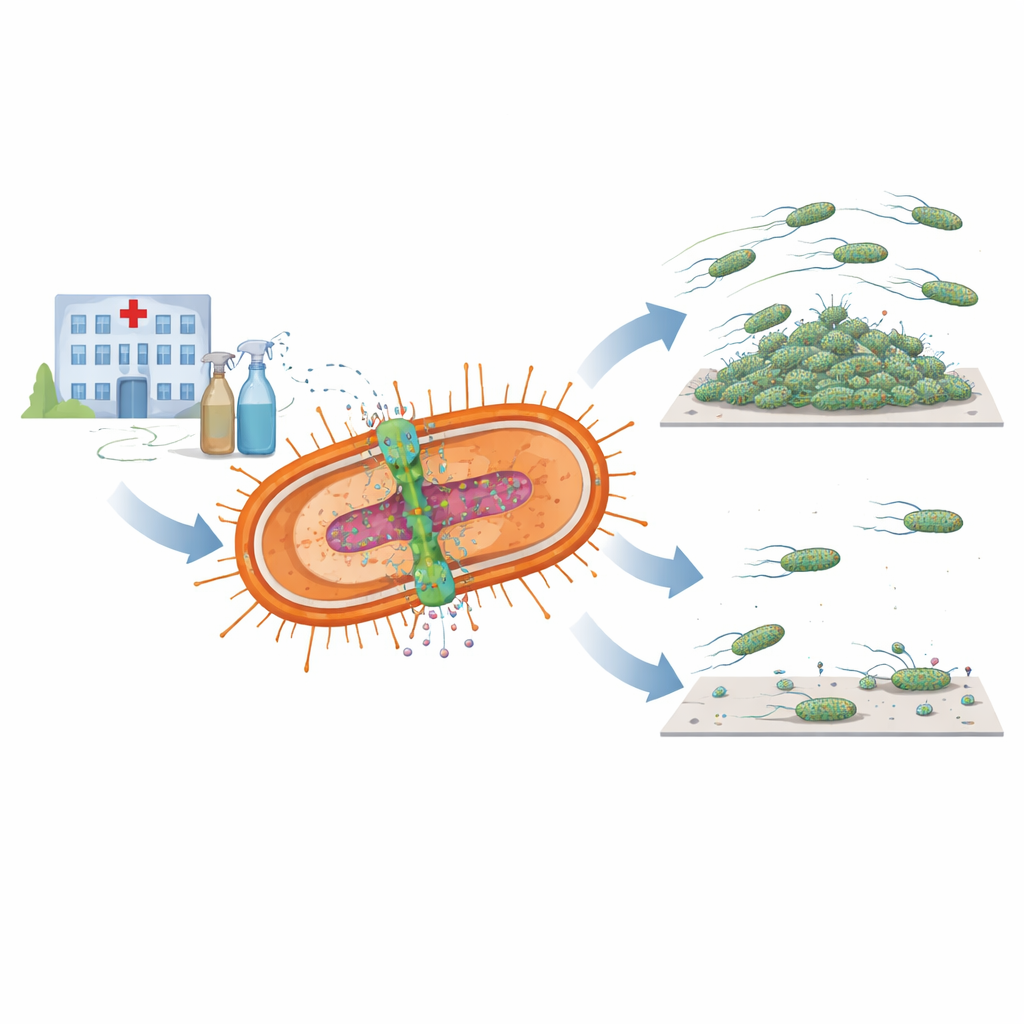
Os pesquisadores focaram em um par de componentes bacterianos intimamente ligados, conhecidos em conjunto como sistema AmvAR. Uma parte, AmvA, fica na membrana celular e funciona como uma bomba microscópica que expulsa desinfetantes e outras moléculas nocivas para fora da célula. A outra parte, AmvR, atua como um interruptor genético que normalmente mantém a bomba sob controle. Ao examinar centenas de genomas bacterianos, a equipe encontrou versões de ambas as partes em quase todas as cepas disponíveis de A. baumannii, sugerindo que esse sistema é central para a sobrevivência do microrganismo em condições adversas de hospitais, incluindo o contato frequente com desinfetantes como a clorexidina.
Como alterar esse sistema muda movimento e muco
Para entender o que o AmvAR faz além da resistência a drogas, os cientistas criaram bactérias mutantes sem a bomba ou sem seu regulador e as compararam à linhagem normal. Eles observaram que remover AmvR, o regulador, tornou a bactéria menos capaz de se espalhar sobre uma superfície macia, mostrando motilidade prejudicada. Ambos os mutantes, sem a bomba ou sem o regulador, formaram biofilmes muito mais fracos: as comunidades pegajosas e em camadas sobre plástico e vidro que ajudam as bactérias a aderir a dispositivos médicos e resistir à limpeza. Quando os pesquisadores reintroduziram os genes ausentes, conseguiram restaurar ou até aumentar a formação de biofilme, sugerindo que o equilíbrio adequado desse sistema é crucial para construir comunidades estáveis na superfície.
Como a bactéria se prende às células do hospedeiro
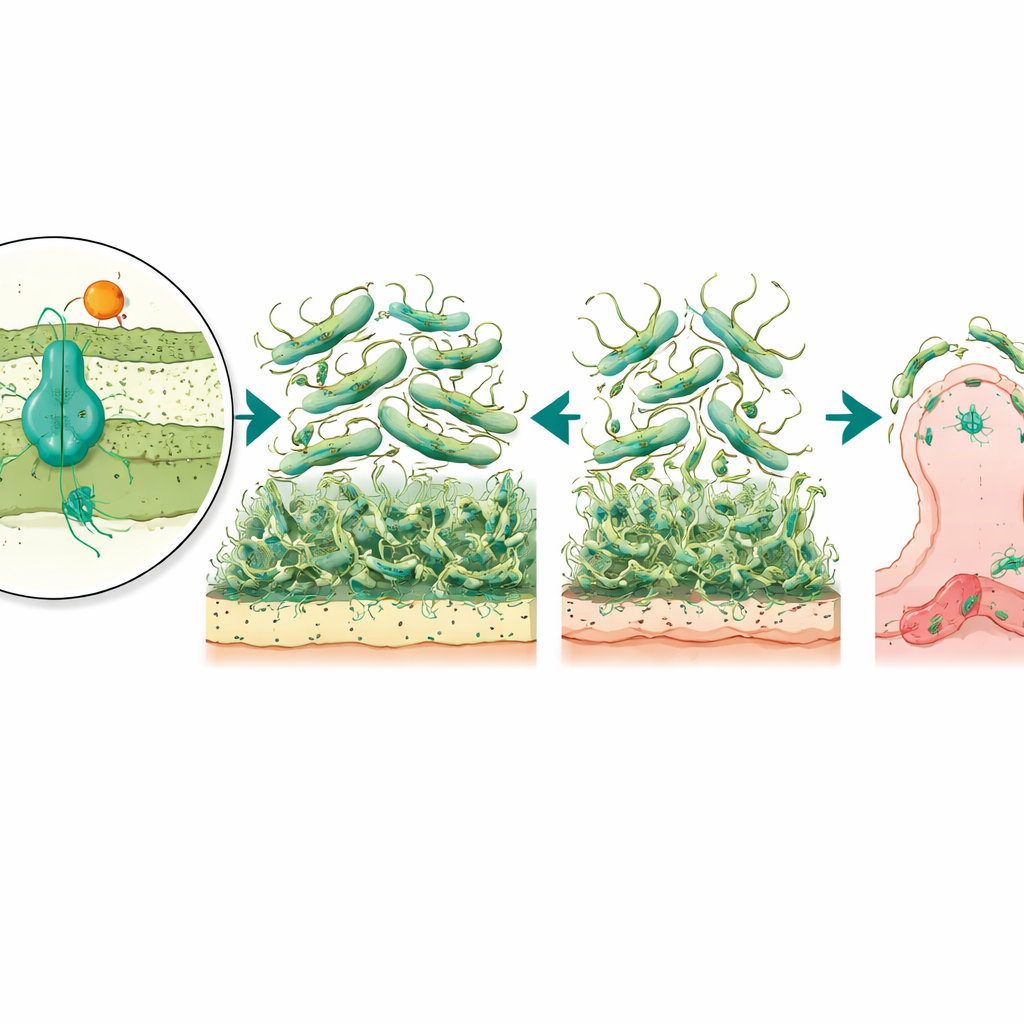
Como biofilmes e estruturas de superfície ajudam as bactérias a se agarrar aos tecidos humanos, a equipe testou em seguida quão bem os mutantes conseguiam se anexar a células da bexiga cultivadas em laboratório, um modelo para infecções do trato urinário. Ambos os mutantes aderiram muito menos do que a linhagem normal, com a versão sem a bomba apresentando a maior queda na fixação. Isso sugere que o sistema AmvAR não apenas ajuda a bactéria a resistir a desinfetantes, mas também ajusta sua superfície externa para que ela possa se ligar às nossas células. Apoiando essa ideia, o mutante do regulador mostrou uma superprodução dramática de uma subunidade de píleo, um bloco de construção de fibras semelhantes a pelos que mediam a adesão à superfície. Paradoxalmente, essa superprodução esteve ligada a biofilmes e movimento piores, o que implica que fibras em excesso ou mal coordenadas podem de fato atrapalhar o comportamento normal na superfície.
De larvas de traça à gravidade da doença
Para conectar esses achados de laboratório à infecção real, os cientistas recorreram a um modelo vivo: larvas da traça-da-cera Galleria mellonella, um modelo estabelecido para estudar a virulência bacteriana. Quando infectadas com a linhagem normal de A. baumannii, muitas larvas morreram, mas aquelas infectadas com o mutante sem o regulador sobreviveram em taxas muito mais altas. Em contraste, remover apenas a bomba deixou a gravidade geral da doença inalterada. Esse padrão sugere que AmvR, o regulador, desempenha um papel mais amplo de coordenação no controle de características como movimento, formação de biofilme e adesão celular que, em conjunto, determinam quão bem a bactéria pode invadir e persistir dentro de um hospedeiro.
O que isso significa para tratamentos futuros
Em termos simples, este trabalho mostra que o sistema AmvAR em A. baumannii é mais do que uma bomba química: ele ajuda a moldar o revestimento externo do microrganismo, sua capacidade de se mover, de se colar a superfícies, de construir camadas protetoras de muco e, em última instância, de causar doença. Interromper apenas a bomba pode não ser suficiente para controlar a infecção, mas interferir no regulador ou em suas vias conectadas pode enfraquecer vários truques-chave de sobrevivência de uma só vez. Isso torna o AmvAR, e sistemas de controle semelhantes, alvos promissores para novas estratégias que visem tanto superar a resistência a antibióticos quanto reduzir a virulência desse persistente patógeno hospitalar.
Citação: Gaona, M., Corral, J., Sánchez-Osuna, M. et al. Role of the AmvAR efflux system on the pathogenesis of Acinetobacter baumannii. Sci Rep 16, 10753 (2026). https://doi.org/10.1038/s41598-026-46007-w
Palavras-chave: Acinetobacter baumannii, bombas de efluxo, biofilme, resistência antimicrobiana, virulência bacteriana