Clear Sky Science · pl
Rola systemu efflux AmvAR w patogenezie Acinetobacter baumannii
Dlaczego ten szpitalny drobnoustrój ma znaczenie
Acinetobacter baumannii to trudny do zwalczenia drobnoustrój szpitalny, który może powodować zapalenie płuc, zakażenia krwi oraz poważne zakażenia ran i dróg moczowych, zwłaszcza u pacjentów w ciężkim stanie. Słynie z odporności na wiele antybiotyków, a nawet na niektóre środki dezynfekujące, co sprawia, że znajduje się na liście krytycznych zagrożeń Światowej Organizacji Zdrowia. W tym badaniu postawiono kluczowe pytanie: poza pomocą w wypompowywaniu toksycznych związków, czy jeden z jego systemów obronnych zwiększa też zdolność bakterii do przylegania do powierzchni, tworzenia śluzowych skupisk i wywoływania choroby?
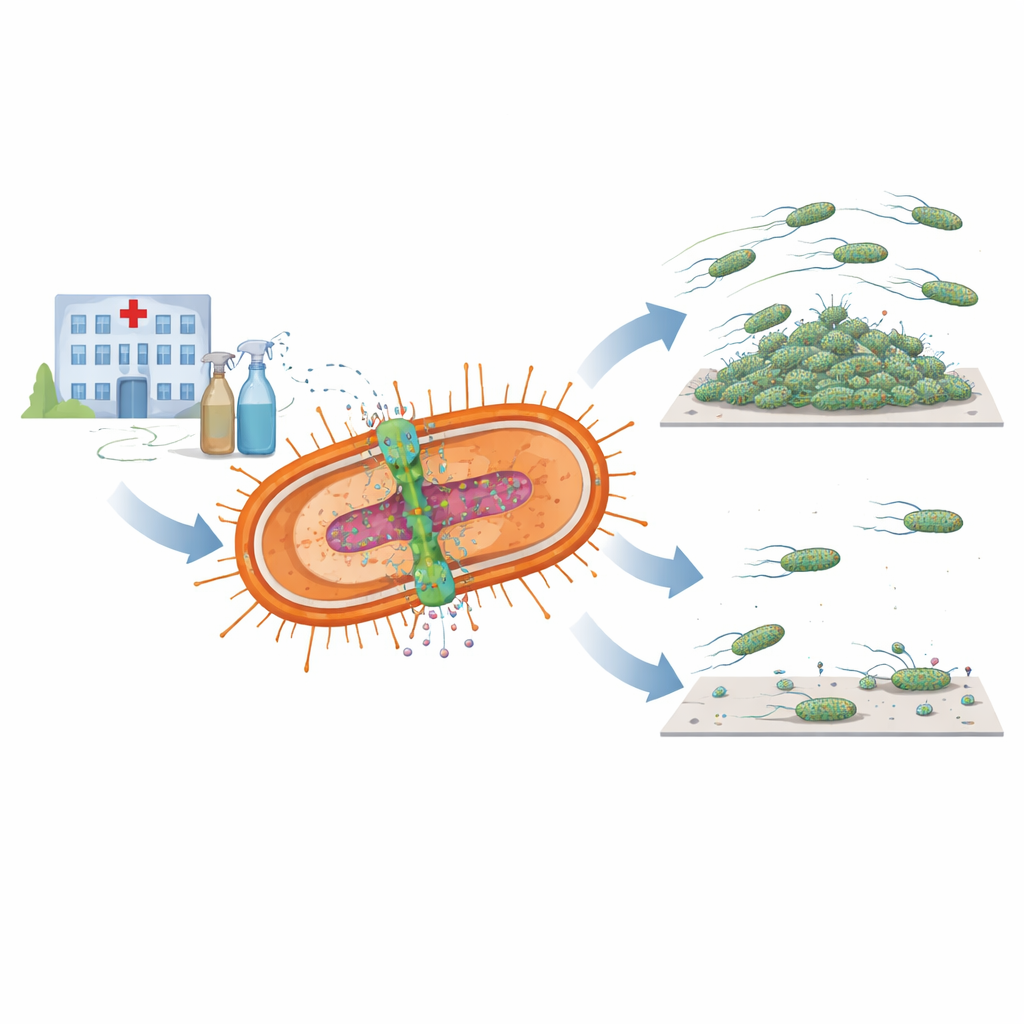
Podwójne narzędzie do przetrwania
Naukowcy skupili się na parze blisko powiązanych składników bakterii znanych razem jako system AmvAR. Jedna część, AmvA, osadzona jest w błonie komórkowej i działa jak mikroskopijna pompa, która wypycha środki dezynfekujące i inne szkodliwe cząsteczki na zewnątrz komórki. Druga część, AmvR, pełni rolę genetycznego włącznika/wyłącznika, który zwykle hamuje działanie pompy. Przeszukując setki genomów bakteryjnych, zespół znalazł wersje obu składników w niemal wszystkich dostępnych szczepach A. baumannii, co sugeruje, że system ten jest kluczowy dla przetrwania drobnoustroju w trudnych warunkach szpitalnych, w tym przy częstym kontakcie ze środkami dezynfekcyjnymi takimi jak chloroheksydyna.
Jak zmiany w tym systemie wpływają na ruch i śluz
Aby zrozumieć, co AmvAR robi poza opornością na leki, naukowcy stworzyli mutanty bakteryjne pozbawione albo pompy, albo jej regulatora, i porównali je ze szczepem referencyjnym. Zaobserwowali, że usunięcie AmvR, regulatora, zmniejszało zdolność bakterii do rozprzestrzeniania się po miękkiej powierzchni, co wskazywało na upośledzoną motoryczność. Oba mutanty, zarówno pozbawiony pompy, jak i regulatora, tworzyły znacznie słabsze biofilmy — lepkie, warstwowe społeczności na plastiku i szkle, które pomagają bakteriom przyczepiać się do urządzeń medycznych i opierać się czyszczeniu. Gdy badacze ponownie wprowadzili brakujące geny, mogli przywrócić, a nawet zwiększyć tworzenie biofilmu, co sugeruje, że właściwa równowaga tego systemu jest kluczowa dla budowy stabilnych społeczności powierzchniowych.
Jak bakteria przyczepia się do komórek gospodarza
Ponieważ biofilmy i struktury powierzchniowe pomagają bakteriom chwytać tkanki ludzkie, zespół sprawdził następnie, jak mutanty radzą sobie z przyleganiem do hodowanych w laboratorium komórek pęcherza, będących modelem zakażeń dróg moczowych. Oba mutanty przyczepiały się znacznie gorzej niż szczep normalny, przy czym wariant pozbawiony pompy wykazywał największy spadek przylegania. Sugeruje to, że system AmvAR nie tylko pomaga bakterii przeciwstawiać się środkom dezynfekującym, ale też precyzuje jej zewnętrzną powłokę, umożliwiając przyczepianie się do naszych komórek. Wspierając tę ideę, mutant pozbawiony regulatora wykazywał dramatycznie zwiększoną produkcję podjednostki pilusa — elementu budulcowego włosopodobnych włókien pośredniczących w przyczepności. Paradoksalnie, nadprodukcja ta wiązała się z gorszymi biofilmami i ruchem, co sugeruje, że zbyt dużo lub źle skoordynowanych włókien może zaburzać normalne zachowania powierzchniowe.
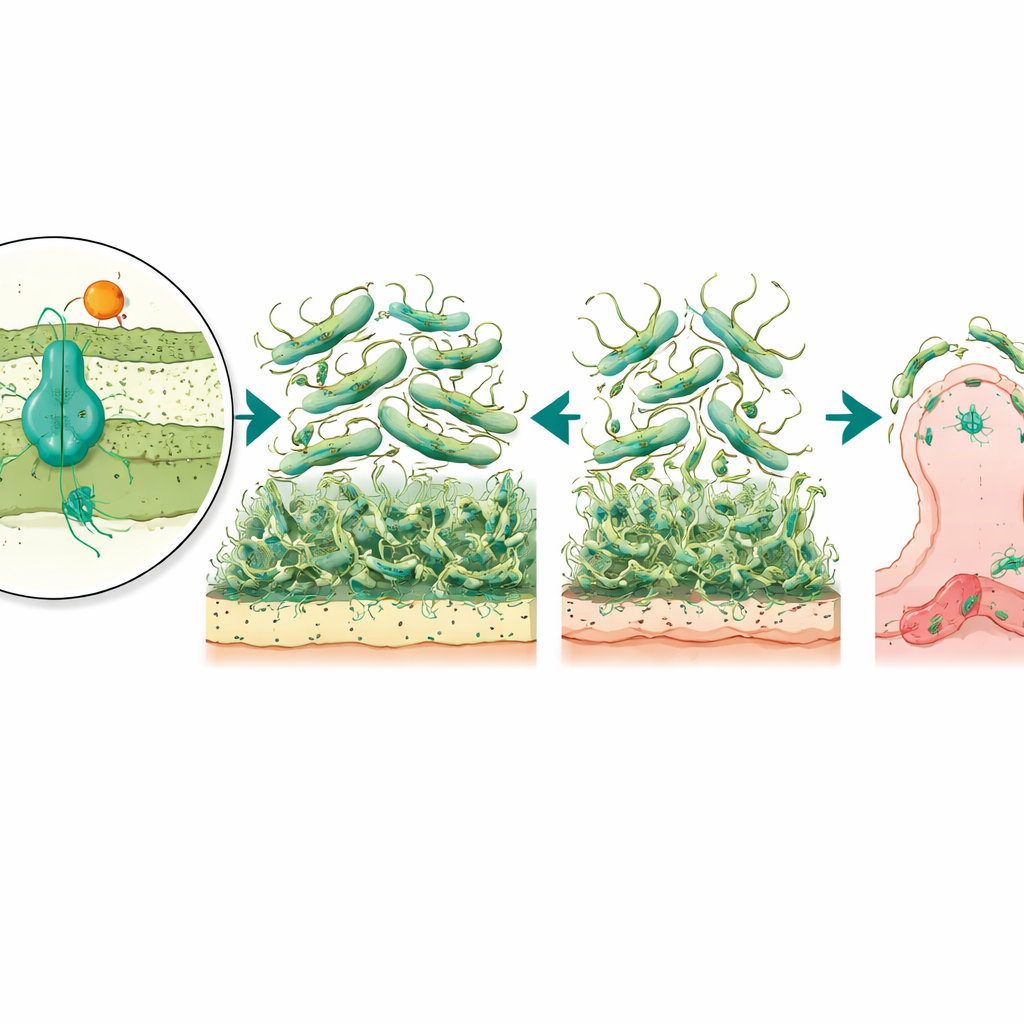
Od gąsienic woszczyn do nasilenia choroby
Aby powiązać te laboratoryjne odkrycia z rzeczywistą infekcją, badacze sięgnęli po model żywy: larwy ćmy woskowej Galleria mellonella, powszechnie stosowane jako model do badania zjadliwości bakteryjnej. Po zakażeniu szczepem referencyjnym A. baumannii wiele larw zginęło, podczas gdy te zakażone mutantem pozbawionym regulatora przeżywały w znacznie większym odsetku. W przeciwieństwie do tego, usunięcie wyłącznie pompy nie zmieniało ogólnego ciężaru choroby. Ten wzorzec sugeruje, że AmvR, regulator, pełni szerszą rolę koordynacyjną w kontroli cech takich jak ruch, tworzenie biofilmu i przyczepność do komórek, które razem decydują o zdolności bakterii do inwazji i przetrwania w organizmie gospodarza.
Co to oznacza dla przyszłych terapii
Mówiąc prosto, praca ta pokazuje, że system AmvAR w A. baumannii to coś więcej niż pompa chemiczna: kształtuje zewnętrzną powłokę drobnoustroju, jego zdolność do ruchu, przyklejania się do powierzchni, budowania ochronnych warstw śluzu i ostatecznie wywoływania choroby. Zakłócenie samej pompy może nie wystarczyć, by okiełznać infekcję, ale ingerencja w regulator lub skojarzone szlaki mogłaby osłabić kilka kluczowych mechanizmów przetrwania jednocześnie. To czyni AmvAR i podobne systemy kontrolne obiecującymi celami dla nowych strategii mających zarówno przezwyciężać oporność na antybiotyki, jak i redukować zjadliwość tego opornego patogenu szpitalnego.
Cytowanie: Gaona, M., Corral, J., Sánchez-Osuna, M. et al. Role of the AmvAR efflux system on the pathogenesis of Acinetobacter baumannii. Sci Rep 16, 10753 (2026). https://doi.org/10.1038/s41598-026-46007-w
Słowa kluczowe: Acinetobacter baumannii, pompy wypompowujące, biofilm, oporność na środki przeciwdrobnoustrojowe, zjadliwość bakterii