Clear Sky Science · fr
Rôle du système d’efflux AmvAR dans la pathogenèse d’Acinetobacter baumannii
Pourquoi ce germe hospitalier compte
Acinetobacter baumannii est un germe nosocomial difficile à éliminer qui peut provoquer des pneumonies, des infections sanguines, et des infections sévères de plaies et des voies urinaires, en particulier chez les patients très malades. Il est tristement célèbre pour résister à de nombreux antibiotiques et même à certains désinfectants, ce qui en fait une préoccupation majeure sur la liste des menaces critiques de l’Organisation mondiale de la Santé. Cette étude pose une question centrale : au‑delà d’aider la bactérie à expulser des molécules toxiques, l’un de ses systèmes de défense améliore‑t‑il aussi sa capacité à adhérer aux surfaces, à former des communautés visqueuses et à provoquer la maladie ?
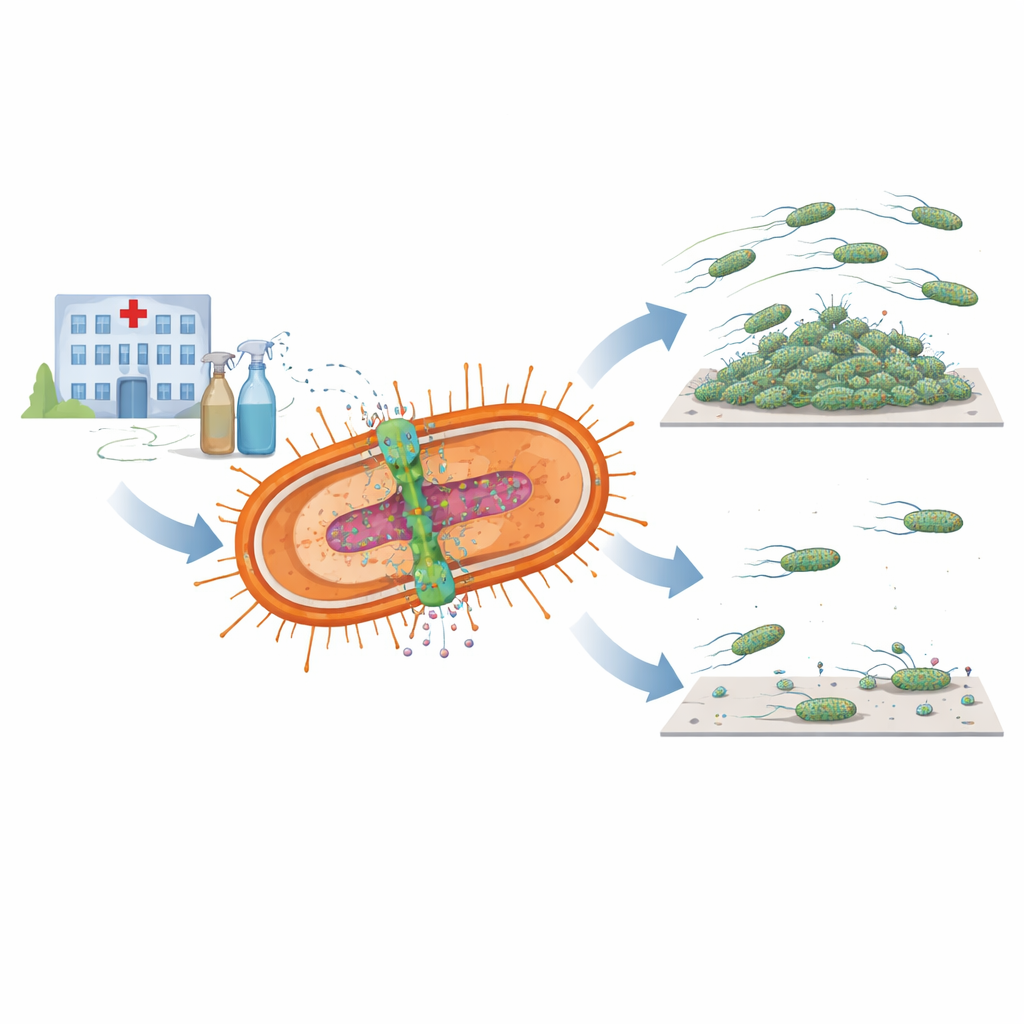
Un double outil pour la survie
Les chercheurs se sont concentrés sur une paire de composants bactériens étroitement liés, connus sous le nom de système AmvAR. Une partie, AmvA, se situe dans la membrane cellulaire et fonctionne comme une pompe microscopique qui expulse les désinfectants et d’autres molécules nocives hors de la cellule. L’autre partie, AmvR, agit comme un interrupteur génétique marche–arrêt qui maintient normalement la pompe sous contrôle. En analysant des centaines de génomes bactériens, l’équipe a trouvé des versions des deux composants dans presque toutes les souches disponibles d’A. baumannii, ce qui suggère que ce système est central pour la survie du germe dans les conditions hostiles des hôpitaux, notamment l’exposition fréquente à des désinfectants comme la chlorhexidine.
Comment la modification de ce système change la mobilité et le mucus
Pour comprendre ce que fait AmvAR en dehors de la résistance aux médicaments, les scientifiques ont créé des mutants bactériens dépourvus soit de la pompe soit de son régulateur et les ont comparés à la souche normale. Ils ont constaté que la suppression d’AmvR, le régulateur, réduisait la capacité de la bactérie à se propager sur une surface molle, révélant une mobilité altérée. Les deux mutants, dépourvus soit de la pompe soit du régulateur, formaient des biofilms beaucoup plus faibles : ces communautés collantes et stratifiées sur plastique et verre aident les bactéries à adhérer aux dispositifs médicaux et à résister au nettoyage. Lorsque les chercheurs ont réintroduit les gènes manquants, ils ont pu restaurer ou même renforcer la formation de biofilm, ce qui suggère qu’un équilibre approprié de ce système est crucial pour construire des communautés de surface stables.
Comment la bactérie s’accroche aux cellules hôtes
Parce que les biofilms et les structures de surface aident les bactéries à s’agripper aux tissus humains, l’équipe a testé ensuite la capacité des mutants à se fixer sur des cellules de la vessie cultivées en laboratoire, un modèle pour les infections urinaires. Les deux mutants adhéraient beaucoup moins efficacement que la souche normale, la version sans pompe montrant la plus forte diminution d’attachement. Cela suggère que le système AmvAR n’aide pas seulement la bactérie à résister aux désinfectants, mais ajuste aussi sa surface externe afin de mieux se fixer à nos cellules. À l’appui de cette idée, le mutant du régulateur présentait une surproduction spectaculaire d’une sous‑unité de pilus, un élément constituant de fibres en forme de poils qui médiatisent l’attachement de surface. Paradoxalement, cette surproduction était liée à des biofilms et une mobilité plus faibles, ce qui implique qu’un excès ou une coordination défectueuse des fibres peut en réalité perturber le comportement de surface normal.
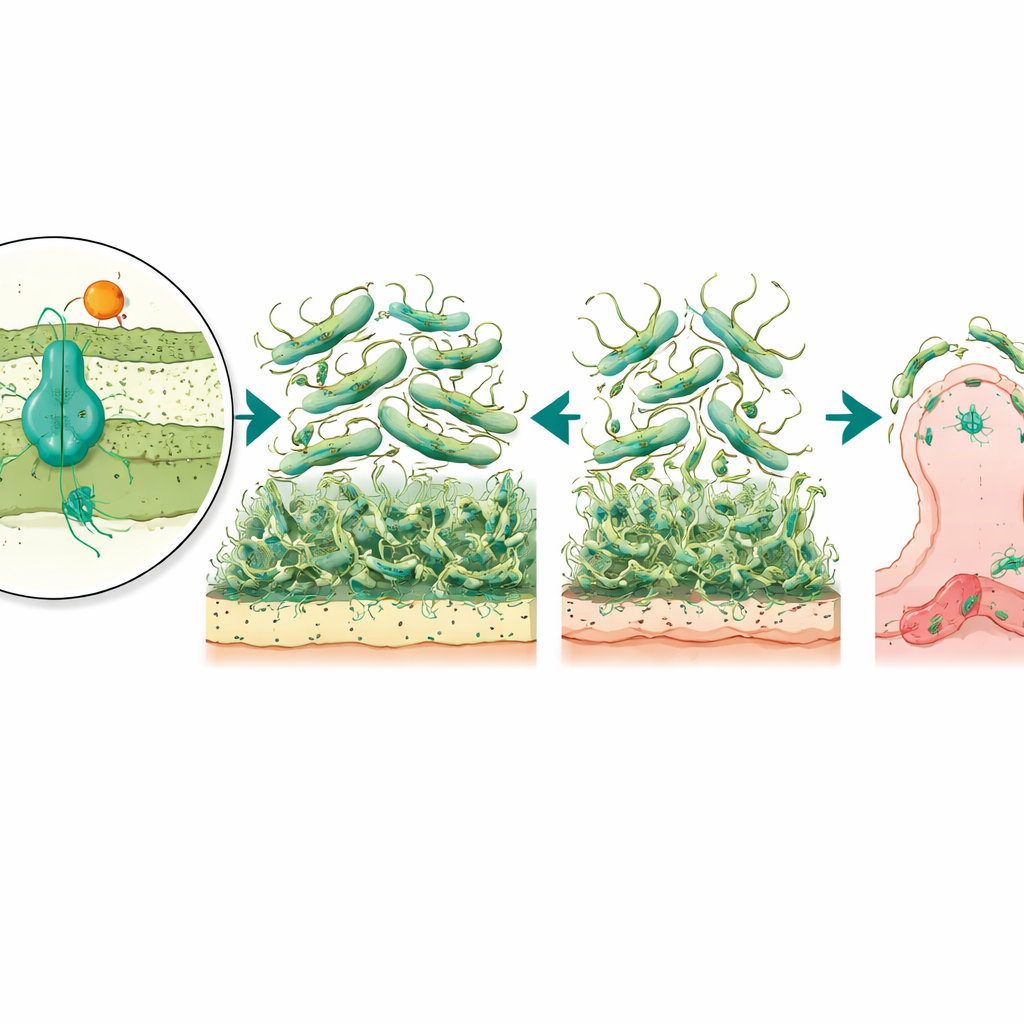
Des vers de cire à la sévérité de la maladie
Pour relier ces observations de laboratoire à l’infection réelle, les scientifiques ont utilisé un modèle vivant : les larves de la teigne de la cire Galleria mellonella, un substitut établi pour étudier la virulence bactérienne. Lorsqu’elles étaient infectées par la souche normale d’A. baumannii, de nombreuses larves mouraient, mais celles infectées par le mutant dépourvu du régulateur survivaient à des taux beaucoup plus élevés. En revanche, la suppression de la seule pompe n’a pas modifié la gravité globale de la maladie. Ce schéma suggère qu’AmvR, le régulateur, joue un rôle coordonnateur plus large dans le contrôle de traits tels que la motilité, la formation de biofilm et l’attachement cellulaire qui déterminent ensemble la capacité de la bactérie à envahir et à persister chez un hôte.
Ce que cela signifie pour les traitements futurs
En termes simples, ce travail montre que le système AmvAR chez A. baumannii est plus qu’une pompe chimique : il contribue à façonner la couche externe du germe, sa capacité à se déplacer, à se coller aux surfaces, à construire des couches protectrices de mucus et, in fine, à provoquer la maladie. Perturber uniquement la pompe peut ne pas suffire à maîtriser l’infection, mais interférer avec le régulateur ou ses voies associées pourrait affaiblir plusieurs stratégies de survie clés en une seule fois. Cela fait d’AmvAR, et de systèmes de contrôle similaires, des cibles prometteuses pour de nouvelles stratégies visant à la fois à surmonter la résistance aux antibiotiques et à diminuer la virulence de ce pathogène hospitalier tenace.
Citation: Gaona, M., Corral, J., Sánchez-Osuna, M. et al. Role of the AmvAR efflux system on the pathogenesis of Acinetobacter baumannii. Sci Rep 16, 10753 (2026). https://doi.org/10.1038/s41598-026-46007-w
Mots-clés: Acinetobacter baumannii, pompes d’efflux, biofilm, résistance aux antimicrobiens, virulence bactérienne