Clear Sky Science · de
Rolle des AmvAR-Effluxsystems bei der Pathogenese von Acinetobacter baumannii
Warum dieses Krankenhauskeim wichtig ist
Acinetobacter baumannii ist ein schwer zu bekämpfender Krankenhauskeim, der vor allem bei schwer kranken Patientinnen und Patienten Pneumonien, Blutinfektionen sowie schwere Wund- und Harnwegsinfektionen auslösen kann. Er ist berüchtigt dafür, vielen Antibiotika und sogar einigen Desinfektionsmitteln zu widerstehen, weshalb er auf der Liste der kritischen Bedrohungen der Weltgesundheitsorganisation steht. Diese Studie geht einer zentralen Frage nach: Trägt eines seiner Abwehrsysteme neben dem Auspumpen toxischer Substanzen auch dazu bei, dass der Erreger besser an Oberflächen haftet, schleimige Gemeinschaften bildet und Krankheiten verursacht?
Ein doppeltes Werkzeug zum Überleben
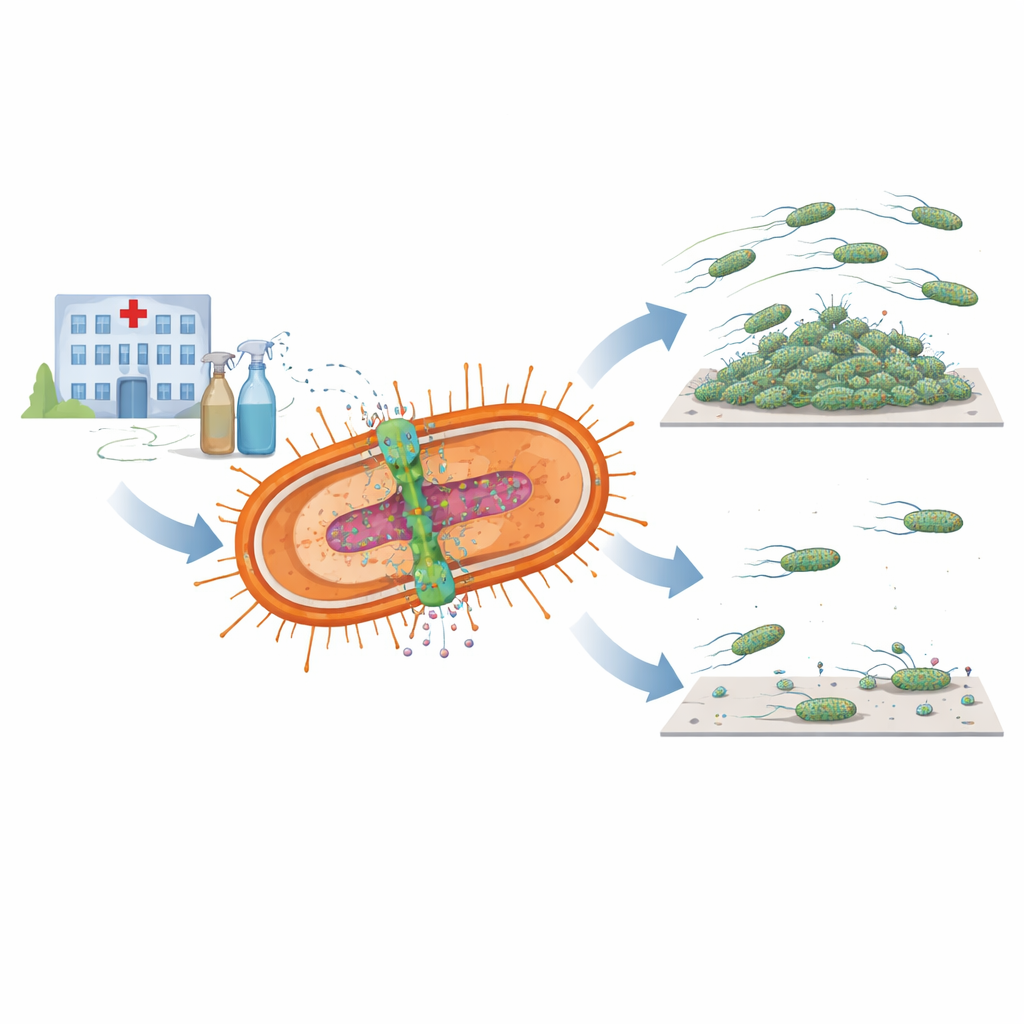
Die Forschenden konzentrierten sich auf ein Paar eng verbundener bakterieller Komponenten, das zusammen als AmvAR-System bekannt ist. Ein Teil, AmvA, sitzt in der Zellmembran und arbeitet wie eine mikroskopische Pumpe, die Desinfektionsmittel und andere schädliche Moleküle aus der Zelle herausschiebt. Der andere Teil, AmvR, fungiert als genetischer Ein–Aus-Schalter, der die Pumpe normalerweise in Schach hält. Beim Durchsuchen hunderter bakterieller Genome fanden die Autorinnen und Autoren Versionen beider Komponenten in fast allen verfügbaren A.-baumannii-Stämmen, was darauf hindeutet, dass dieses System zentral für das Überleben des Keims unter den im Krankenhaus herrschenden harten Bedingungen ist, etwa bei häufigem Kontakt mit Desinfektionsmitteln wie Chlorhexidin.
Wie Veränderungen dieses Systems Bewegung und Schleimbildung verändern
Um zu verstehen, was AmvAR über die Arzneimittelempfindlichkeit hinaus bewirkt, erzeugten die Wissenschaftlerinnen und Wissenschaftler Mutanten, denen entweder die Pumpe oder ihr Regulator fehlte, und verglichen diese mit dem normalen Stamm. Sie stellten fest, dass das Entfernen von AmvR, dem Regulator, die Fähigkeit des Bakteriums, sich über eine weiche Oberfläche auszubreiten, verringerte und so die Motilität schwächte. Beide Mutanten, sowohl ohne Pumpe als auch ohne Regulator, bildeten deutlich schwächere Biofilme: die klebrigen, geschichteten Gemeinschaften auf Plastik und Glas, die Bakterien helfen, an medizinischen Geräten zu haften und Reinigungsmaßnahmen zu widerstehen. Als die Forschenden die fehlenden Gene wieder einführten, konnten sie die Biofilmbildung wiederherstellen oder sogar steigern, was darauf hindeutet, dass das richtige Gleichgewicht dieses Systems entscheidend für den Aufbau stabiler Oberflächengemeinschaften ist.
Wie das Bakterium an Wirtszellen haftet
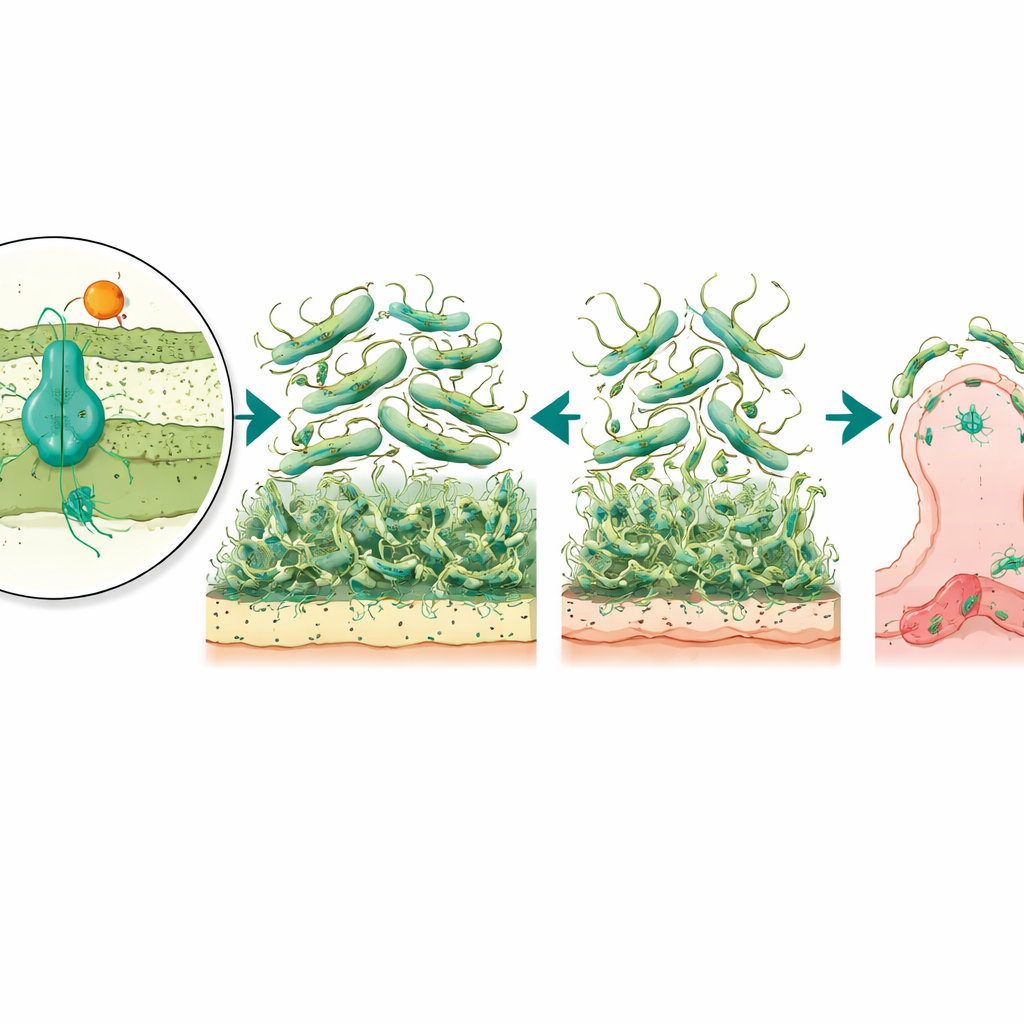
Da Biofilme und Oberflächenstrukturen Bakterien dabei helfen, an menschlichem Gewebe zu haften, prüfte das Team als Nächstes, wie gut die Mutanten an im Labor gezüchtete Blasenzellen anheften können, ein Modell für Harnwegsinfektionen. Beide Mutanten hafteten deutlich schlechter als der normale Stamm, wobei die Variante ohne Pumpe den stärksten Rückgang der Anhaftung zeigte. Das legt nahe, dass das AmvAR-System nicht nur dem Bakterium beim Widerstehen von Desinfektionsmitteln hilft, sondern auch seine Außenhülle so abstimmt, dass es an unsere Zellen andocken kann. Diese Idee wird gestützt durch die Beobachtung, dass der Regulatormutant eine dramatische Überproduktion einer Pili-Untereinheit zeigte, eines Bausteins haarähnlicher Fasern, die die Oberflächenanheftung vermitteln. Paradoxerweise war diese Überproduktion mit schlechteren Biofilmen und geringerer Bewegung verbunden, was darauf hindeutet, dass zu viele oder schlecht koordinierte Fasern das normale Oberflächenverhalten stören können.
Von Wachsraupen bis zur Krankheitsintensität
Um diese Laborbefunde mit realen Infektionen zu verknüpfen, verwendeten die Wissenschaftlerinnen und Wissenschaftler ein lebendes Modell: Larven der Wachsmotte Galleria mellonella, ein etabliertes Modell zur Untersuchung bakterieller Virulenz. Bei einer Infektion mit dem normalen A.-baumannii-Stamm starben viele Larven, während diejenigen, die mit dem Regulator-defizienten Mutanten infiziert wurden, deutlich höhere Überlebensraten zeigten. Das Entfernen nur der Pumpe veränderte dagegen die allgemeine Krankheitsintensität nicht. Dieses Muster legt nahe, dass AmvR, der Regulator, eine umfassendere koordinierende Rolle bei der Steuerung von Merkmalen wie Bewegung, Biofilmbildung und Zellanhaftung spielt, die zusammen bestimmen, wie gut der Erreger in einen Wirt eindringen und dort bestehen kann.
Was das für zukünftige Behandlungen bedeutet
Kurz gesagt zeigt diese Arbeit, dass das AmvAR-System in A. baumannii mehr ist als eine chemische Pumpe: Es prägt die Außenhülle des Keims, seine Beweglichkeit, seine Fähigkeit, sich an Oberflächen zu kleben, schützende Schleimschichten zu bilden und letztlich Krankheiten zu verursachen. Allein die Pumpe zu stören, reicht möglicherweise nicht aus, um eine Infektion zu bändigen; das Eingreifen in den Regulator oder seine verknüpften Signalwege könnte jedoch gleichzeitig mehrere wichtige Überlebensstrategien schwächen. Damit sind AmvAR und ähnliche Kontrollsysteme vielversprechende Ziele für neue Strategien, die sowohl die Antibiotikaresistenz überwinden als auch die Virulenz dieses hartnäckigen Krankenhauspathogens verringern sollen.
Zitation: Gaona, M., Corral, J., Sánchez-Osuna, M. et al. Role of the AmvAR efflux system on the pathogenesis of Acinetobacter baumannii. Sci Rep 16, 10753 (2026). https://doi.org/10.1038/s41598-026-46007-w
Schlüsselwörter: Acinetobacter baumannii, Effluxpumpen, Biofilm, antimikrobielle Resistenz, bakterielle Virulenz