Clear Sky Science · es
Papel del sistema de expulsión AmvAR en la patogénesis de Acinetobacter baumannii
Por qué importa este germen hospitalario
Acinetobacter baumannii es un germen hospitalario difícil de eliminar que puede causar neumonía, infecciones sanguíneas y afecciones graves en heridas y del tracto urinario, especialmente en pacientes muy enfermos. Es famoso por resistir muchos antibióticos e incluso algunos desinfectantes, lo que lo sitúa como una de las principales amenazas en la lista de la Organización Mundial de la Salud. Este estudio plantea una pregunta clave: además de ayudar a la bacteria a expulsar compuestos tóxicos, ¿hace uno de sus sistemas de defensa que sea mejor para adherirse a superficies, formar comunidades viscosa y causar enfermedad?
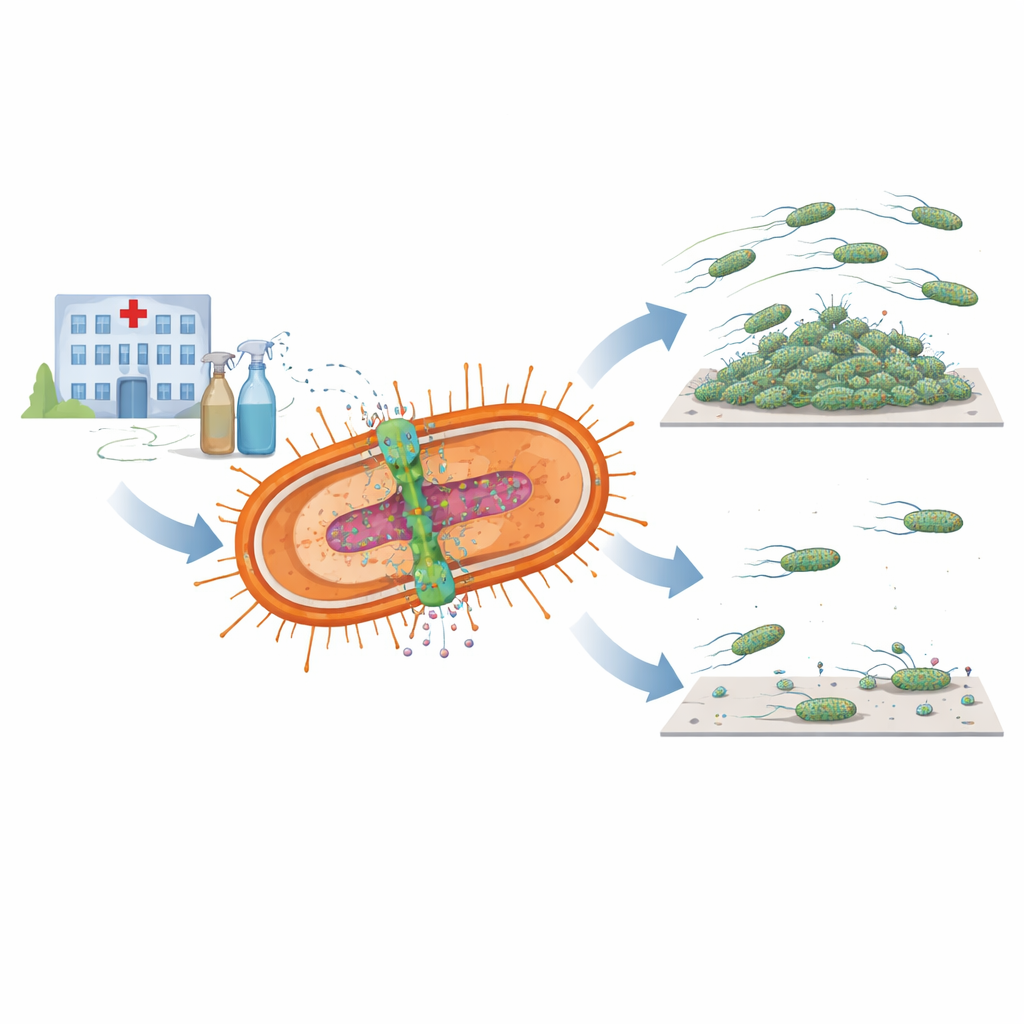
Una doble herramienta para la supervivencia
Los investigadores se centraron en un par de componentes bacterianos estrechamente vinculados conocidos conjuntamente como el sistema AmvAR. Una parte, AmvA, se sitúa en la membrana celular y actúa como una bomba microscópica que expulsa desinfectantes y otras moléculas dañinas fuera de la célula. La otra parte, AmvR, funciona como un interruptor genético que normalmente mantiene la bomba bajo control. Al analizar cientos de genomas bacterianos, el equipo encontró versiones de ambas partes en casi todas las cepas disponibles de A. baumannii, lo que sugiere que este sistema es central para que el germen sobreviva a condiciones adversas en hospitales, incluido el contacto frecuente con desinfectantes como la clorhexidina.
Cómo altera el movimiento y la mucosidad
Para entender qué hace AmvAR más allá de la resistencia a fármacos, los científicos crearon bacterias mutantes carentes de la bomba o de su regulador y las compararon con la cepa normal. Observaron que la eliminación de AmvR, el regulador, reducía la capacidad de la bacteria para desplazarse sobre una superficie blanda, mostrando una motilidad disminuida. Ambos mutantes, carentes de la bomba o del regulador, formaron biopelículas mucho más débiles: las comunidades pegajosas y estratificadas en plástico y vidrio que ayudan a las bacterias a adherirse a dispositivos médicos y resistir la limpieza. Cuando los investigadores reintrodujeron los genes ausentes, pudieron restaurar o incluso aumentar la formación de biopelículas, lo que sugiere que el equilibrio adecuado de este sistema es crucial para construir comunidades superficiales estables.
Cómo la bacteria se agarra a las células del huésped
Dado que las biopelículas y las estructuras superficiales ayudan a las bacterias a unirse a los tejidos humanos, el equipo probó a continuación qué tan bien podían adherirse los mutantes a células de la vejiga cultivadas en el laboratorio, un modelo para infecciones del tracto urinario. Ambos mutantes se adhirieron con mucha menos eficacia que la cepa normal, siendo el que carecía de la bomba el que mostró la mayor caída en adherencia. Esto sugiere que el sistema AmvAR no solo ayuda a la bacteria a resistir desinfectantes, sino que también ajusta finamente su superficie externa para poder anclarse a nuestras células. En apoyo de esta idea, el mutante del regulador mostró una producción dramáticamente aumentada de una subunidad de pili, un bloque de construcción de fibras tipo pelo que median la adhesión superficial. Paradójicamente, esta sobreproducción se relacionó con biopelículas y motilidad peores, lo que implica que un exceso o una coordinación deficiente de estas fibras puede perturbar el comportamiento superficial normal.
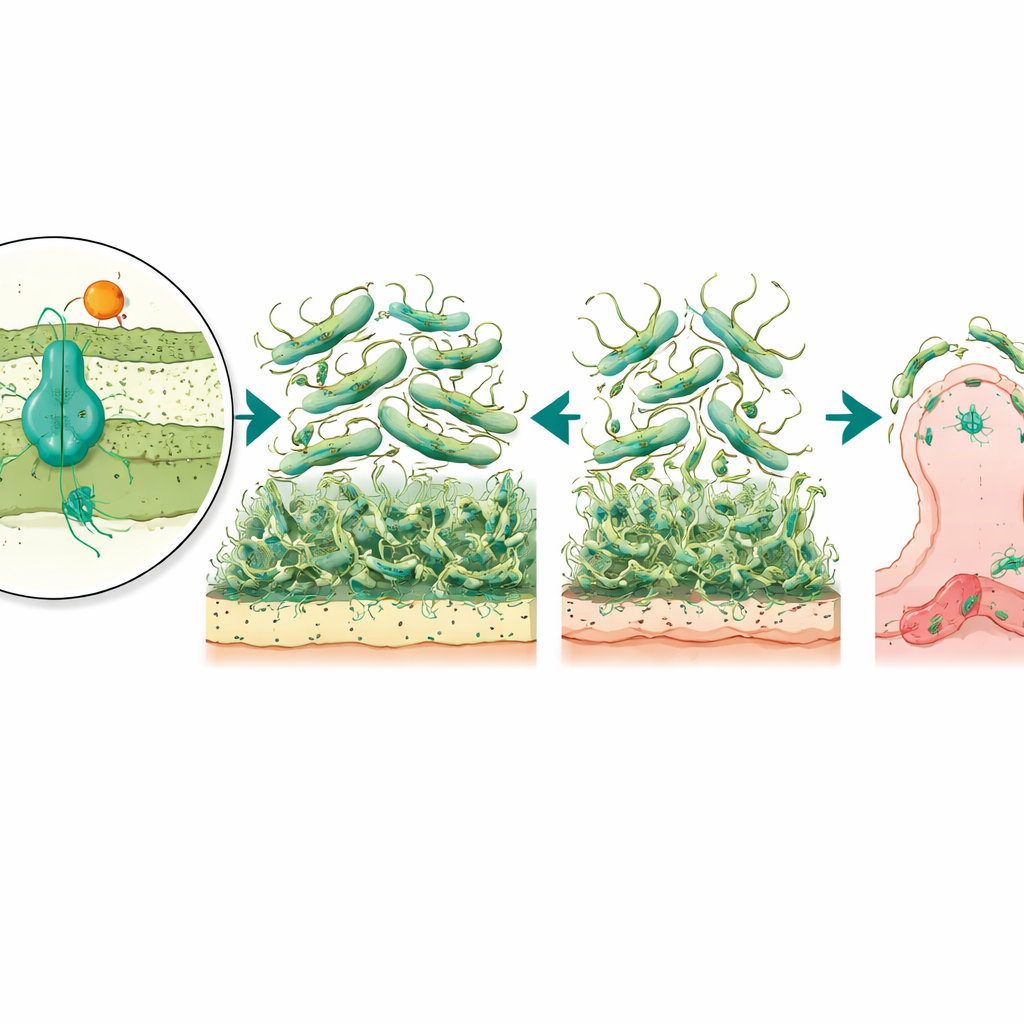
De gusanos de cera a la gravedad de la enfermedad
Para conectar estos hallazgos de laboratorio con la infección real, los científicos recurrieron a un modelo vivo: larvas de la polilla de la cera Galleria mellonella, un sustituto establecido para estudiar la virulencia bacteriana. Cuando se infectaron las larvas con la cepa normal de A. baumannii, muchas murieron, pero las infectadas con el mutante sin el regulador sobrevivieron a tasas mucho más altas. En contraste, eliminar solo la bomba no cambió la gravedad general de la enfermedad. Este patrón sugiere que AmvR, el regulador, desempeña un papel más amplio de coordinación en el control de rasgos como la motilidad, la formación de biopelículas y la adhesión celular que, en conjunto, determinan qué tan bien la bacteria puede invadir y persistir dentro de un huésped.
Qué significa esto para tratamientos futuros
En términos sencillos, este trabajo muestra que el sistema AmvAR en A. baumannii es más que una bomba química: ayuda a moldear el recubrimiento exterior del germen, su capacidad de moverse, de pegarse a superficies, de construir capas protectoras de mucosidad y, en última instancia, de causar enfermedad. Interrumpir únicamente la bomba puede no ser suficiente para controlar la infección, pero interferir con el regulador o las vías conectadas podría debilitar varias estrategias clave de supervivencia a la vez. Eso convierte a AmvAR, y a sistemas de control similares, en objetivos prometedores para nuevas estrategias destinadas tanto a superar la resistencia a antibióticos como a reducir la virulencia de este persistente patógeno hospitalario.
Cita: Gaona, M., Corral, J., Sánchez-Osuna, M. et al. Role of the AmvAR efflux system on the pathogenesis of Acinetobacter baumannii. Sci Rep 16, 10753 (2026). https://doi.org/10.1038/s41598-026-46007-w
Palabras clave: Acinetobacter baumannii, bombas de expulsión, biopelícula, resistencia a antimicrobianos, virulencia bacteriana