Clear Sky Science · it
Ruolo del sistema di efflusso AmvAR nella patogenesi di Acinetobacter baumannii
Perché questo germe ospedaliero è importante
Acinetobacter baumannii è un germe ospedaliero difficile da eliminare che può causare polmoniti, infezioni del sangue e gravi infezioni di ferite e delle vie urinarie, soprattutto nei pazienti molto malati. È noto per resistere a molti antibiotici e persino ad alcuni disinfettanti, rendendolo una preoccupazione principale nella lista delle minacce critiche dell’Organizzazione Mondiale della Sanità. Questo studio pone una domanda centrale: oltre ad aiutare il batterio a espellere sostanze tossiche, uno dei suoi sistemi di difesa lo rende anche più bravo ad aderire alle superfici, formare comunità viscide e causare malattia?
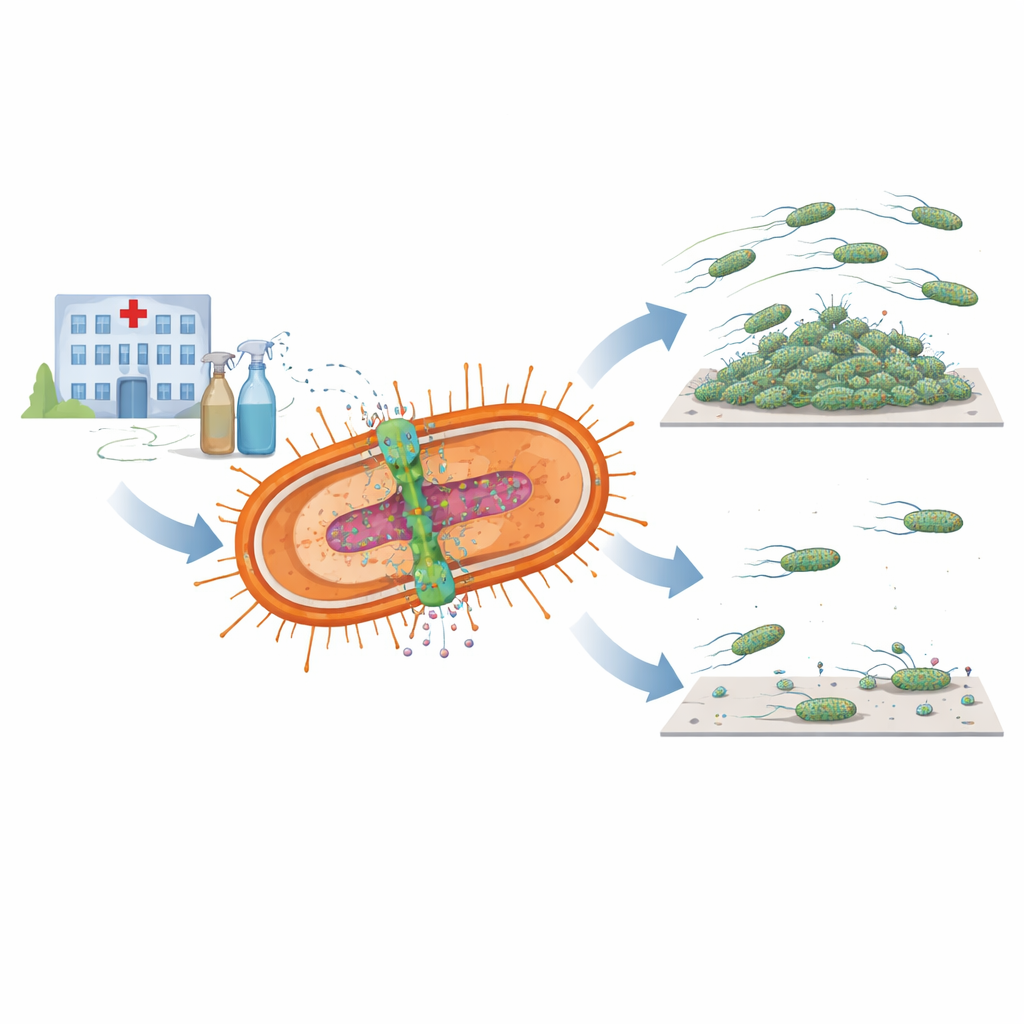
Un doppio strumento per la sopravvivenza
I ricercatori si sono concentrati su un coppia di componenti batteriche strettamente collegate, note insieme come sistema AmvAR. Una parte, AmvA, è inserita nella membrana cellulare e funziona come una pompa microscopica che spinge fuori dalla cellula disinfettanti e altre molecole dannose. L’altra parte, AmvR, agisce come un interruttore genetico on–off che normalmente mantiene la pompa sotto controllo. Scansionando centinaia di genomi batterici, il team ha trovato versioni di entrambe le componenti in quasi tutti i ceppi di A. baumannii disponibili, suggerendo che questo sistema sia centrale per la sopravvivenza del germe in condizioni ospedaliere avverse, inclusi i contatti frequenti con disinfettanti come la clorexidina.
Come la modifica di questo sistema altera movimento e muco
Per capire cosa fa AmvAR oltre alla resistenza ai farmaci, gli scienziati hanno creato ceppi mutanti privi della pompa o del suo regolatore e li hanno confrontati con il ceppo normale. Hanno osservato che la rimozione di AmvR, il regolatore, riduceva la capacità del batterio di diffondersi su una superficie morbida, mostrando una motilità compromessa. Entrambi i mutanti, privi della pompa o del regolatore, hanno formato biofilm molto più deboli: le comunità appiccicose e stratificate su plastica e vetro che aiutano i batteri ad aderire ai dispositivi medici e a resistere alla pulizia. Quando i ricercatori hanno reintrodotto i geni mancanti, hanno potuto ripristinare o addirittura aumentare la formazione del biofilm, suggerendo che il giusto equilibrio di questo sistema è cruciale per costruire comunità superficiali stabili.
Come il batterio si aggrappa alle cellule ospiti
Poiché i biofilm e le strutture superficiali aiutano i batteri ad ancorarsi ai tessuti umani, il team ha poi testato quanto bene i mutanti potessero attaccarsi a cellule della vescica coltivate in laboratorio, un modello per le infezioni delle vie urinarie. Entrambi i mutanti aderivano molto meno rispetto al ceppo normale, con la versione priva della pompa che mostrava la diminuzione maggiore nell’adesione. Ciò suggerisce che il sistema AmvAR non solo aiuta il batterio a resistere ai disinfettanti, ma modula anche la superficie esterna in modo da potersi attaccare alle nostre cellule. A sostegno di questa idea, il mutante del regolatore mostrava una marcata sovrapproduzione di una subunità pilina, un componente delle fibre simili a capelli che mediano l’adesione alla superficie. Paradossalmente, questa sovrapproduzione era collegata a biofilm e motilità peggiori, implicando che troppe fibre o fibre mal coordinate possono in realtà disturbare il comportamento superficiale normale.
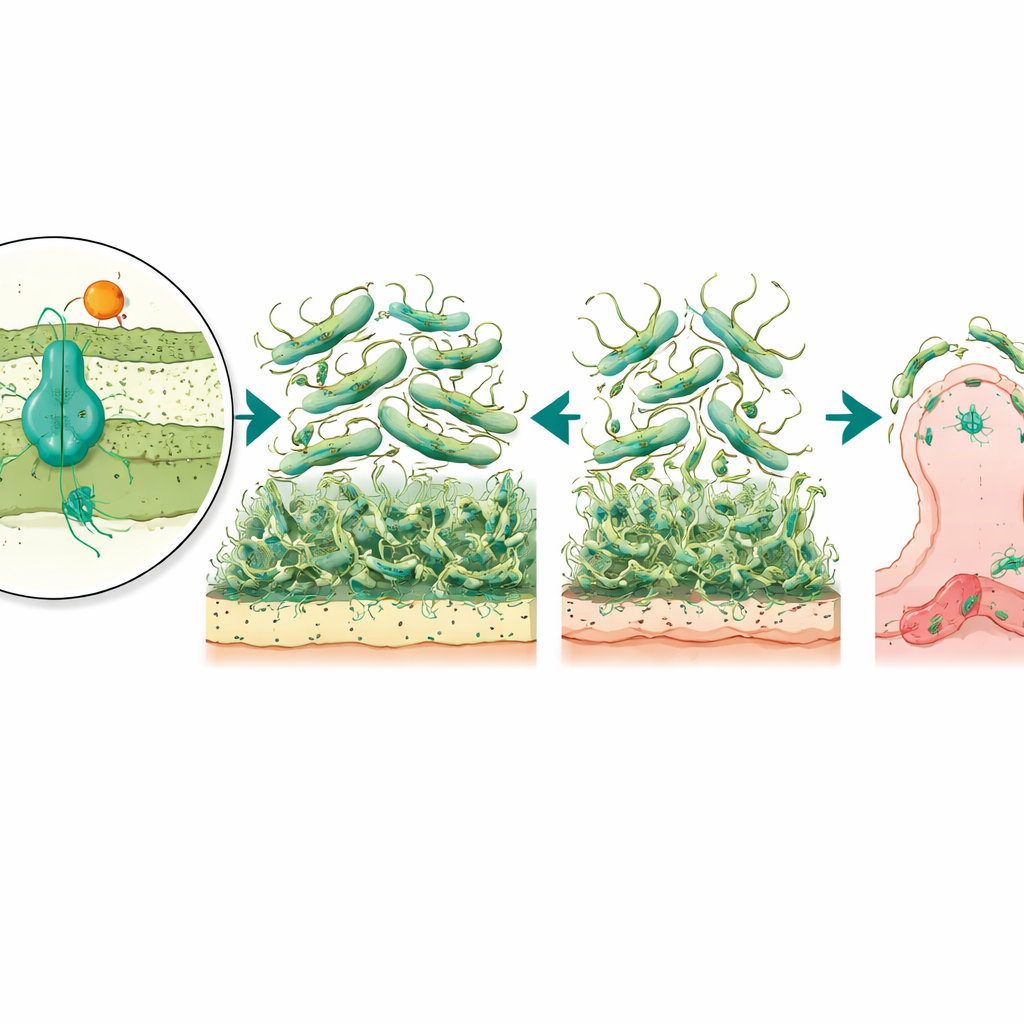
Dai bruchi ceratoidei alla gravità della malattia
Per collegare questi risultati di laboratorio all’infezione reale, gli scienziati hanno utilizzato un modello animale: le larve della falena della cera Galleria mellonella, un sostituto consolidato per lo studio della virulenza batterica. Quando sono state infettate con il ceppo normale di A. baumannii, molte larve sono morte, ma quelle infettate con il mutante privo del regolatore sono sopravvissute a tassi molto più alti. Al contrario, la rimozione solo della pompa non ha cambiato in modo significativo la gravità complessiva della malattia. Questo schema suggerisce che AmvR, il regolatore, svolge un ruolo di coordinamento più ampio nel controllare tratti come motilità, formazione di biofilm e adesione cellulare che insieme determinano quanto bene il batterio può invadere e persistere all’interno di un ospite.
Cosa significa per i trattamenti futuri
In termini semplici, questo lavoro mostra che il sistema AmvAR in A. baumannii è più di una pompa chimica: aiuta a plasmare il mantello esterno del germe, la sua capacità di muoversi, di incollarsi alle superfici, di costruire strati viscidi protettivi e, in ultima analisi, di causare malattia. Disattivare solo la pompa potrebbe non essere sufficiente per domare l’infezione, ma interferire con il regolatore o con le vie connesse potrebbe indebolire contemporaneamente diversi stratagemmi chiave di sopravvivenza. Questo rende AmvAR, e sistemi di controllo simili, obiettivi promettenti per nuove strategie mirate sia a superare la resistenza agli antibiotici sia ad attenuare la virulenza di questo ostinato patogeno ospedaliero.
Citazione: Gaona, M., Corral, J., Sánchez-Osuna, M. et al. Role of the AmvAR efflux system on the pathogenesis of Acinetobacter baumannii. Sci Rep 16, 10753 (2026). https://doi.org/10.1038/s41598-026-46007-w
Parole chiave: Acinetobacter baumannii, pompe di efflusso, biofilm, resistenza antimicrobica, virulenza batterica