Clear Sky Science · ja
Acinetobacter baumanniiの病原因性におけるAmvAR排出系の役割
なぜこの病院感染菌が問題なのか
Acinetobacter baumanniiは、特に重症患者に肺炎、血流感染、重篤な創傷感染や尿路感染を引き起こす、駆除が難しい病院内感染菌です。多くの抗生物質や一部の消毒薬にも耐えることで知られており、世界保健機関の重大な脅威リストに挙げられています。本研究は重要な問いを立てます:毒性物質を細胞外に排出する以外に、この防御システムの一つは表面への付着、粘性のある集団形成、そして病原因性を高める働きも持つのか?
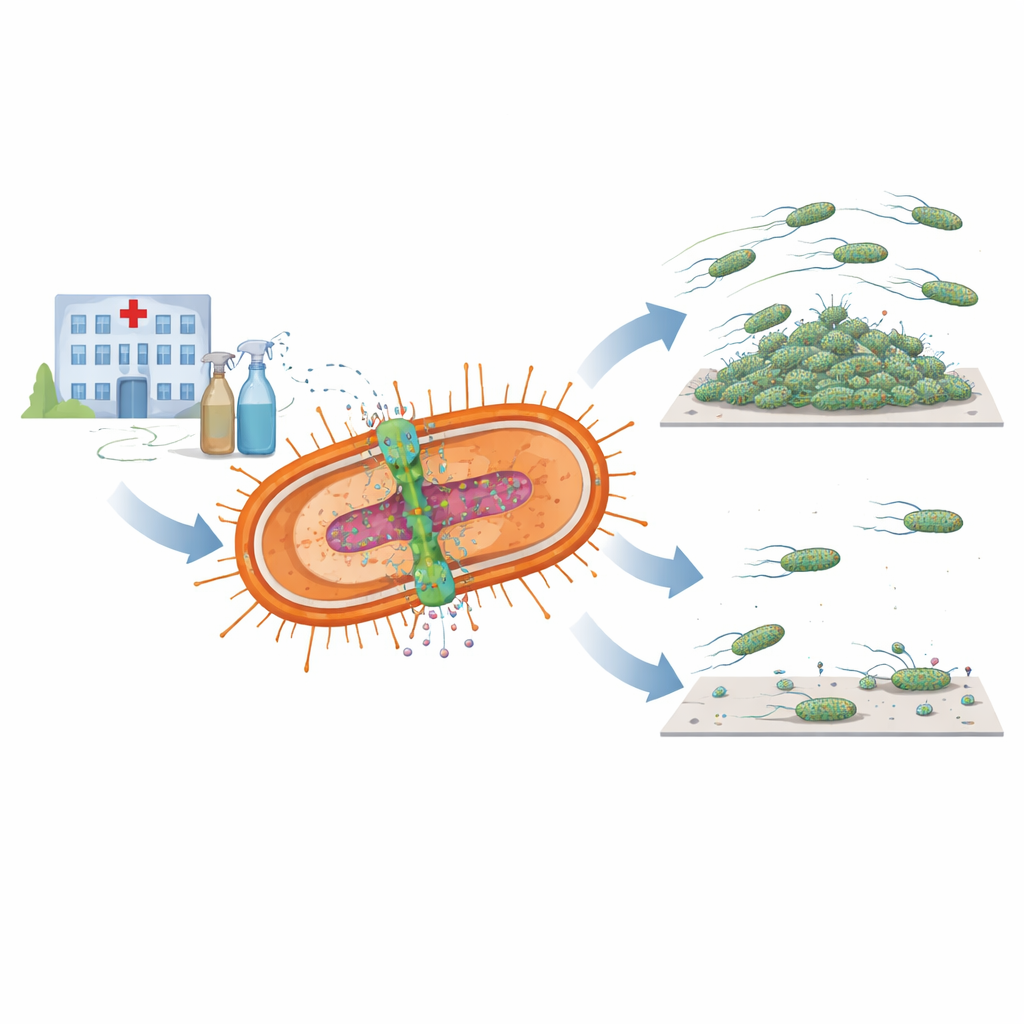
生存のための二重の道具
研究者らはAmvARとしてまとめられる、密接に連携する二つの細菌成分に注目しました。一方のAmvAは細胞膜に位置し、消毒薬やその他有害分子を細胞外へ押し出す微小なポンプの働きをします。もう一方のAmvRは遺伝子のオン・オフを制御する調節因子で、通常はポンプを抑制しています。何百もの細菌ゲノムをスキャンしたところ、ほぼ全ての入手可能なA. baumannii株に両方の構成要素のバージョンが見つかり、この系が塩素系消毒薬など頻繁に接触する病院の過酷な環境下で生存する上で中心的役割を果たしていることを示唆しました。
この系を変えると運動性と粘性がどう変わるか
AmvARが薬剤耐性以外に何をしているかを調べるため、研究者らはポンプかその調節因子のいずれかを欠く変異株を作製し、通常株と比較しました。調節因子AmvRを欠くと軟らかい表面上を広がる能力が低下し、運動性が損なわれることが観察されました。ポンプ欠損株と調節因子欠損株の両方は、医療機器に付着して洗浄に抵抗するプラスチックやガラス上の粘着的で層状の集団であるバイオフィルムを大幅に弱く形成しました。欠失した遺伝子を再導入するとバイオフィルム形成が回復あるいは増強されることから、この系の適切なバランスが安定した表面集団の構築に重要であることが示唆されます。
細菌が宿主細胞に取り付く仕組み
バイオフィルムや表面構造は細菌がヒト組織に取り付くのを助けるため、研究チームは次に変異株が培養した膀胱上皮細胞にどれほど付着できるかを調べました(尿路感染のモデルとして)。双方の変異株は通常株よりもはるかに付着率が低く、特にポンプ欠損株で付着の落ち込みが最も大きくなりました。これはAmvAR系が消毒薬への抵抗を助けるだけでなく、細菌の外膜構造を微調整して我々の細胞に取り付く能力を高めていることを示唆します。支持する証拠として、調節因子欠損株では細胞付着に関わる毛状繊維の構成要素であるピラスサブユニットが劇的に過剰生産されていました。逆説的に、この過剰生産はバイオフィルムや運動性の低下と結びつき、過剰または協調性を欠いた繊維が正常な表面挙動を乱す可能性を示しています。
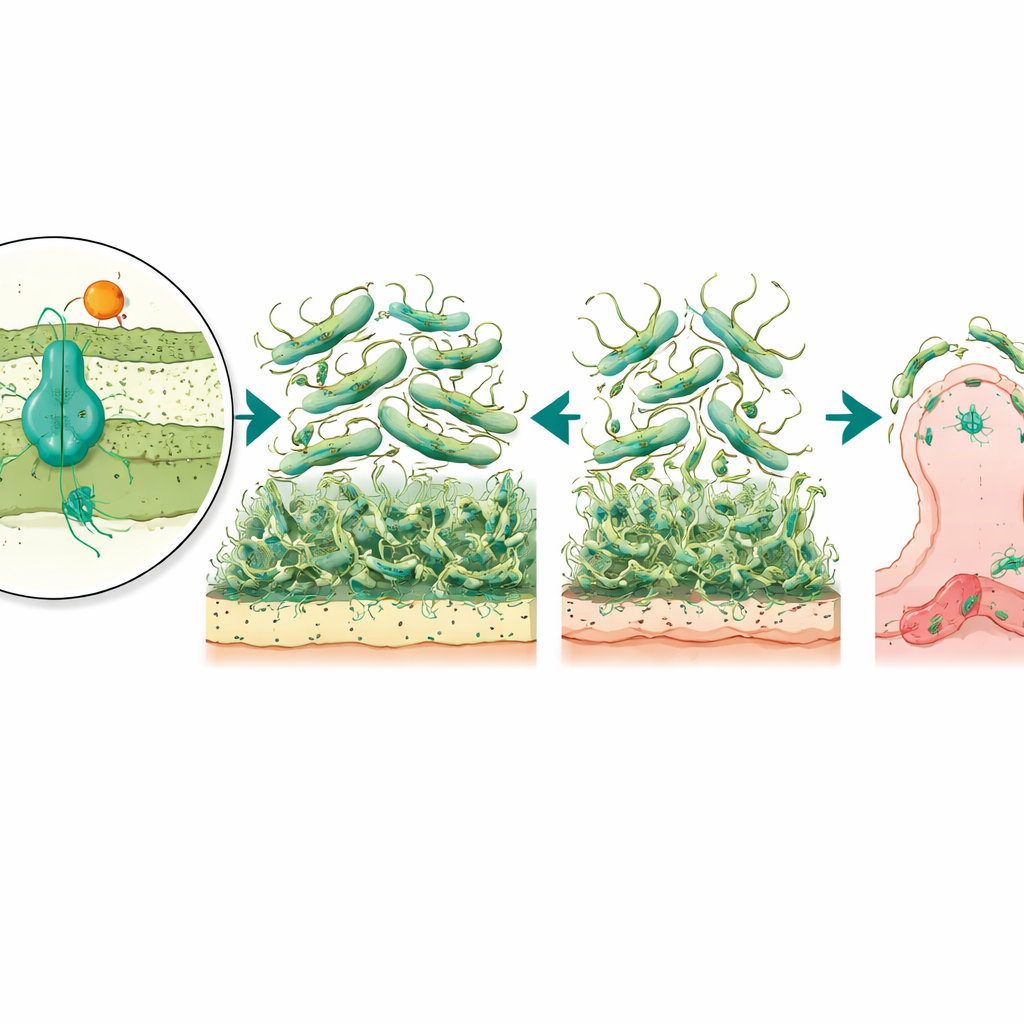
ワックスワームから病気の重症度へ
これらの試験管内の知見を実際の感染と結びつけるため、研究者らは生体モデルとしてワックス蛾(Galleria mellonella)の幼虫を用いました。これは細菌の病原性を研究する確立された代替モデルです。通常株で感染させると多くの幼虫が死亡しましたが、調節因子欠損株で感染させた幼虫ははるかに高い生存率を示しました。一方、ポンプだけを欠く場合は全体的な病気の重症度に変化が見られませんでした。このパターンは、AmvRが運動、バイオフィルム形成、細胞付着などの性質を広く調整する役割を果たし、それらが合わさって宿主内での侵入や持続能を決定していることを示唆します。
今後の治療への示唆
簡潔に言えば、本研究はA. baumanniiのAmvAR系が単なる化学物質排出のポンプ以上の役割を持ち、外膜の造形、運動性、表面への付着、保護的な粘性層の形成、ひいては病原因性の発揮に寄与することを示しています。ポンプだけを標的にしても感染制御には不十分な場合があり得ますが、調節因子やそれに関連する経路を妨げれば複数の重要な生存戦略を同時に弱められる可能性があります。したがって、AmvARや類似の制御システムは、抗生物質耐性を克服し、この頑強な病院病原体の病原性を低下させる新たな戦略の有望な標的となります。
引用: Gaona, M., Corral, J., Sánchez-Osuna, M. et al. Role of the AmvAR efflux system on the pathogenesis of Acinetobacter baumannii. Sci Rep 16, 10753 (2026). https://doi.org/10.1038/s41598-026-46007-w
キーワード: Acinetobacter baumannii, 排出ポンプ, バイオフィルム, 抗菌薬耐性, 細菌の病原性