Clear Sky Science · nl
Rol van het AmvAR-effluxsysteem bij de pathogenese van Acinetobacter baumannii
Waarom deze ziekenhuisbacterie ertoe doet
Acinetobacter baumannii is een moeilijk te bestrijden ziekenhuisbacterie die longontsteking, bloedinfecties en ernstige wond- en urineweginfecties kan veroorzaken, vooral bij ernstig zieke patiënten. De bacterie staat bekend om het weerstaan van veel antibiotica en zelfs sommige ontsmettingsmiddelen, waardoor ze op de lijst van kritieke bedreigingen van de Wereldgezondheidsorganisatie staat. Deze studie onderzoekt een belangrijke vraag: behalve het pompen van toxische stoffen naar buiten, maakt één van zijn verdedigingssystemen de bacterie ook beter in het hechten aan oppervlakken, het vormen van slijmachtige gemeenschappen en het veroorzaken van ziekte?
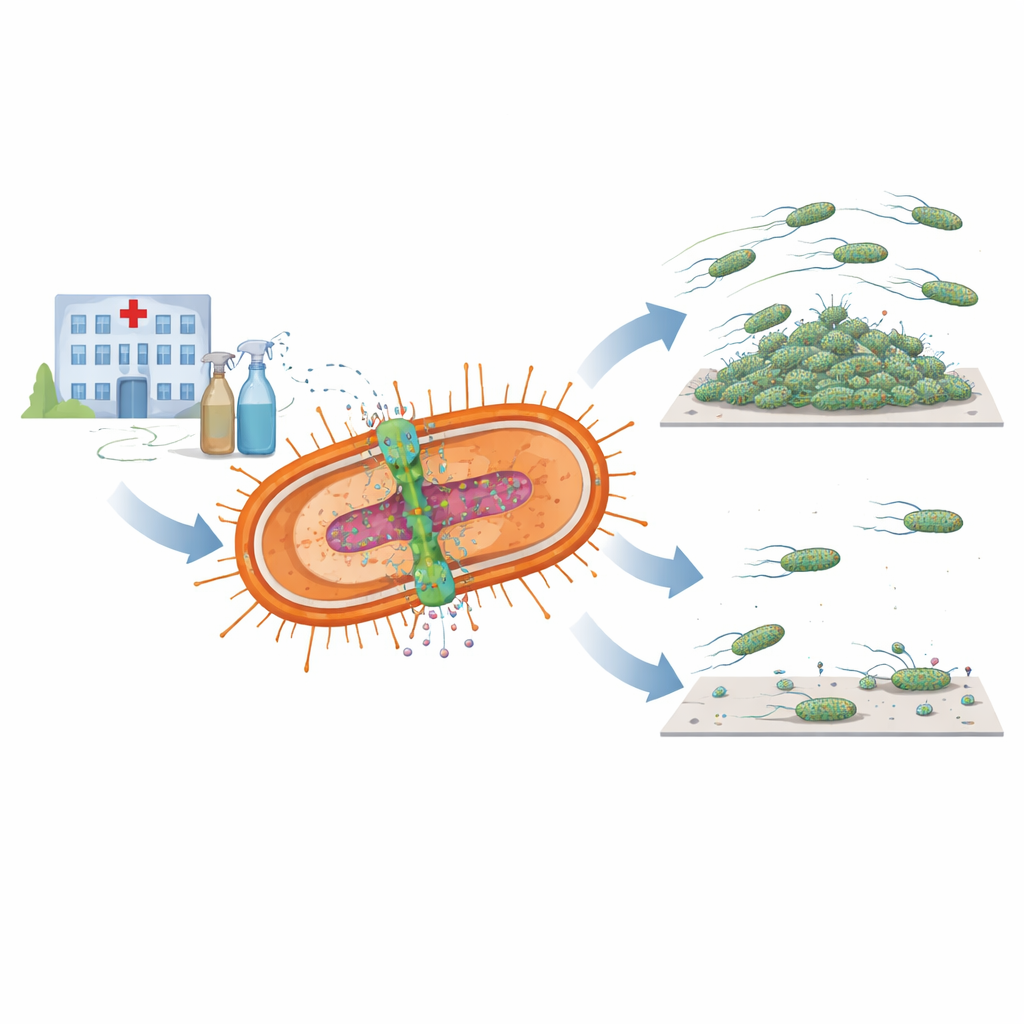
Een dubbel instrument voor overleving
De onderzoekers richtten zich op een paar nauw verbonden bacteriële componenten die samen bekendstaan als het AmvAR-systeem. Het ene deel, AmvA, bevindt zich in het celmembraan en werkt als een microscopische pomp die ontsmettingsmiddelen en andere schadelijke moleculen uit de cel duwt. Het andere deel, AmvR, fungeert als een genetische aan/uit-schakelaar die de pomp normaal gesproken onder controle houdt. Door honderden bacteriële genomen te doorzoeken, vonden de onderzoekers versies van beide onderdelen in bijna alle beschikbare A. baumannii-stammen, wat erop wijst dat dit systeem centraal staat in hoe de bacterie harde omstandigheden in ziekenhuizen overleeft, inclusief veelvuldig contact met ontsmettingsmiddelen zoals chloorhexidine.
Hoe verandering van dit systeem beweging en slijm beïnvloedt
Om te begrijpen wat AmvAR doet naast medicijnresistentie, maakten de wetenschappers mutanten zonder óf de pomp óf de regulator en vergeleken die met de normale stam. Ze zagen dat het wegnemen van AmvR, de regulator, de bacterie minder goed maakte in het zich verspreiden over een zacht oppervlak, met verminderde motiliteit als gevolg. Beide mutanten, zowel die zonder de pomp als die zonder de regulator, vormden veel zwakkere biofilms: de kleverige, gelaagde gemeenschappen op plastic en glas die bacteriën helpen zich aan medische hulpmiddelen te hechten en reinigen te weerstaan. Toen de onderzoekers de ontbrekende genen opnieuw introduceerden, konden ze de biofilmvorming herstellen of zelfs versterken, wat suggereert dat de juiste balans van dit systeem cruciaal is voor het opbouwen van stabiele oppervlaktengemeenschappen.
Hoe de bacterie zich aan gastheercellen vasthecht
Aangezien biofilms en oppervlakte-eigenschappen bacteriën helpen zich aan menselijk weefsel te hechten, testte het team vervolgens hoe goed de mutanten zich konden hechten aan in het laboratorium gekweekte blaascellen, een model voor urineweginfecties. Beide mutanten hechten veel minder effectief dan de normale stam, waarbij de variant zonder pomp de grootste afname in hechting liet zien. Dit suggereert dat het AmvAR-systeem de bacterie niet alleen helpt ontsmettingsmiddelen te weerstaan, maar ook het buitenoppervlak zodanig fijnstelt dat het zich aan onze cellen kan vastklampen. Ter ondersteuning van dit idee toonde de regulator-mutant een dramatische overproductie van een pilus-subunit, een bouwsteen van haarachtige vezels die oppervlaktehechting mediëren. Paradoxaal genoeg was deze overproductie gekoppeld aan slechtere biofilms en verminderde beweging, wat impliceert dat te veel of slecht gecoördineerde vezels het normale oppervlaktegedrag kunnen verstoren.
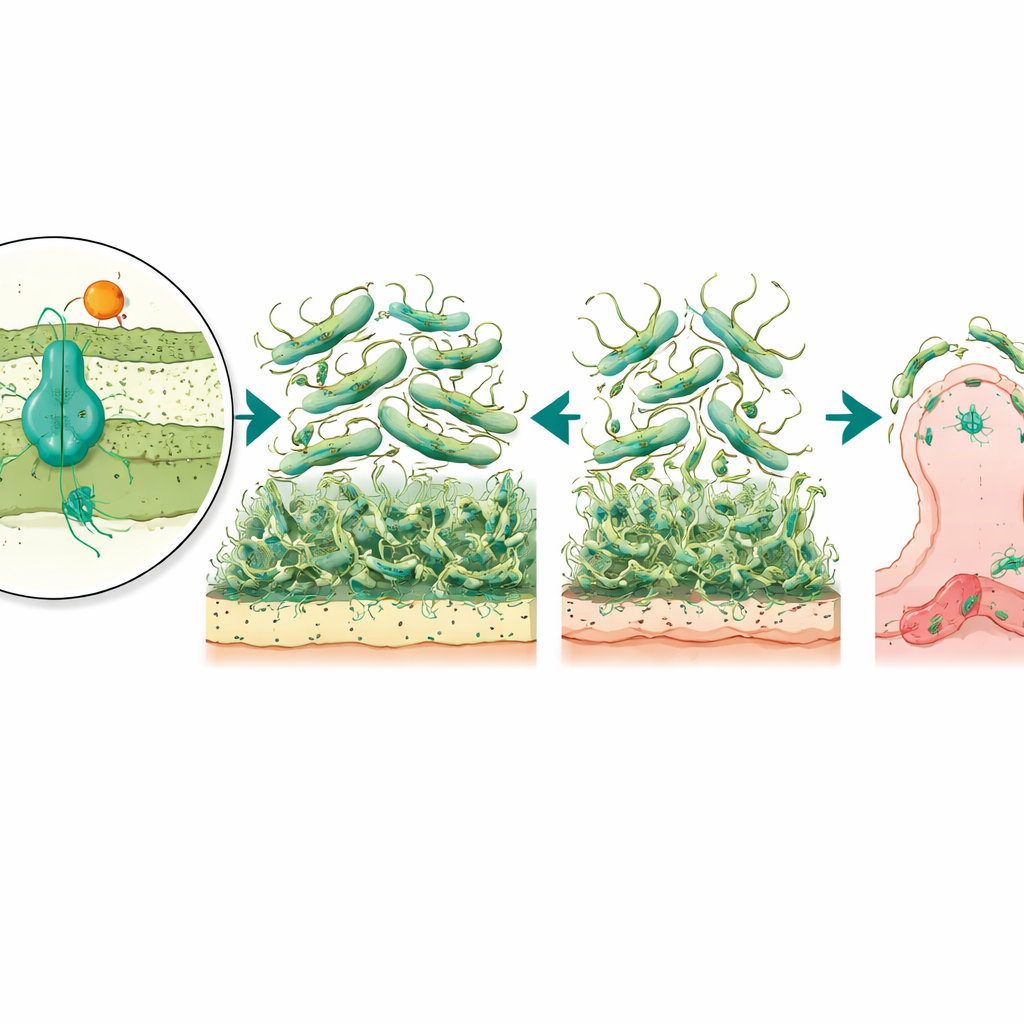
Van wasmotlarven tot ziekteernst
Om deze laboratoriumbevindingen aan echte infecties te koppelen, gebruikten de onderzoekers een levend model: larven van de wasmot Galleria mellonella, een erkend model om bacteriële virulentie te bestuderen. Toen zij werden geïnfecteerd met de normale A. baumannii-stam, stierven veel larven, maar die geïnfecteerd met de regulatorloze mutant overleefden in veel hogere mate. Het verwijderen van alleen de pomp veranderde de algemene ziekteernst daarentegen niet. Dit patroon suggereert dat AmvR, de regulator, een bredere coördinerende rol speelt in het regelen van eigenschappen zoals beweging, biofilmvorming en celhechting die samen bepalen hoe goed de bacterie een gastheer kan binnendringen en blijven voortbestaan.
Wat dit betekent voor toekomstige behandelingen
In eenvoudige termen laat dit werk zien dat het AmvAR-systeem in A. baumannii meer is dan een chemische pomp: het helpt de buitenlaag van de bacterie te vormen, beïnvloedt de beweging, het vermogen zich aan oppervlakken vast te kleven, het bouwen van beschermende slijmlaagjes en uiteindelijk het veroorzaken van ziekte. Alleen de pomp uitschakelen is mogelijk niet voldoende om een infectie te temmen, maar het verstoren van de regulator of de daaraan gekoppelde routes zou tegelijk meerdere belangrijke overlevingstrucs kunnen verzwakken. Dat maakt AmvAR en vergelijkbare controlesystemen veelbelovende doelen voor nieuwe strategieën die zowel antibioticaresistentie willen overwinnen als de virulentie van deze hardnekkige ziekenhuispathogeen willen verminderen.
Bronvermelding: Gaona, M., Corral, J., Sánchez-Osuna, M. et al. Role of the AmvAR efflux system on the pathogenesis of Acinetobacter baumannii. Sci Rep 16, 10753 (2026). https://doi.org/10.1038/s41598-026-46007-w
Trefwoorden: Acinetobacter baumannii, effluxpompen, biofilm, antimicrobiële resistentie, bacteriële virulentie