Clear Sky Science · ru
Роль системы выведения AmvAR в патогенезе Acinetobacter baumannii
Почему этот госпитальный микроб важен
Acinetobacter baumannii — трудно устраняемый госпитальный микроорганизм, который может вызывать пневмонию, бактериемию и тяжёлые инфекции ран и мочевыводящих путей, особенно у тяжело больных пациентов. Он известен своей способностью противостоять многим антибиотикам и даже некоторым дезинфицирующим средствам, что делает его важной угрозой в списке Всемирной организации здравоохранения. В этом исследовании поставлен ключевой вопрос: кроме выведения токсичных веществ, делает ли одна из его защитных систем бактерию более способной цепляться за поверхности, формировать слизистые сообщества и вызывать болезнь?
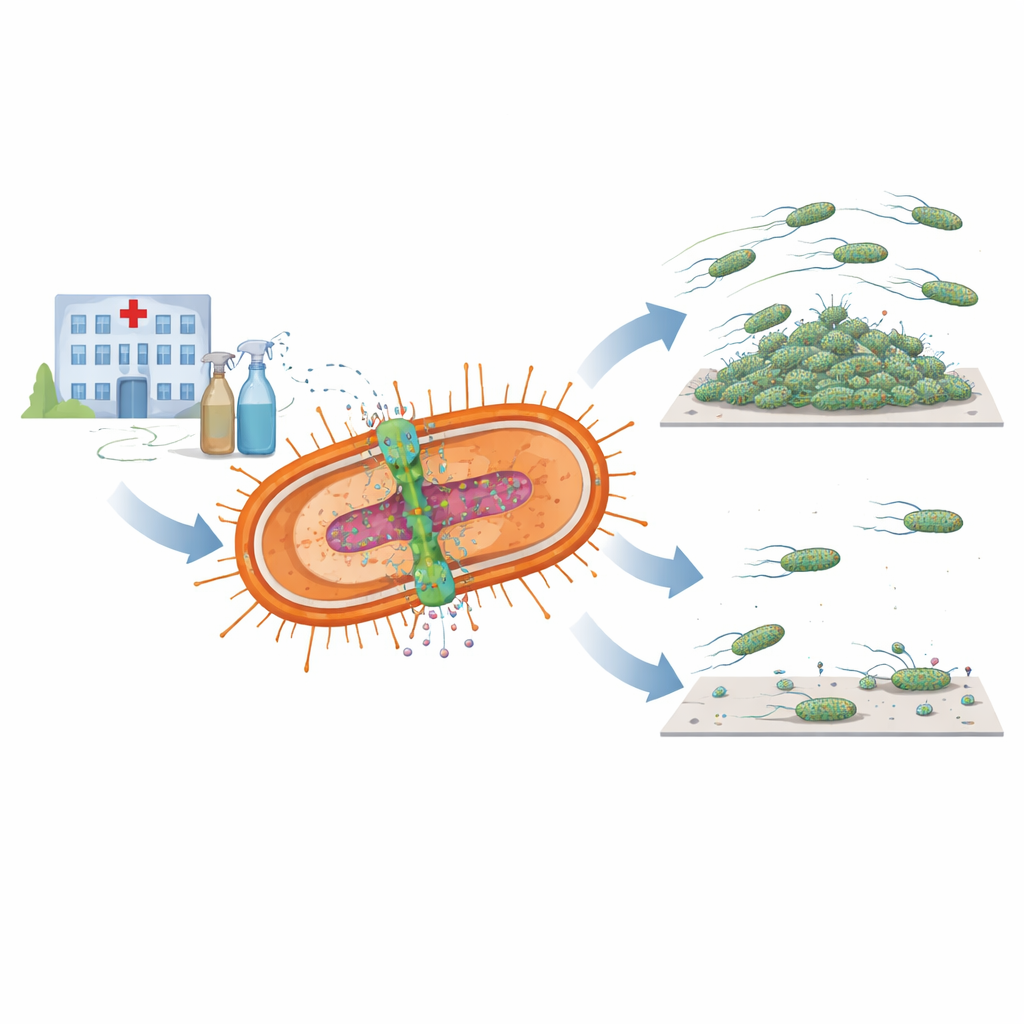
Двойной инструмент для выживания
Исследователи сосредоточились на паре тесно связанных бактериальных компонентов, известных как система AmvAR. Одна часть, AmvA, расположена в клеточной мембране и работает как микроскопический насос, выталкивающий дезинфектанты и другие вредные молекулы из клетки. Другая часть, AmvR, действует как генетический выключатель, который обычно сдерживает работу насоса. Сканируя сотни бактериальных геномов, команда обнаружила версии обеих составляющих почти во всех доступных штаммах A. baumannii, что указывает на то, что эта система важна для выживания микроба в суровых условиях больниц, включая частые контакты с дезинфектантами, такими как хлоргексидин.
Как изменение этой системы влияет на движение и слизь
Чтобы понять, что делает AmvAR помимо устойчивости к препаратам, учёные создали мутантные бактерии, лишённые либо насоса, либо его регулятора, и сравнили их с нормальным штамлем. Они обнаружили, что удаление AmvR, регулятора, снижало способность бактерий расползаться по мягкой поверхности — наблюдалась нарушенная подвижность. Оба мутанта, лишённые либо насоса, либо регулятора, формировали заметно более слабые биоплёнки — липкие, слоистые сообщества на пластике и стекле, которые помогают бактериям прикрепляться к медицинским устройствам и сопротивляться очистке. Когда исследователи возвращали недостающие гены, они могли восстановить или даже усилить формирование биоплёнок, что указывает на то, что правильный баланс этой системы критически важен для построения стабильных поверхностных сообществ.
Как бактерия хватается за клетки хозяина
Поскольку биоплёнки и поверхностные структуры помогают бактериям захватывать ткани человека, команда далее протестировала, насколько хорошо мутанты прикрепляются к культивируемым в лаборатории клеткам мочевого пузыря, модели инфекций мочевыводящих путей. Оба мутанта прикреплялись значительно хуже, чем нормальный штамм, при этом вариант без насоса показал наибольшее снижение адгезии. Это предполагает, что система AmvAR не только помогает бактерии противостоять дезинфектантам, но и тонко настраивает её наружную поверхность, чтобы она могла сцепляться с нашими клетками. В подтверждение этой идеи регуляторный мутант показал драматическое сверхпроизводство субъединицы пилюс — строительного блока волосковидных фибрилл, обеспечивающих прикрепление к поверхностям. Парадоксально, что это перепроизводство связывали с худшими биоплёнками и подвижностью, что означает: слишком много или плохо скоординированные фибриллы могут нарушать нормальное поведение на поверхностях.
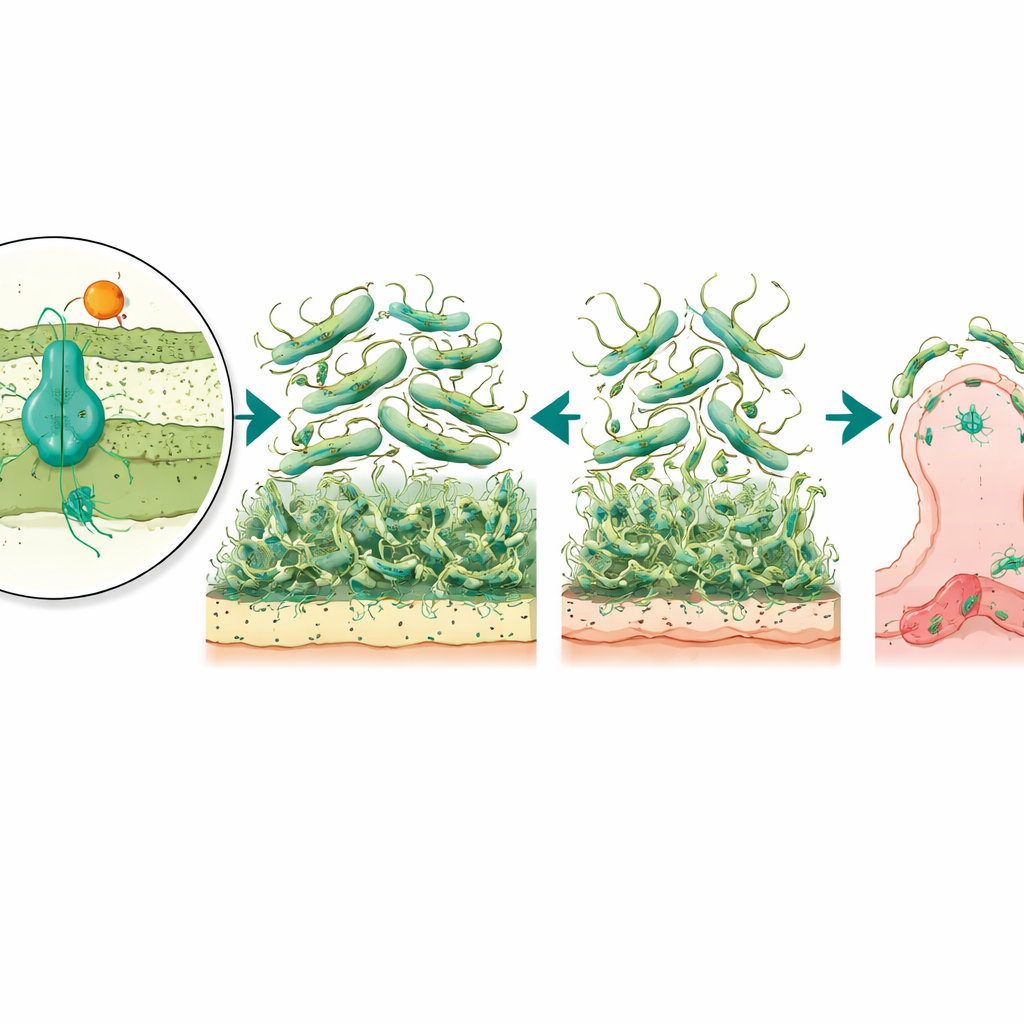
От восковых гусениц до тяжести болезни
Чтобы связать лабораторные наблюдения с реальной инфекцией, учёные обратились к живой модели: личинкам восковой моли Galleria mellonella, признанной модели для изучения вирулентности бактерий. При инфекции нормальным штаммом A. baumannii многие личинки погибали, тогда как инфицированные мутантом без регулятора выживали в гораздо большей степени. Напротив, удаление только насоса не меняло общую тяжесть заболевания. Эта картина указывает на то, что AmvR, регулятор, выполняет более широкую координирующую роль в контроле таких признаков, как подвижность, формирование биоплёнок и прикрепление к клеткам, которые вместе определяют способность бактерии проникать и удерживаться в организме хозяина.
Что это значит для будущих методов лечения
Проще говоря, эта работа показывает, что система AmvAR у A. baumannii — это не просто химический насос: она формирует наружный покров микроба, его способность двигаться, приклеиваться к поверхностям, строить защитные слизистые слои и в конечном счёте вызывать болезнь. Нарушение работы только насоса может быть недостаточно, чтобы укротить инфекцию, но вмешательство в работу регулятора или связанных с ним путей может ослабить сразу несколько ключевых приёмов выживания. Это делает AmvAR и подобные управляющие системы многообещающими мишенями для новых стратегий, направленных одновременно на преодоление антибиотикорезистентности и снижение вирулентности этого упрямого госпитального патогена.
Цитирование: Gaona, M., Corral, J., Sánchez-Osuna, M. et al. Role of the AmvAR efflux system on the pathogenesis of Acinetobacter baumannii. Sci Rep 16, 10753 (2026). https://doi.org/10.1038/s41598-026-46007-w
Ключевые слова: Acinetobacter baumannii, насосы выведения, биопленка, антимикробная резистентность, бактериальная вирулентность