Clear Sky Science · sv
Cilostazol minskar amiodaroninducerad lungtoxicitet och fibros genom att reglera cAMP/TGF-β1‑vägen medierad epitelialt till mesenkymalt övergång hos råttor
Varför denna lungstudie är viktig
Lungfibros är en långsam ärrbildande skada på lungorna som gör varje andetag svårare, och den kan utlösas av vissa livräddande hjärtmediciner. Denna studie på råttor undersöker om ett befintligt läkemedel, cilostazol, kan skydda lungorna mot skador orsakade av den ofta använda antiarytmiska substansen amiodaron. Genom att följa både synliga lungskador och de dolda kemiska signalerna inne i lungcellerna ställer forskarna en hoppfull fråga: kan vi behålla viktiga hjärtbehandlingar samtidigt som vi bättre skyddar lungorna?
En hjärtmedicin med en dold kostnad
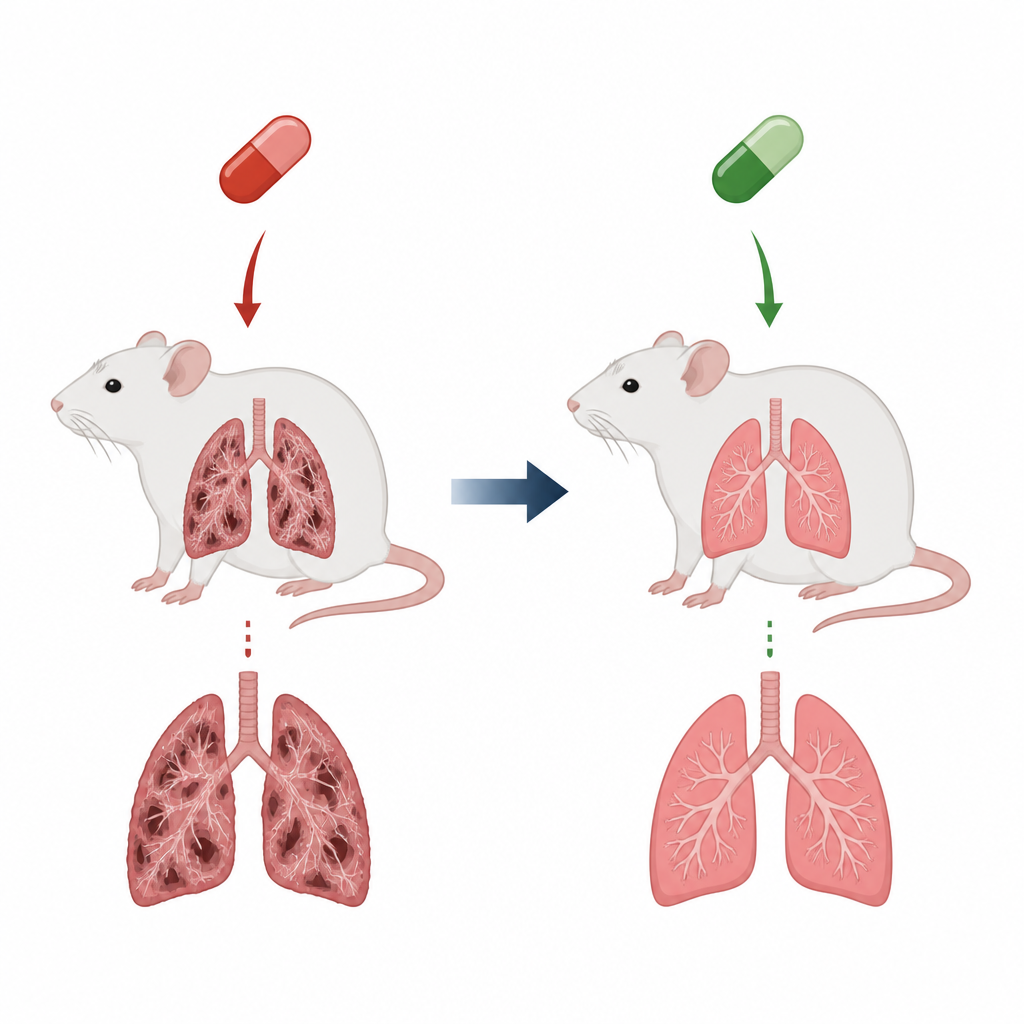
Amiodaron ordineras för att korrigera farliga hjärtrytmrubbningar, men en allvarlig nackdel är dess potential att skada lungvävnad och leda till lungfibros. Vid fibros blir de känsliga luftblåsorna som utbyter syre stela och ärriga, vilket gör andningen tung och förkortar livslängden. I den här råttmodellen återproducerade dagliga amiodarondoser under flera veckor många drag av detta tillstånd: tyngre lungor, inflammerade luftvägar fyllda med immunceller, och tjocka kollagena band som förvrängde normal lungstruktur. Dessa förändringar speglar vad kliniker fruktar hos patienter som utvecklar läkemedelsrelaterad ärrbildning i lungorna.
Test av ett skyddande tilläggsläkemedel
Cilostazol är en tablett som redan används för att förbättra blodflödet i tilltäppta benartärer och för att minska risken för vissa typer av stroke. Den verkar delvis genom att höja nivåerna av ett litet signalsubstans kallat cAMP, vilket kan dämpa inflammation och begränsa ärrbildning i vävnader. Forskarna delade in råttorna i tre grupper: friska kontroller, djur som fick enbart amiodaron, och djur som fick cilostazol före varje amiodarondos. De samlade sedan vätska från lungorna, granskade vävnadssnitt i mikroskop och mätte kemiska markörer för oxidation, inflammation och ärrbildning för att se om cilostazol kunde dämpa lungskaden.
Vad som hände inne i de skadade lungorna
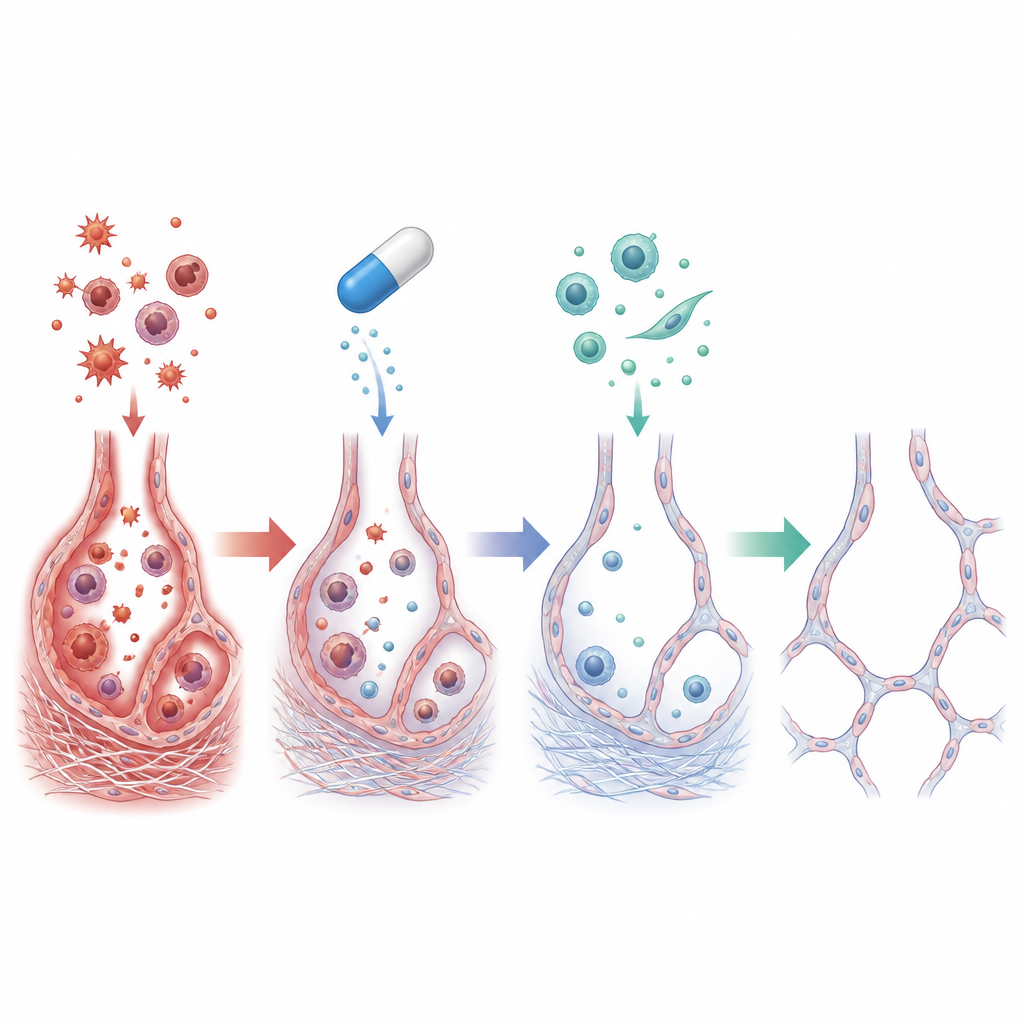
Hos råttor som enbart fått amiodaron visade lungorna intensiv inflammation: antalet immunceller i luftvätskan ökade kraftigt, och nivåerna av inflammatoriska budbärare som TNF‑alpha och IL‑1 beta steg flera gånger om. Kemiska spår av oxidativ stress ökade, med mer lipidskador och uttömda antioxidantförsvar. I mikroskopet såg teamet kollapsade och förvrängda luftblåsor omgivna av tunga kollageninlagringar. Djupare inne i cellerna fanns tecken på att epitelcellerna som bekläder luftblåsorna började bete sig mer som ärrbildande celler, en förskjutning känd som epitelialt till mesenkymalt övergång som driver bestående fibros.
Hur cilostazol förändrade bilden
När cilostazol lades till reducerades många av dessa skadliga förändringar markant. Lungorna från behandlade råttor vägde mindre och såg mycket mer normala ut, med betydligt mindre kollagenuppbyggnad och bättre bevarade luftblåsor. Inflammatoriska celler och cytokiner sjönk mot kontrollnivåer, och markörer för oxidativ skada minskade medan naturliga antioxidanter återhämtade sig. På molekylär nivå ökade cilostazol cAMP och ökade aktiviteten hos skyddande faktorer såsom SIRT1 och EPAC1, samtidigt som signaler kopplade till ärrbildning, inklusive TGF‑beta1 och vimentin, dämpades. Tillsammans tyder dessa förändringar på att cilostazol inte bara tystade inflammation och oxidativ stress utan också avbröt den cellulära omskrivning som förvandlar friska beklädnadsceller till ärrproducerande celler.
Från råttlunga till framtida behandlingsidéer
Studien drar slutsatsen att cilostazol markant kan mildra amiodaroninducerad lungskada och ärrbildning hos råttor genom att återställa en hälsosammare balans av cellsignaler och blockera nyckelsteg som leder till permanent fibros. Även om dessa fynd ännu inte visar hur cilostazol kommer att fungera hos människor, pekar de på en praktisk strategi: att återanvända ett godkänt läkemedel för att skydda lungorna hos patienter som är beroende av kraftfulla hjärtmediciner. Ytterligare arbete i andra modeller och så småningom kliniska prövningar kommer att krävas, men resultaten skickar ett tydligt budskap till icke‑specialister: en del av den skada som orsakas av nödvändiga läkemedel kan kanske förebyggas genom att kombinera dem med noggrant utvalda följeslagare.
Citering: El-Gammal, M.A., Yousef, E.H., Abd Elhameed, A.G. et al. Cilostazol mitigates amiodarone-induced pulmonary toxicity and fibrosis by regulating the cAMP/TGF-β1 pathway-mediated epithelial-to-mesenchymal transition in rats. Sci Rep 16, 15055 (2026). https://doi.org/10.1038/s41598-026-45341-3
Nyckelord: lungfibros, amiodaron‑lungtoxicitet, cilostazol, Läkemedelsinducerad lungsjukdom, cAMP‑signalering