Clear Sky Science · es
Cilostazol atenúa la toxicidad pulmonar y la fibrosis inducidas por amiodarona regulando la transición epitelio-mesénquima mediada por la vía cAMP/TGF-β1 en ratas
Por qué importa este estudio pulmonar
La fibrosis pulmonar es una lesión progresiva y cicatricial en los pulmones que hace que cada respiración sea más difícil, y puede ser desencadenada por algunos fármacos cardiacos que salvan vidas. Este estudio en ratas investiga si un medicamento ya existente, el cilostazol, puede proteger los pulmones frente al daño causado por el ampliamente usado antiarrítmico amiodarona. Al seguir tanto la lesión visible en el pulmón como las señales químicas ocultas dentro de las células pulmonares, los investigadores plantean una pregunta esperanzadora: ¿podemos mantener tratamientos cardiacos vitales a la vez que protegemos mejor los pulmones?
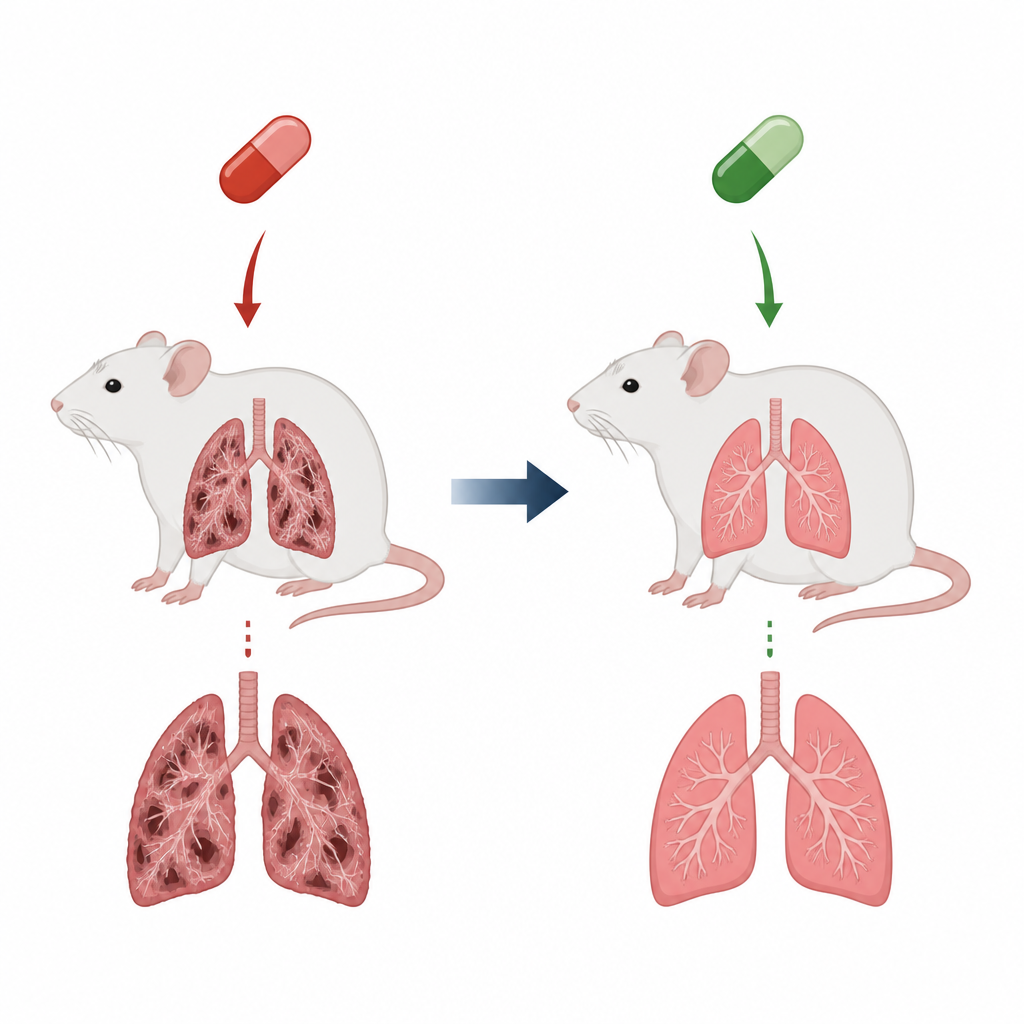
Un fármaco cardiaco con un coste oculto
La amiodarona se prescribe para corregir arritmias cardiacas peligrosas, pero una desventaja grave es su potencial para dañar el tejido pulmonar y provocar fibrosis pulmonar. En la fibrosis, los delicados sacos de aire que intercambian oxígeno se vuelven rígidos y cicatrizados, haciendo la respiración penosa y acortando la expectativa de vida. En este modelo de rata, dosis diarias de amiodarona durante varias semanas reprodujeron muchas características de esta condición: pulmones más pesados, vías respiratorias inflamadas llenas de células inmunitarias y gruesos depósitos de colágeno que deformaron la estructura pulmonar normal. Estos cambios reflejan lo que los clínicos temen en pacientes que desarrollan cicatrización pulmonar relacionada con fármacos.
Probando un fármaco compañero protector
El cilostazol es una pastilla ya usada para mejorar el flujo sanguíneo en arterias obstruidas de las piernas y para reducir el riesgo de ciertos tipos de ictus. Funciona en parte elevando los niveles de una pequeña molécula mensajera llamada cAMP, que puede calmar la inflamación y limitar la cicatrización en los tejidos. Los investigadores dividieron a las ratas en tres grupos: controles sanos, animales que recibieron solo amiodarona y animales tratados con cilostazol antes de cada dosis de amiodarona. Luego recogieron líquido de los pulmones, examinaron cortes de tejido al microscopio y midieron marcadores químicos de oxidación, inflamación y cicatrización para ver si el cilostazol podía atenuar el daño pulmonar.
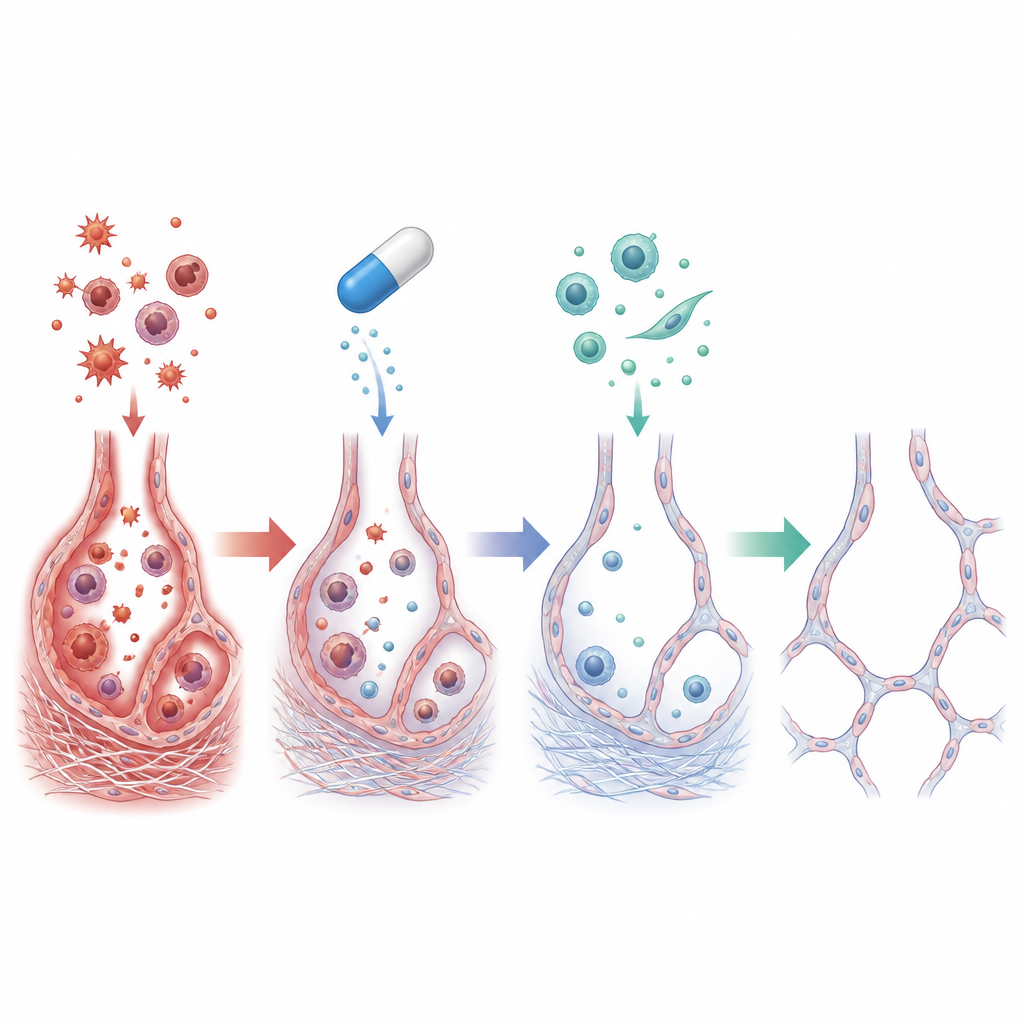
Qué sucedió dentro de los pulmones lesionados
En las ratas que recibieron solo amiodarona, los pulmones mostraron una intensa inflamación: el recuento de células inmunitarias en el líquido de las vías respiratorias se disparó y los niveles de mensajeros inflamatorios como TNF-alfa e IL-1 beta aumentaron varias veces. Los signos químicos de estrés oxidativo se incrementaron, con más daño lipídico y defensas antioxidantes agotadas. Al microscopio, el equipo observó sacos de aire colapsados y distorsionados rodeados por depósitos abundantes de colágeno. Más profundamente en las células, hubo indicios de que las células epiteliales que revisten los sacos de aire empezaban a comportarse más como células formadoras de cicatriz, un cambio conocido como transición epitelio-mesénquima que impulsa la fibrosis duradera.
Cómo cambió el panorama con cilostazol
Cuando se añadió cilostazol, muchos de estos cambios perjudiciales se redujeron drásticamente. Los pulmones de las ratas tratadas pesaban menos y se parecían mucho más a los normales, con una acumulación de colágeno mucho más leve y sacos de aire mejor conservados. Las células inflamatorias y las citoquinas descendieron hacia niveles de control, y los marcadores de daño oxidativo disminuyeron mientras que los antioxidantes naturales se recuperaron. A nivel molecular, el cilostazol aumentó el cAMP y elevó la actividad de actores protectores como SIRT1 y EPAC1, a la vez que redujo las señales vinculadas a la cicatrización, incluyendo TGF-beta1 y vimentina. En conjunto, estos cambios sugieren que el cilostazol no solo calmó la inflamación y el estrés oxidativo, sino que también interrumpió la reprogramación celular que convierte células del revestimiento sanas en productoras de cicatriz.
De los pulmones de rata a ideas para futuros tratamientos
El estudio concluye que el cilostazol puede atenuar de forma notable la lesión pulmonar y la cicatrización inducidas por amiodarona en ratas al restaurar un equilibrio más saludable de señales celulares y bloquear pasos clave que conducen a la fibrosis permanente. Aunque estos hallazgos aún no muestran cómo se comportará el cilostazol en humanos, señalan una estrategia práctica: reutilizar un fármaco aprobado para proteger los pulmones de pacientes que dependen de medicamentos cardiacos potentes. Será necesario trabajo adicional en distintos modelos y, eventualmente, ensayos clínicos, pero los resultados transmiten un mensaje claro para el público general: parte del daño causado por fármacos esenciales puede ser prevenible emparejándolos con compounds cuidadosamente seleccionados.
Cita: El-Gammal, M.A., Yousef, E.H., Abd Elhameed, A.G. et al. Cilostazol mitigates amiodarone-induced pulmonary toxicity and fibrosis by regulating the cAMP/TGF-β1 pathway-mediated epithelial-to-mesenchymal transition in rats. Sci Rep 16, 15055 (2026). https://doi.org/10.1038/s41598-026-45341-3
Palabras clave: fibrosis pulmonar, toxicidad pulmonar por amiodarona, cilostazol, enfermedad pulmonar inducida por fármacos, señalización cAMP