Clear Sky Science · pt
Cilostazol mitiga a toxicidade pulmonar e a fibrose induzidas por amiodarona ao regular a transição epitélio-mesenquimal mediada pela via cAMP/TGF-β1 em ratos
Por que este estudo pulmonar é importante
A fibrose pulmonar é uma lesão lenta e cicatricial nos pulmões que torna cada respiração mais difícil, e pode ser desencadeada por alguns medicamentos cardíacos que salvam vidas. Este estudo em ratos investiga se um medicamento já existente, o cilostazol, pode proteger os pulmões dos danos causados pelo amplamente usado antiarrítmico amiodarona. Ao seguir tanto a lesão visível nos pulmões quanto os sinais químicos ocultos dentro das células pulmonares, os pesquisadores fazem uma pergunta otimista: podemos manter tratamentos cardíacos vitais protegendo melhor os pulmões?
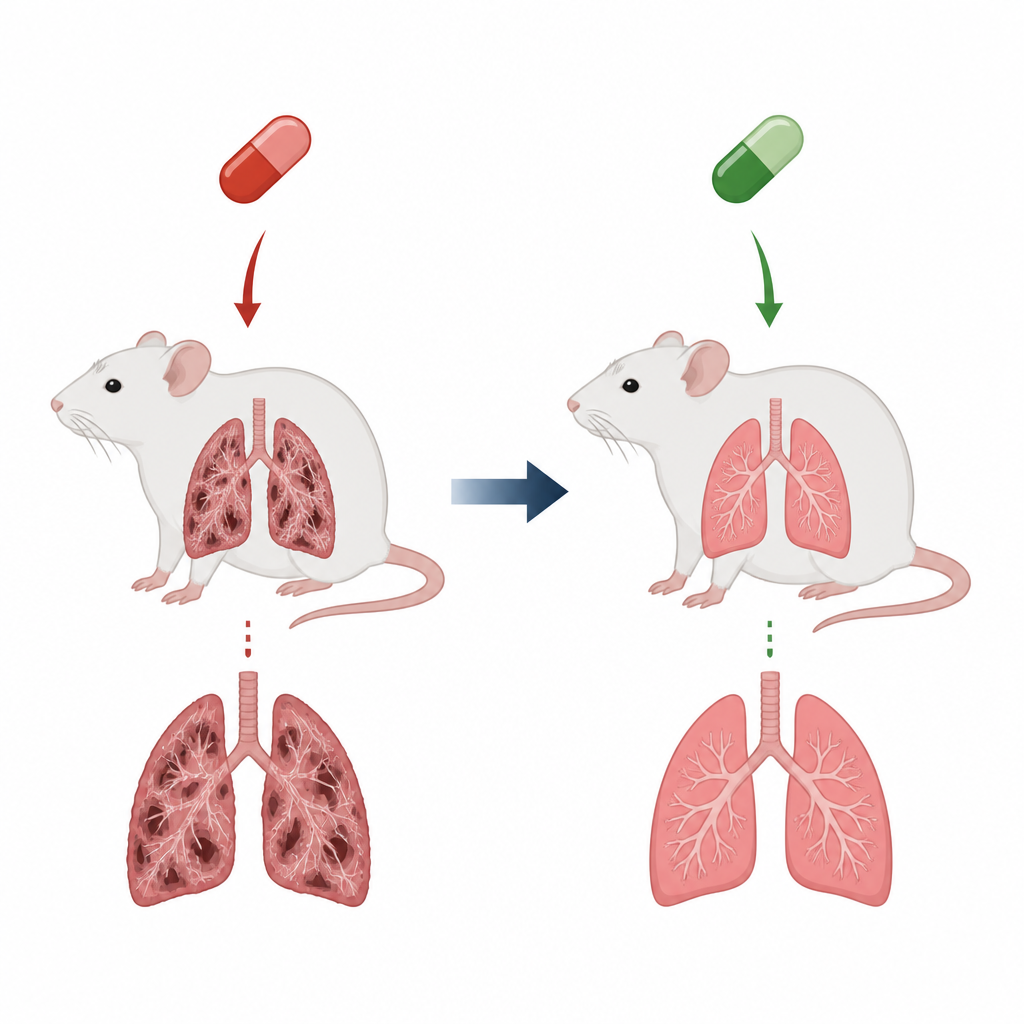
Um remédio cardíaco com um custo oculto
A amiodarona é prescrita para corrigir problemas perigosos de ritmo cardíaco, mas uma desvantagem séria é seu potencial de danificar o tecido pulmonar e levar à fibrose pulmonar. Na fibrose, os delicados alvéolos que trocam oxigênio tornam-se rígidos e cicatrizados, dificultando a respiração e reduzindo a expectativa de vida. Neste modelo de rato, doses diárias de amiodarona por várias semanas reproduziram muitas características dessa condição: pulmões mais pesados, vias aéreas inflamadas cheias de células imunes e espessas faixas de colágeno que distorceram a estrutura pulmonar normal. Essas mudanças espelham o que os clínicos temem em pacientes que desenvolvem cicatrização pulmonar relacionada a fármacos.
Testando um medicamento parceiro protetor
O cilostazol é um comprimido já usado para melhorar o fluxo sanguíneo em artérias das pernas obstruídas e para reduzir certos tipos de risco de AVC. Ele atua em parte elevando os níveis de uma pequena molécula de sinalização chamada cAMP, que pode acalmar a inflamação e limitar a formação de cicatrizes nos tecidos. Os pesquisadores dividiram os ratos em três grupos: controles saudáveis, animais recebendo apenas amiodarona e animais tratados com cilostazol antes de cada dose de amiodarona. Em seguida, coletaram líquido dos pulmões, examinaram fatias de tecido ao microscópio e mediram marcadores químicos de oxidação, inflamação e cicatrização para ver se o cilostazol poderia atenuar o dano pulmonar.
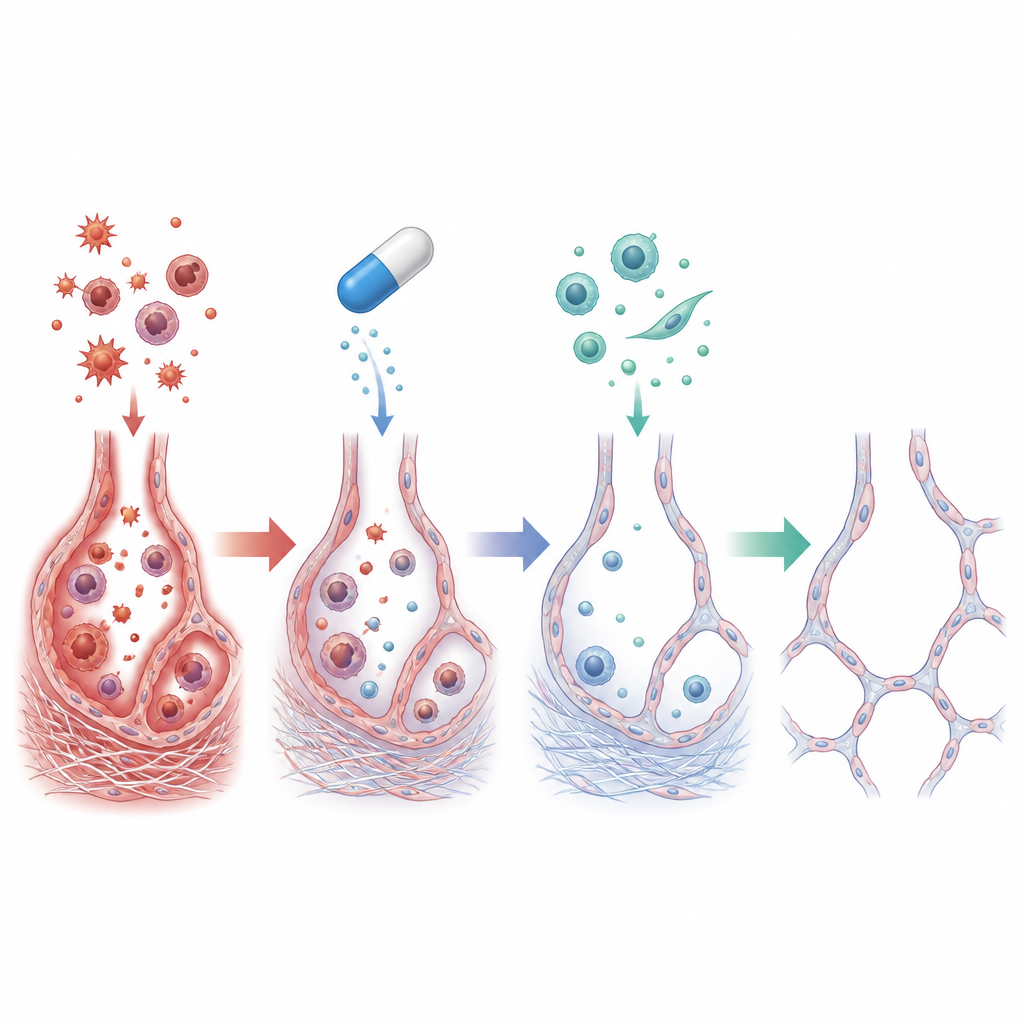
O que aconteceu dentro dos pulmões lesionados
Nos ratos que receberam apenas amiodarona, os pulmões apresentaram inflamação intensa: a contagem de células imunes no líquido das vias aéreas disparou e os níveis de mensageiros inflamatórios como TNF-alfa e IL-1 beta aumentaram várias vezes. Impressões químicas de estresse oxidativo cresceram, com mais dano lipídico e defesas antioxidantes reduzidas. Ao microscópio, a equipe observou alvéolos colapsados e distorcidos rodeados por depósitos pesados de colágeno. Mais profundamente nas células, havia sinais de que as células epiteliais que revestem os alvéolos começavam a comportar-se mais como células formadoras de cicatriz, uma mudança conhecida como transição epitélio-mesenquimal que impulsiona a fibrose de longa duração.
Como o cilostazol mudou o cenário
Quando o cilostazol foi adicionado, muitas dessas alterações nocivas foram fortemente reduzidas. Pulmões de ratos tratados pesaram menos e pareceram muito mais próximos do normal, com acúmulo de colágeno bastante menor e alvéolos melhor preservados. Células inflamatórias e citocinas caíram em direção aos níveis dos controles, e os marcadores de dano oxidativo diminuíram enquanto os antioxidantes naturais se recuperaram. No nível molecular, o cilostazol aumentou o cAMP e elevou a atividade de fatores protetores como SIRT1 e EPAC1, enquanto reduziu sinais ligados à cicatrização, incluindo TGF-beta1 e vimentina. Juntas, essas mudanças sugerem que o cilostazol não apenas acalmou a inflamação e o estresse oxidativo, mas também interrompeu a reprogramação celular que transforma células de revestimento saudáveis em produtoras de cicatriz.
Dos pulmões de rato a ideias para tratamentos futuros
O estudo conclui que o cilostazol pode atenuar significativamente a lesão pulmonar e a cicatrização induzidas por amiodarona em ratos ao restaurar um equilíbrio mais saudável de sinais celulares e bloquear etapas-chave que levam à fibrose permanente. Embora esses achados ainda não mostrem como o cilostazol atuará em humanos, apontam para uma estratégia prática: reaproveitar um medicamento aprovado para proteger os pulmões de pacientes que dependem de fármacos cardíacos potentes. Serão necessários mais trabalhos em modelos diferentes e, eventualmente, ensaios clínicos, mas os resultados oferecem uma mensagem clara para não especialistas: parte do dano causado por medicamentos essenciais pode ser evitável ao pareá-los com parceiros cuidadosamente escolhidos.
Citação: El-Gammal, M.A., Yousef, E.H., Abd Elhameed, A.G. et al. Cilostazol mitigates amiodarone-induced pulmonary toxicity and fibrosis by regulating the cAMP/TGF-β1 pathway-mediated epithelial-to-mesenchymal transition in rats. Sci Rep 16, 15055 (2026). https://doi.org/10.1038/s41598-026-45341-3
Palavras-chave: fibrose pulmonar, toxicidade pulmonar por amiodarona, cilostazol, doença pulmonar induzida por fármacos, sinalização cAMP