Clear Sky Science · ru
Цилостазол ослабляет пульмональный токсический эффект и фиброз, вызванные амиодароном, через регуляцию эпителиально-мезенхимального перехода, опосредованного путем cAMP/TGF-β1 у крыс
Почему это исследование лёгких важно
Пульмональный фиброз — это медленное рубцевание лёгочной ткани, которое затрудняет дыхание, и его может вызывать часть жизненно важных сердечных препаратов. Это исследование на крысах изучает, может ли существующее лекарство, цилостазол, защитить лёгкие от повреждений, вызванных широко применяемым антиаритмическим средством амиодароном. Отслеживая как видимые повреждения лёгких, так и скрытые химические сигналы внутри клеток лёгкой ткани, авторы задают обнадеживающий вопрос: можно ли сохранить важные сердечные терапии и при этом лучше защищать лёгкие?
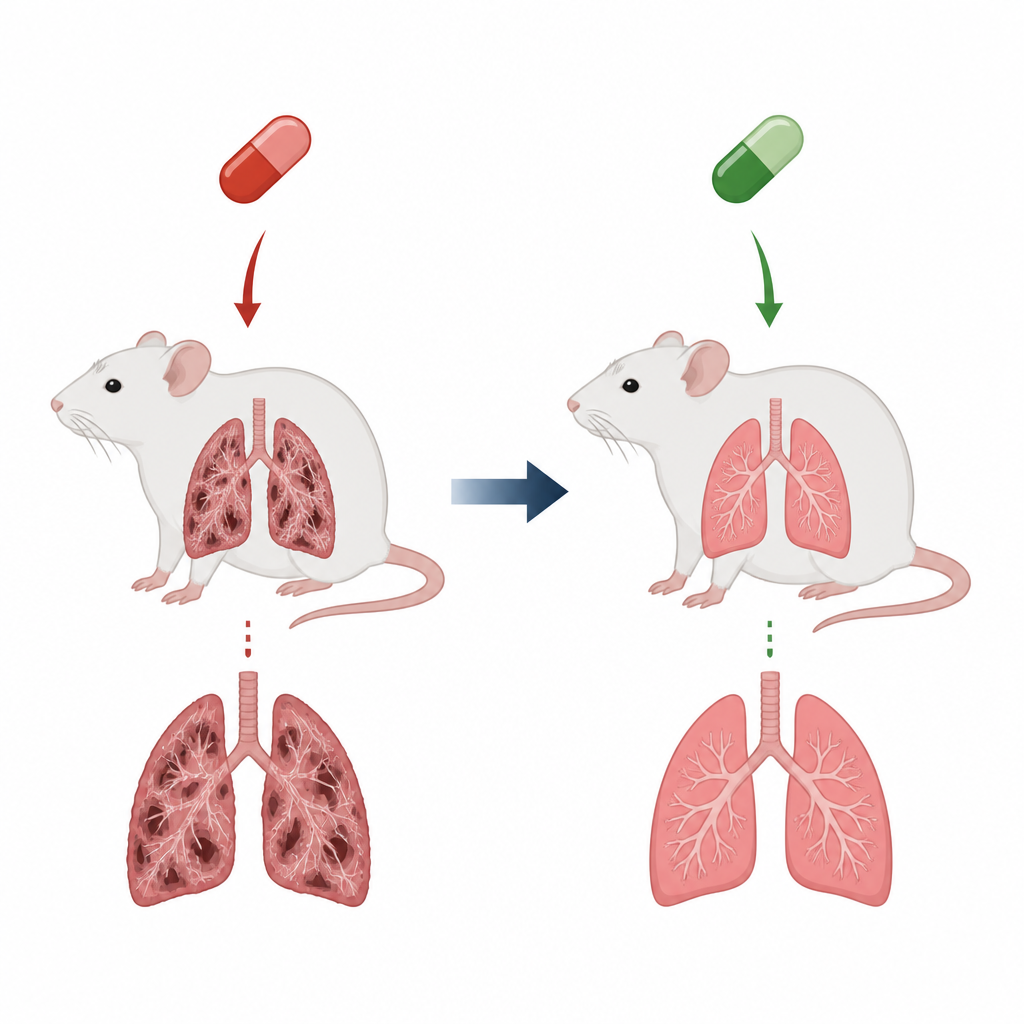
Сердечное лекарство с скрытой ценой
Амиодарон назначают для коррекции опасных нарушений ритма сердца, но серьёзным недостатком является его потенциал повреждать лёгкую ткань и приводить к пульмональному фиброзу. При фиброзе тонкие альвеолы, где происходит газообмен, становятся жесткими и рубцованными, что делает дыхание затруднённым и сокращает продолжительность жизни. В этой модели на крысах ежедневные дозы амиодарона в течение нескольких недель воспроизвели многие черты этого состояния: утяжелённые лёгкие, воспалённые дыхательные пути, заполненные иммунными клетками, и плотные участки коллагена, искажающие нормальную структуру лёгкого. Эти изменения отражают то, чего опасаются клиницисты у пациентов с лекарственно‑индуцированным рубцеванием лёгких.
Испытание защитного сопутствующего препарата
Цилостазол — таблетка, уже используемая для улучшения кровотока при закупорке артерий ног и для снижения риска некоторых типов инсульта. Он действует частично за счёт повышения уровня небольшого сигнального молекулы cAMP, которая может успокаивать воспаление и ограничивать образование рубцовой ткани в органах. Исследователи разделили крыс на три группы: здоровые контрольные животные, животные, получавшие только амиодарон, и животные, получавшие цилостазол перед каждой дозой амиодарона. Затем они собирали жидкость из лёгких, изучали срезы тканей под микроскопом и измеряли химические маркёры окисления, воспаления и фиброза, чтобы выяснить, может ли цилостазол ослабить повреждение лёгких.
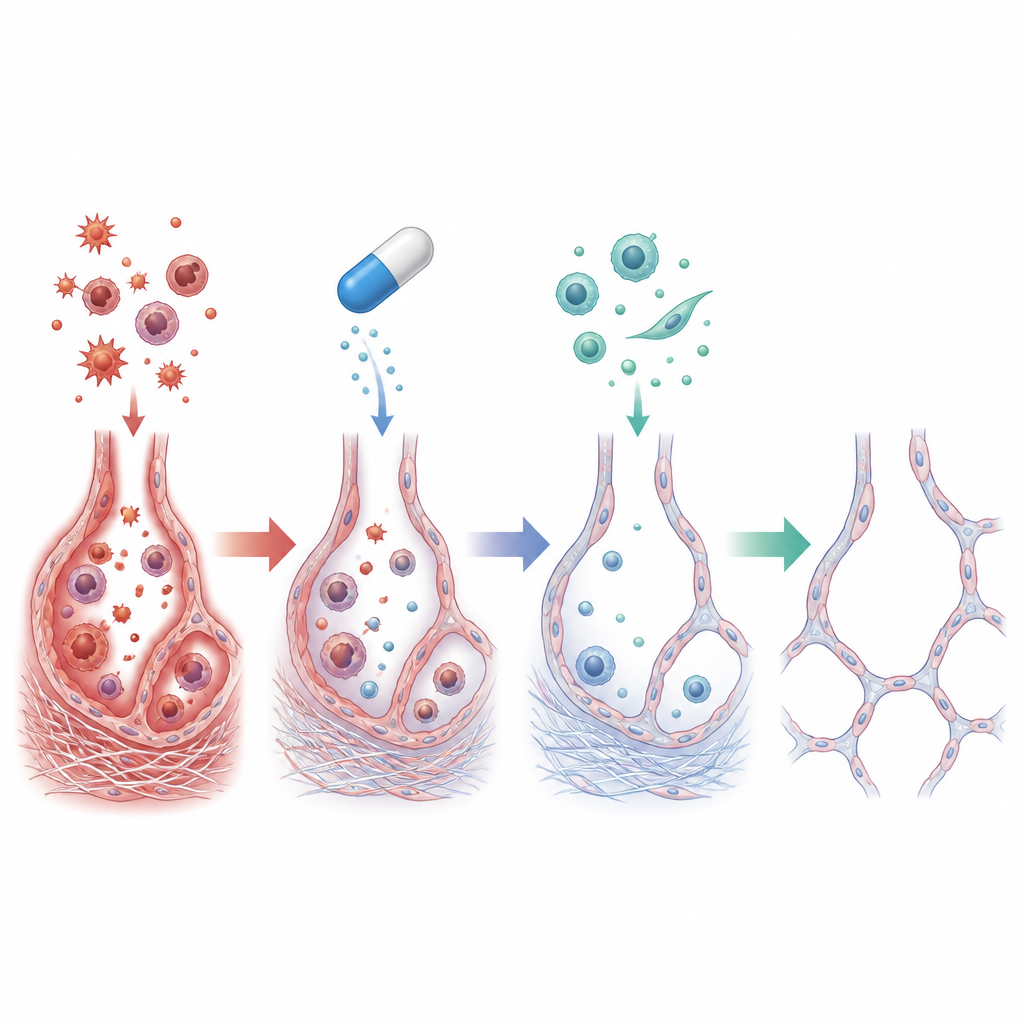
Что происходило внутри повреждённых лёгких
У крыс, получавших только амиодарон, лёгкие демонстрировали сильное воспаление: количество иммунных клеток в бронхиальном лаваже резко выросло, а уровни провоспалительных медиаторов, таких как TNF‑α и IL‑1β, увеличились в несколько раз. Химические следы окислительного стресса также возросли — больше повреждения липидов и истощение антиоксидантной защиты. Под микроскопом исследователи видели спад и деформацию альвеол, окружённых обильными отложениями коллагена. Глубже в клетках наблюдались признаки того, что эпителиальные клетки, выстилающие альвеолы, начинают вести себя как клетки, формирующие рубцовую ткань — переход, известный как эпителиально‑мезенхимальный переход, который способствует устойчивому фиброзу.
Как цилостазол изменил картину
При добавлении цилостазола многие из этих вредных изменений заметно уменьшились. Лёгкие обработанных животных были легче и выглядели гораздо ближе к норме, с гораздо меньшими отложениями коллагена и лучше сохранёнными альвеолами. Число воспалительных клеток и уровень цитокинов снизились к значениям контроля, а маркёры окислительного повреждения упали, в то время как природные антиоксиданты восстановились. На молекулярном уровне цилостазол повышал уровень cAMP и усиливал активность защитных посредников, таких как SIRT1 и EPAC1, одновременно подавляя сигналы, связанные с фиброзом, включая TGF‑β1 и виментин. В совокупности эти изменения указывают на то, что цилостазол не только ослаблял воспаление и окислительный стресс, но и прерывал клеточную перепрограммировку, превращающую здоровые эпителиальные клетки в продуцирующие рубцовую ткань.
От лёгких крыс к идеям для будущего лечения
Авторы приходят к выводу, что цилостазол может существенно смягчать повреждение и рубцевание лёгких, вызванные амиодароном у крыс, восстанавливая более здоровый баланс клеточных сигналов и блокируя ключевые шаги, ведущие к перманентному фиброзу. Хотя эти данные ещё не показывают, как цилостазол проявит себя у людей, они указывают на практическую стратегию: перепрофилирование одобренного препарата для защиты лёгких у пациентов, зависящих от мощных сердечных средств. Потребуются дальнейшие исследования на других моделях и, в конечном счёте, клинические испытания, но результаты дают ясное послание неспециалистам: часть вреда, наносимого жизненно важными лекарствами, возможно предотвратить, сочетая их с тщательно подобранными партнёрами.
Цитирование: El-Gammal, M.A., Yousef, E.H., Abd Elhameed, A.G. et al. Cilostazol mitigates amiodarone-induced pulmonary toxicity and fibrosis by regulating the cAMP/TGF-β1 pathway-mediated epithelial-to-mesenchymal transition in rats. Sci Rep 16, 15055 (2026). https://doi.org/10.1038/s41598-026-45341-3
Ключевые слова: пульмональный фиброз, токсичность лёгких от амиодарона, цилостазол, лекарственно-индуцированные заболевания лёгких, сигнализация cAMP