Clear Sky Science · fr
Le cilostazol atténue la toxicité pulmonaire et la fibrose induites par l’amiodarone en régulant la transition épithélio-mésenchymateuse médiée par la voie cAMP/TGF-β1 chez le rat
Pourquoi cette étude pulmonaire compte
La fibrose pulmonaire est une lésion progressive et cicatricielle des poumons qui rend chaque respiration plus difficile, et elle peut être déclenchée par certains médicaments cardiaques salvateurs. Cette étude chez le rat examine si un médicament existant, le cilostazol, peut protéger les poumons des lésions causées par l’antidysrythmique largement utilisé, l’amiodarone. En suivant à la fois les lésions visibles et les signaux chimiques dissimulés à l’intérieur des cellules pulmonaires, les chercheurs posent une question porteuse d’espoir : peut-on préserver des traitements cardiaques vitaux tout en mieux protégeant les poumons ?
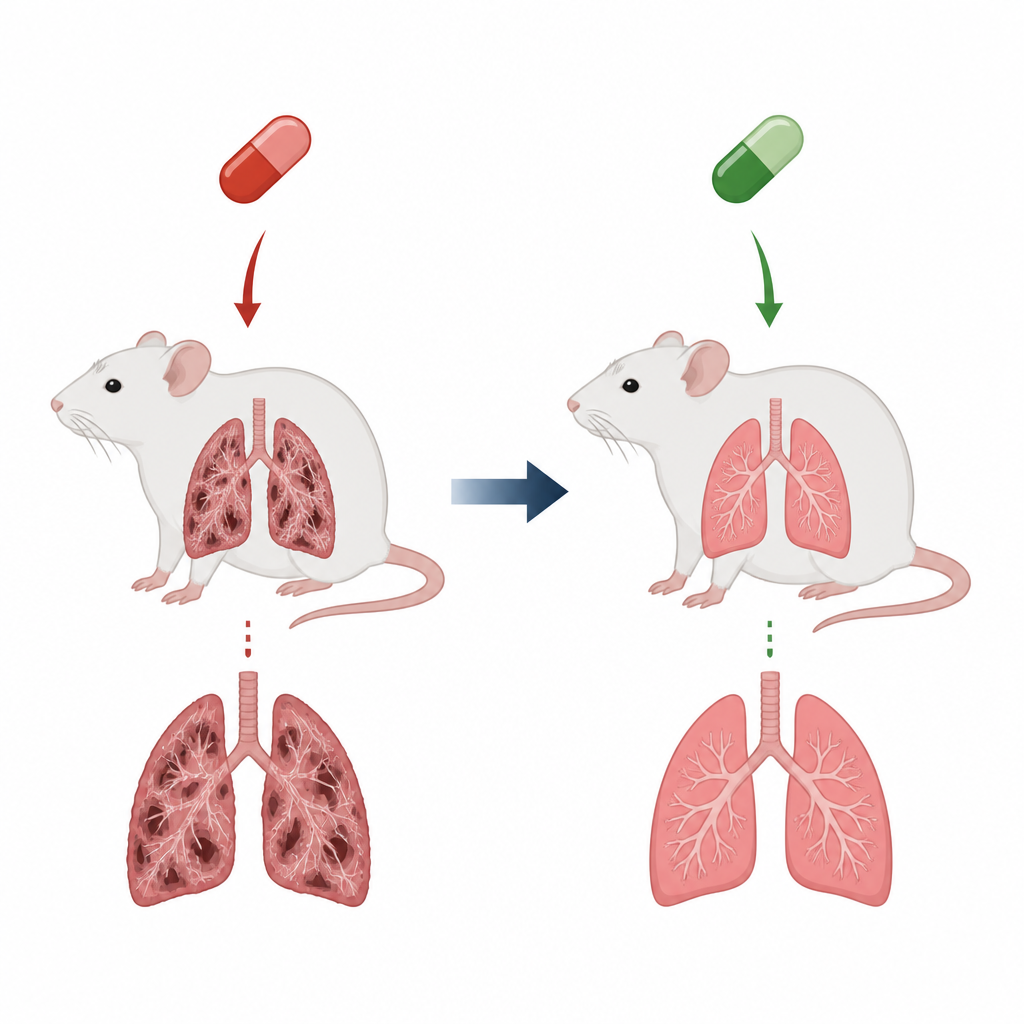
Un médicament cardiaque au coût caché
L’amiodarone est prescrite pour corriger des troubles du rythme cardiaque dangereux, mais un inconvénient sérieux est son potentiel à endommager le tissu pulmonaire et à conduire à une fibrose pulmonaire. Dans la fibrose, les alvéoles délicates qui échangent l’oxygène deviennent rigides et cicatrisées, rendant la respiration laborieuse et raccourcissant l’espérance de vie. Dans ce modèle de rat, des doses quotidiennes d’amiodarone pendant plusieurs semaines ont reproduit de nombreuses caractéristiques de ce tableau : des poumons alourdis, des voies respiratoires enflammées remplies de cellules immunitaires, et d’épaisses bandes de collagène déformant la structure pulmonaire normale. Ces changements reflètent ce que les cliniciens redoutent chez les patients qui développent une cicatrisation pulmonaire d’origine médicamenteuse.
Tester un médicament partenaire protecteur
Le cilostazol est un comprimé déjà utilisé pour améliorer le flux sanguin dans les artères obstruées des jambes et pour réduire certains risques d’accident vasculaire. Il agit en partie en augmentant les niveaux d’une petite molécule de signalisation appelée cAMP, qui peut calmer l’inflammation et limiter la cicatrisation des tissus. Les chercheurs ont réparti les rats en trois groupes : témoins sains, animaux recevant uniquement de l’amiodarone, et animaux traités par cilostazol avant chaque dose d’amiodarone. Ils ont ensuite prélevé du liquide pulmonaire, examiné des coupes de tissu au microscope et mesuré des marqueurs chimiques d’oxydation, d’inflammation et de fibrose pour savoir si le cilostazol pouvait atténuer les lésions pulmonaires.
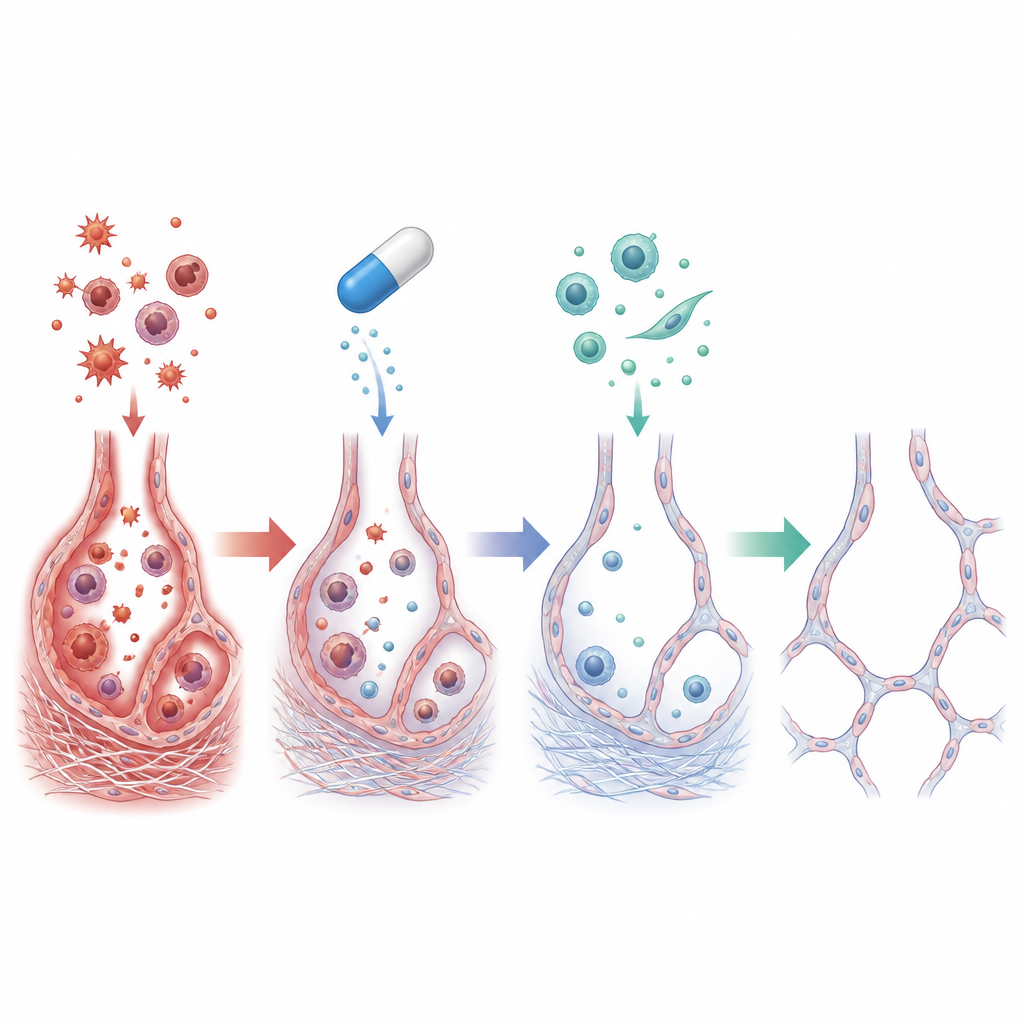
Ce qui s’est passé dans les poumons atteints
Chez les rats ayant reçu seulement de l’amiodarone, les poumons présentaient une inflammation intense : le nombre de cellules immunitaires dans le liquide des voies aériennes a fortement augmenté, et les niveaux de médiateurs inflammatoires tels que le TNF-alpha et l’IL-1 beta ont crû de plusieurs fois. Les empreintes chimiques du stress oxydatif se sont accrues, avec davantage de dommages lipidiques et des défenses antioxydantes appauvries. Au microscope, l’équipe a observé des alvéoles effondrées et déformées entourées de dépôts massifs de collagène. Plus profondément dans les cellules, on notait des signes que les cellules épithéliales tapissant les alvéoles commençaient à se comporter davantage comme des cellules productrices de cicatrice, un basculement connu sous le nom de transition épithélio-mésenchymateuse qui favorise la fibrose durable.
Comment le cilostazol a changé le tableau
Lorsque le cilostazol a été ajouté, nombre de ces modifications délétères ont été fortement réduites. Les poumons des animaux traités étaient plus légers et paraissaient beaucoup plus proches de la normale, avec une accumulation de collagène bien plus faible et des alvéoles mieux préservées. Les cellules inflammatoires et les cytokines ont diminué vers les niveaux témoins, et les marqueurs de dommage oxydatif ont décliné tandis que les antioxydants naturels rebondissaient. Au niveau moléculaire, le cilostazol a élevé le cAMP et augmenté l’activité d’acteurs protecteurs tels que SIRT1 et EPAC1, tout en réduisant les signaux associés à la fibrose, notamment le TGF-beta1 et la vimentine. Ensemble, ces variations suggèrent que le cilostazol a non seulement calmé l’inflammation et le stress oxydatif, mais a aussi interrompu le reprogrammation cellulaire qui transforme les cellules de revêtement saines en cellules productrices de cicatrice.
Des poumons de rat aux idées de traitements futurs
L’étude conclut que le cilostazol peut atténuer notablement les lésions pulmonaires et la cicatrisation induites par l’amiodarone chez le rat en rétablissant un équilibre plus sain des signaux cellulaires et en bloquant des étapes clés menant à la fibrose permanente. Si ces résultats ne prédisent pas encore la performance du cilostazol chez l’humain, ils pointent vers une stratégie pratique : réutiliser un médicament approuvé pour protéger les poumons des patients qui dépendent de médicaments cardiaques puissants. Des travaux supplémentaires dans d’autres modèles et, à terme, des essais cliniques seront nécessaires, mais les résultats délivrent un message clair pour un public non spécialiste : une partie des dommages causés par des médicaments essentiels pourrait être évitée en les associant à des partenaires choisis avec soin.
Citation: El-Gammal, M.A., Yousef, E.H., Abd Elhameed, A.G. et al. Cilostazol mitigates amiodarone-induced pulmonary toxicity and fibrosis by regulating the cAMP/TGF-β1 pathway-mediated epithelial-to-mesenchymal transition in rats. Sci Rep 16, 15055 (2026). https://doi.org/10.1038/s41598-026-45341-3
Mots-clés: fibrose pulmonaire, toxicité pulmonaire liée à l’amiodarone, cilostazol, maladie pulmonaire médicamenteuse, signalisation cAMP