Clear Sky Science · nl
Cilostazol vermindert amiodaron-geïnduceerde longtoxiciteit en fibrose door regulatie van de cAMP/TGF-β1-route-gemedieerde epitheel-naar-mesenchym transformatie bij ratten
Waarom deze longstudie ertoe doet
Longfibrose is een langzaam verlopende littekenvorming van de longen die elke ademhaling bemoeilijkt en kan worden uitgelokt door sommige levensreddende hartmedicijnen. Deze rattenstudie onderzoekt of een bestaand geneesmiddel, cilostazol, de longen kan beschermen tegen schade veroorzaakt door het veelgebruikte antiaritmicum amiodaron. Door zowel de zichtbare longbeschadiging als de verborgen chemische signalen binnen longcellen te volgen, stellen de onderzoekers een hoopvolle vraag: kunnen we essentiële hartbehandelingen behouden terwijl we de longen beter beschermen?
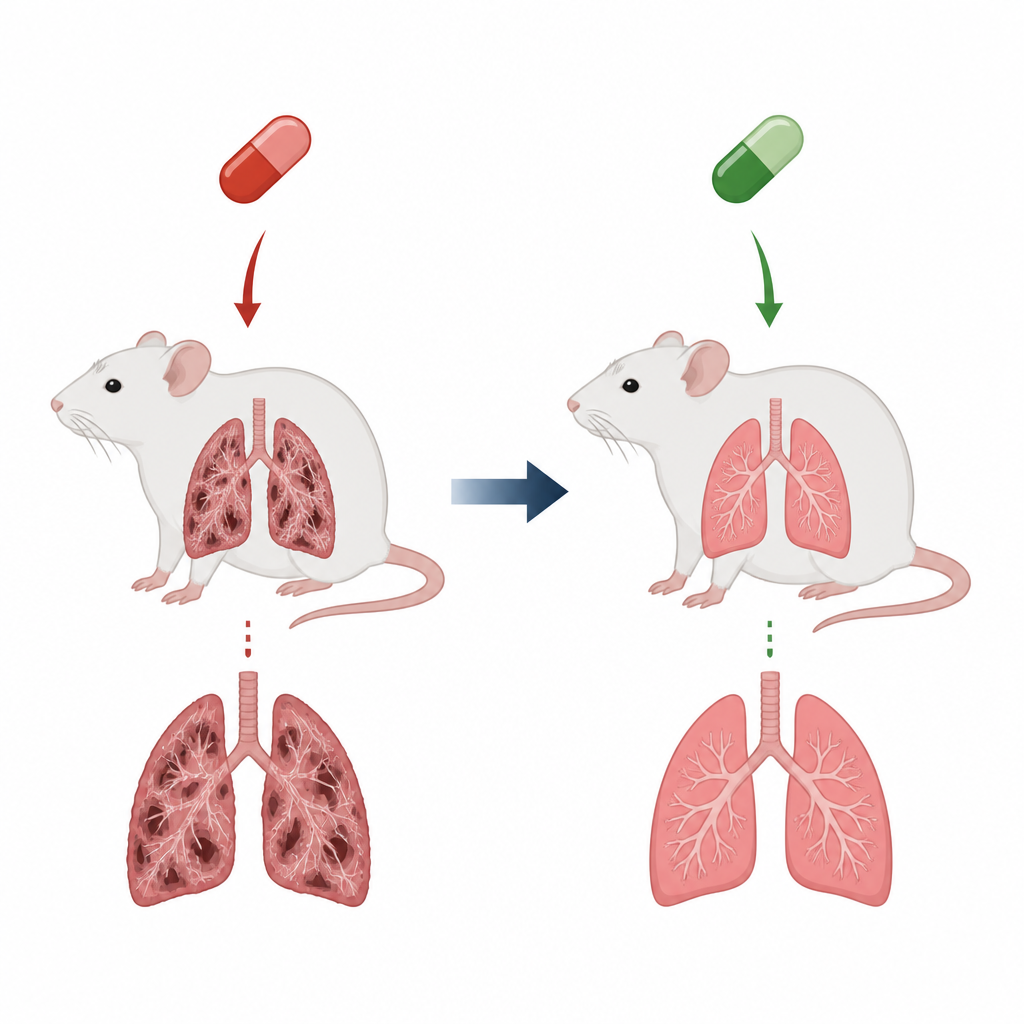
Een hartmedicijn met een verborgen prijs
Amiodaron wordt voorgeschreven om gevaarlijke hartritmestoornissen te corrigeren, maar een ernstig nadeel is het potentieel om longweefsel te beschadigen en te leiden tot longfibrose. Bij fibrose worden de fijne luchtzakjes die zuurstof uitwisselen stijf en littekenachtig, waardoor ademhalen zwaar wordt en de levensverwachting afneemt. In dit rattenschema reproduceerden dagelijkse amiodarondoses gedurende enkele weken veel kenmerken van deze aandoening: zwaardere longen, ontstoken luchtwegen gevuld met immuuncellen, en dikke banden collageen die de normale longstructuur vervormden. Deze veranderingen weerspiegelen wat clinici vrezen bij patiënten die medicatiegerelateerde littekenvorming in hun longen ontwikkelen.
Het testen van een beschermend partnergeneesmiddel
Cilostazol is een pil die al wordt gebruikt om de bloedstroom in verstopte beenaders te verbeteren en om het risico op bepaalde soorten beroerte te verminderen. Het werkt deels door de niveaus van een klein signaalmolecuul, cAMP, te verhogen, wat ontsteking kan kalmeren en littekenvorming in weefsels kan beperken. De onderzoekers verdeelden ratten in drie groepen: gezonde controles, dieren die alleen amiodaron kregen, en dieren die cilostazol kregen vóór elke amiodarondosering. Vervolgens verzamelden ze vloeistof uit de longen, onderzochten weefselplakjes onder de microscoop en maten ze chemische merkers voor oxidatie, ontsteking en littekenvorming om te zien of cilostazol de longschade kon verzachten.
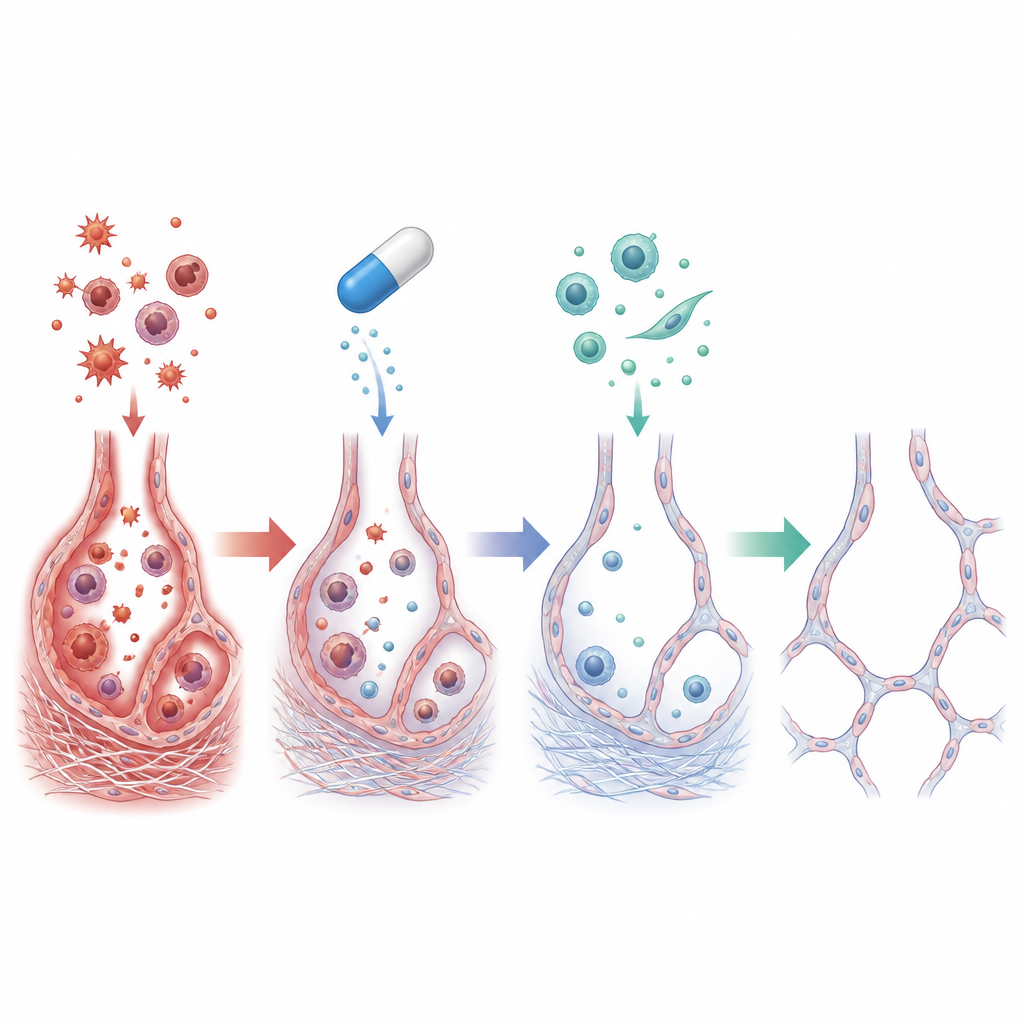
Wat er zich afspeelde in de beschadigde longen
Bij ratten die alleen amiodaron kregen, toonden de longen intense ontsteking: het aantal immuuncellen in de luchtwegvloeistof nam sterk toe en de niveaus van ontstekingsmediatoren zoals TNF-alpha en IL-1 beta stegen meerdere malen. Chemische sporen van oxidatieve stress namen toe, met meer vetbeschadiging en uitgeputte antioxidatieve verdedigingen. Onder de microscoop zag het team ineengezakte en vervormde luchtzakjes omringd door zware collageenafzettingen. Verder in de cellen waren er aanwijzingen dat epitheelcellen die de luchtzakjes bekleden zich begonnen te gedragen als littekenvormende cellen, een verschuiving bekend als epitheel-naar-mesenchym transformatie die blijvende fibrose aanjaagt.
Hoe cilostazol het beeld veranderde
Toen cilostazol werd toegevoegd, werden veel van deze schadelijke veranderingen sterk verminderd. Longen van behandelde ratten wogen minder en leken veel dichter bij normaal, met veel mildere collageenophoping en beter bewaarde luchtzakjes. Ontstekingscellen en cytokinen daalden richting controlevelden en markers voor oxidatieve schade namen af terwijl natuurlijke antioxidanten herstelden. Op moleculair niveau verhoogde cilostazol cAMP en verhoogde de activiteit van beschermende spelers zoals SIRT1 en EPAC1, terwijl signalen die met littekenvorming geassocieerd zijn, waaronder TGF-beta1 en vimentine, werden teruggeschroefd. Gezamenlijk suggereren deze verschuivingen dat cilostazol niet alleen ontsteking en oxidatieve stress dempte maar ook de cellulaire herprogrammering onderbrak die gezonde bekledingscellen in littekenproducerende cellen verandert.
Van ratlongen naar ideeën voor toekomstige behandelingen
De studie concludeert dat cilostazol de door amiodaron veroorzaakte longbeschadiging en littekenvorming bij ratten aanzienlijk kan verzachten door een gezondere balans van celsignalen te herstellen en sleutelstappen die tot permanente fibrose leiden te blokkeren. Hoewel deze bevindingen nog niet laten zien hoe cilostazol zich bij mensen zal gedragen, wijzen ze op een praktische strategie: het herbestemmen van een goedgekeurd geneesmiddel om de longen te beschermen van patiënten die afhankelijk zijn van krachtige hartmedicijnen. Verder onderzoek in andere modellen en uiteindelijk klinische onderzoeken zal nodig zijn, maar de resultaten bieden een duidelijke boodschap voor niet-specialisten: een deel van de schade veroorzaakt door noodzakelijke medicijnen kan mogelijk worden voorkomen door ze te combineren met zorgvuldig gekozen partners.
Bronvermelding: El-Gammal, M.A., Yousef, E.H., Abd Elhameed, A.G. et al. Cilostazol mitigates amiodarone-induced pulmonary toxicity and fibrosis by regulating the cAMP/TGF-β1 pathway-mediated epithelial-to-mesenchymal transition in rats. Sci Rep 16, 15055 (2026). https://doi.org/10.1038/s41598-026-45341-3
Trefwoorden: longfibrose, amiodaron longtoxiciteit, cilostazol, door medicatie veroorzaakte longziekte, cAMP-signaalgeving