Clear Sky Science · de
Cilostazol mildert amiodaroninduzierte Lungentoxizität und Fibrose durch Regulierung des cAMP/TGF-β1-Wegs-vermittelten epithelial-mesenchymalen Übergangs bei Ratten
Warum diese Lungenstudie wichtig ist
Pulmonalfibrose ist eine schleichende Narbenbildung in der Lunge, die das Atmen erschwert, und sie kann durch einige lebensrettende Herzmedikamente ausgelöst werden. Diese Studie an Ratten untersucht, ob ein vorhandenes Medikament, Cilostazol, die Lungen vor Schäden schützen kann, die das weit verbreitete Antiarrhythmikum Amiodaron verursacht. Indem die Forschenden sowohl die sichtbaren Lungenschäden als auch die verborgenen chemischen Signale in Lungenzellen nachverfolgen, stellen sie eine hoffnungsvolle Frage: Können wir wichtige Herzbehandlungen beibehalten und gleichzeitig die Lunge besser schützen?
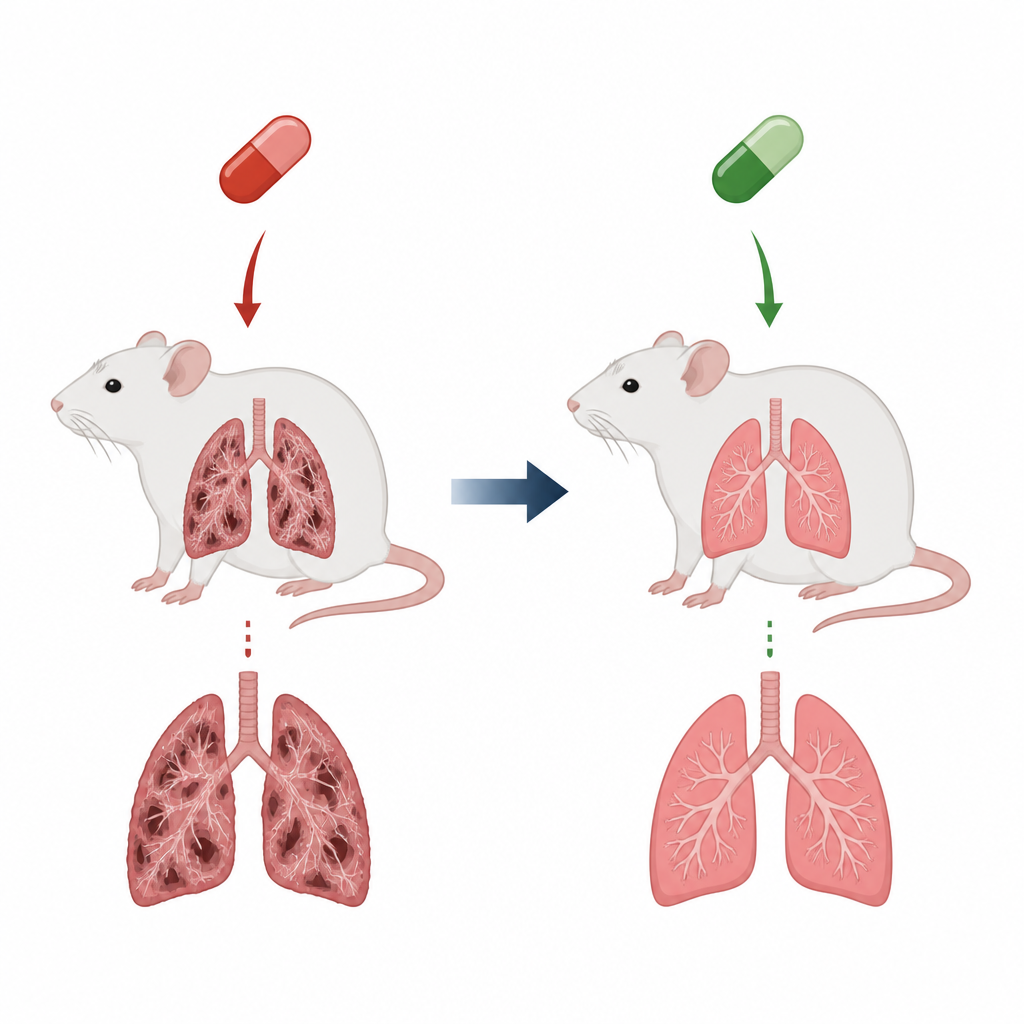
Ein Herzmedikament mit versteckten Kosten
Amiodaron wird zur Behandlung gefährlicher Herzrhythmusstörungen eingesetzt, hat jedoch den ernsten Nachteil, Lungengewebe zu schädigen und eine Pulmonalfibrose zu verursachen. Bei der Fibrose werden die empfindlichen Lungenbläschen, die den Gasaustausch ermöglichen, starr und vernarbt, was das Atmen erschwert und die Lebenserwartung verkürzen kann. In diesem Rattenmodell führten tägliche Amiodarondosen über mehrere Wochen zu vielen Merkmalen dieses Zustands: schwerere Lungen, entzündete Atemwege voller Immunzellen und dicke Kollagenablagerungen, die die normale Lungenstruktur verzerrten. Diese Veränderungen spiegeln das wider, wovor Kliniker Angst haben, wenn Patienten medikamentenbedingte Vernarbungen der Lunge entwickeln.
Test eines schützenden Begleitmedikaments
Cilostazol ist eine Tablette, die bereits zur Verbesserung des Blutflusses bei verengten Beinsarterien und zur Reduktion bestimmter Schlaganfallrisiken eingesetzt wird. Es wirkt zum Teil, indem es die Konzentration eines kleinen Signalmoleküls namens cAMP erhöht, das Entzündungen beruhigen und die Vernarbung von Geweben begrenzen kann. Die Forschenden teilten die Ratten in drei Gruppen: gesunde Kontrollen, Tiere, die nur Amiodaron erhielten, und Tiere, die vor jeder Amiodaron-Gabe Cilostazol bekamen. Anschließend entnahmen sie Flüssigkeit aus den Lungen, untersuchten Gewebeschnitte im Mikroskop und maßen chemische Marker für Oxidation, Entzündung und Vernarbung, um zu sehen, ob Cilostazol den Lungenschaden abschwächen konnte.
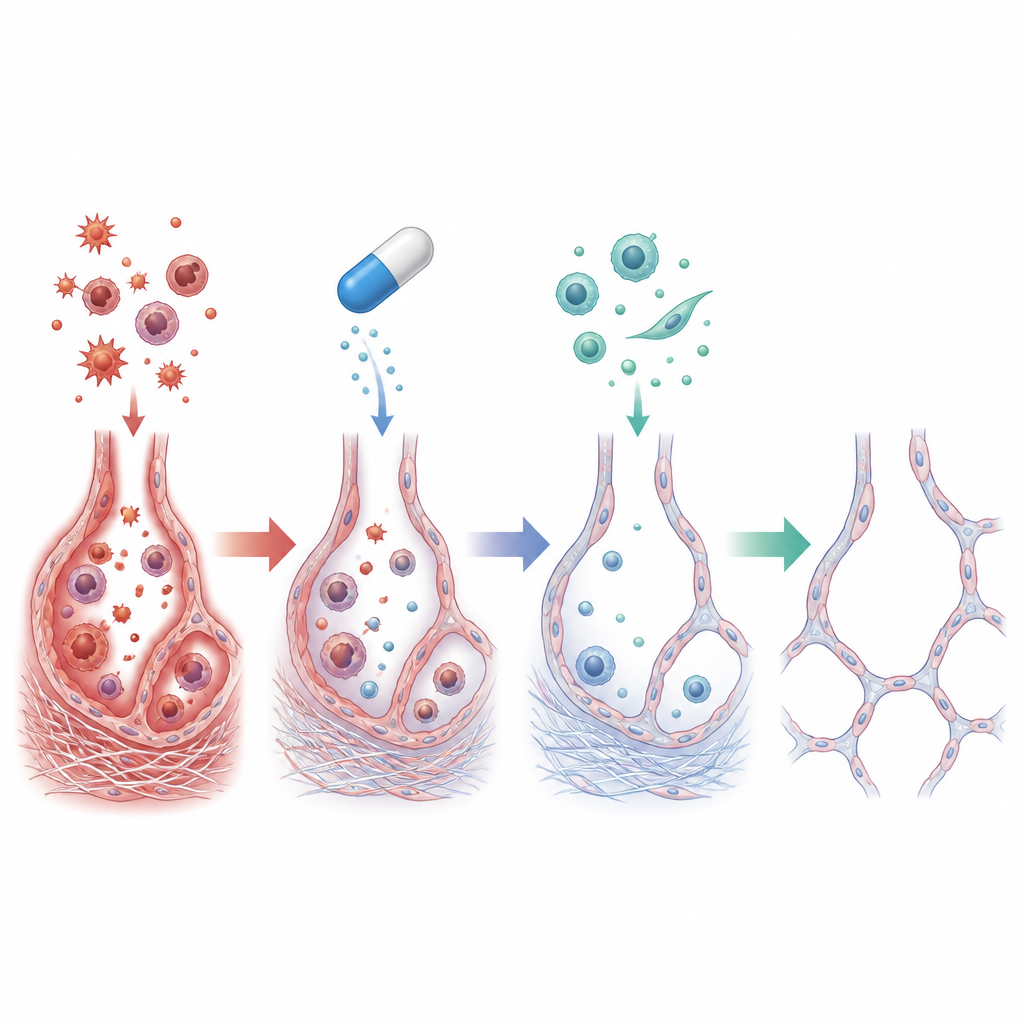
Was sich in den verletzten Lungen abspielte
Bei Ratten, die nur Amiodaron erhielten, zeigten die Lungen starke Entzündungen: Die Zahl der Immunzellen in der Atemwegsflüssigkeit stieg stark an, und die Spiegel entzündlicher Botenstoffe wie TNF-alpha und IL-1 beta erhöhten sich um ein Vielfaches. Chemische Kennzeichen oxidativen Stresses nahmen zu, mit mehr Lipidschäden und erschöpften antioxidativen Abwehrmechanismen. Im Mikroskop waren kollabierte und verzerrte Lungenbläschen zu sehen, umgeben von massiven Kollagenablagerungen. Tiefer in den Zellen gab es Hinweise darauf, dass die Epithelzellen, die die Lungenbläschen auskleiden, begannen, sich eher wie narbenbildende Zellen zu verhalten — eine Umstellung, die als epithelial-mesenchymaler Übergang bekannt ist und die dauerhafte Fibrose vorantreibt.
Wie Cilostazol das Bild veränderte
Mit zusätzlicher Gabe von Cilostazol wurden viele dieser schädlichen Veränderungen deutlich abgeschwächt. Die Lungen der behandelten Ratten wogen weniger und wirkten deutlich normaler, mit deutlich geringeren Kollagenansammlungen und besser erhaltenen Lungenbläschen. Entzündliche Zellen und Zytokine sanken gegen die Kontrollwerte, und Marker für oxidativen Schaden nahmen ab, während natürliche Antioxidantien wieder anstiegen. Auf molekularer Ebene erhöhte Cilostazol cAMP und steigerte die Aktivität schützender Akteure wie SIRT1 und EPAC1, während Signale, die mit Vernarbung verbunden sind — darunter TGF-beta1 und Vimentin — heruntergeregelt wurden. Zusammengenommen deuten diese Veränderungen darauf hin, dass Cilostazol nicht nur Entzündung und oxidativen Stress beruhigte, sondern auch die zelluläre Umprogrammierung unterbrach, die gesunde Epithelzellen in narbenbildende Zellen verwandelt.
Von Rattenlungen zu Ideen für zukünftige Behandlungen
Die Studie kommt zu dem Schluss, dass Cilostazol die amiodaronbedingten Lungenschäden und -vernarbungen bei Ratten deutlich abschwächen kann, indem es ein gesünderes Gleichgewicht der Signalsysteme wiederherstellt und Schlüsselschritte blockiert, die zur dauerhaften Fibrose führen. Während diese Ergebnisse noch nicht zeigen, wie Cilostazol beim Menschen wirkt, deuten sie auf eine praktische Strategie hin: die Umwidmung eines zugelassenen Medikaments, um die Lungen von Patienten zu schützen, die auf starke Herzmedikamente angewiesen sind. Weiterführende Arbeiten in anderen Modellen und schließlich klinische Studien werden nötig sein, doch die Ergebnisse vermitteln Laien eine klare Botschaft: Ein Teil des Schadens, den lebenswichtige Medikamente verursachen, könnte durch Kombination mit sorgsam ausgewählten Begleitmitteln vermeidbar sein.
Zitation: El-Gammal, M.A., Yousef, E.H., Abd Elhameed, A.G. et al. Cilostazol mitigates amiodarone-induced pulmonary toxicity and fibrosis by regulating the cAMP/TGF-β1 pathway-mediated epithelial-to-mesenchymal transition in rats. Sci Rep 16, 15055 (2026). https://doi.org/10.1038/s41598-026-45341-3
Schlüsselwörter: Pulmonalfibrose, Amiodaron-Lungentoxizität, Cilostazol, arzneimittelinduzierte Lungenerkrankung, cAMP-Signalgebung