Clear Sky Science · pl
Cilostazol łagodzi amiodaronem wywołaną toksyczność i włóknienie płuc poprzez regulację przejścia nabłonkowo-mezenchymalnego zależnego od szlaku cAMP/TGF-β1 u szczurów
Dlaczego to badanie płuc ma znaczenie
Włóknienie płuc to postępujące, bliznowaciejące uszkodzenie płuc, które utrudnia każdy oddech i może być wywołane przez niektóre ratujące życie leki kardiologiczne. To badanie na szczurach bada, czy istniejący lek — cilostazol — może chronić płuca przed uszkodzeniem wywołanym szeroko stosowanym lekiem przeciwarytmicznym amiodaronem. Śledząc zarówno widoczne uszkodzenia płuc, jak i ukryte sygnały chemiczne wewnątrz komórek płuc, badacze stawiają optymistyczne pytanie: czy możemy zachować niezbędne leczenie serca, jednocześnie lepiej chroniąc płuca?
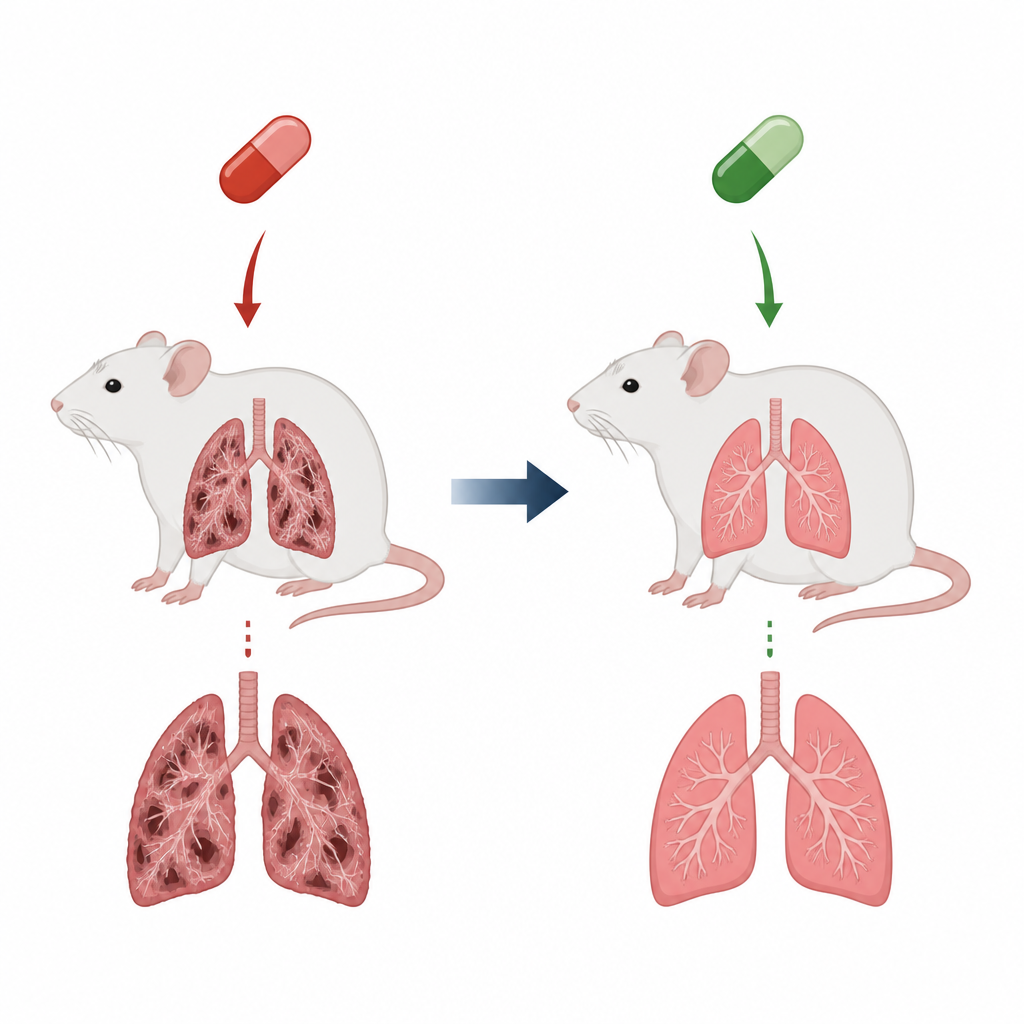
Lek sercowy z ukrytą ceną
Amiodaron jest przepisywany w celu skorygowania groźnych zaburzeń rytmu serca, ale poważnym mankamentem jest jego potencjał do uszkadzania tkanki płucnej i prowadzenia do włóknienia płuc. W przebiegu włóknienia delikatne pęcherzyki płucne odpowiedzialne za wymianę tlenu stają się sztywne i zbliznowaciałe, co utrudnia oddychanie i skraca oczekiwaną długość życia. W tym modelu szczurzym codzienne dawki amiodaronu przez kilka tygodni odtworzyły wiele cech tego stanu: cięższe płuca, zapalone drogi oddechowe wypełnione komórkami układu odpornościowego oraz grube pasma kolagenu zniekształcające normalną strukturę płuca. Te zmiany odzwierciedlają obawy klinicystów dotyczące pacjentów rozwijających lekom wywołane bliznowacenie płuc.
Testowanie leku partnerskiego o działaniu ochronnym
Cilostazol to lek stosowany już w celu poprawy przepływu krwi w zatkanych tętnicach nóg i w zmniejszaniu ryzyka niektórych typów udaru. Działa częściowo poprzez podnoszenie poziomu niewielkiej cząsteczki sygnałowej zwanej cAMP, która może łagodzić zapalenie i ograniczać bliznowacenie tkanek. Badacze podzielili szczury na trzy grupy: kontrolne, zwierzęta otrzymujące sam amiodaron oraz zwierzęta otrzymujące cilostazol przed każdą dawką amiodaronu. Następnie pobrali płyn z płuc, zbadali fragmenty tkanki pod mikroskopem i zmierzyli markery chemiczne oksydacji, zapalenia i bliznowacenia, aby sprawdzić, czy cilostazol może stłumić uszkodzenia płuc.
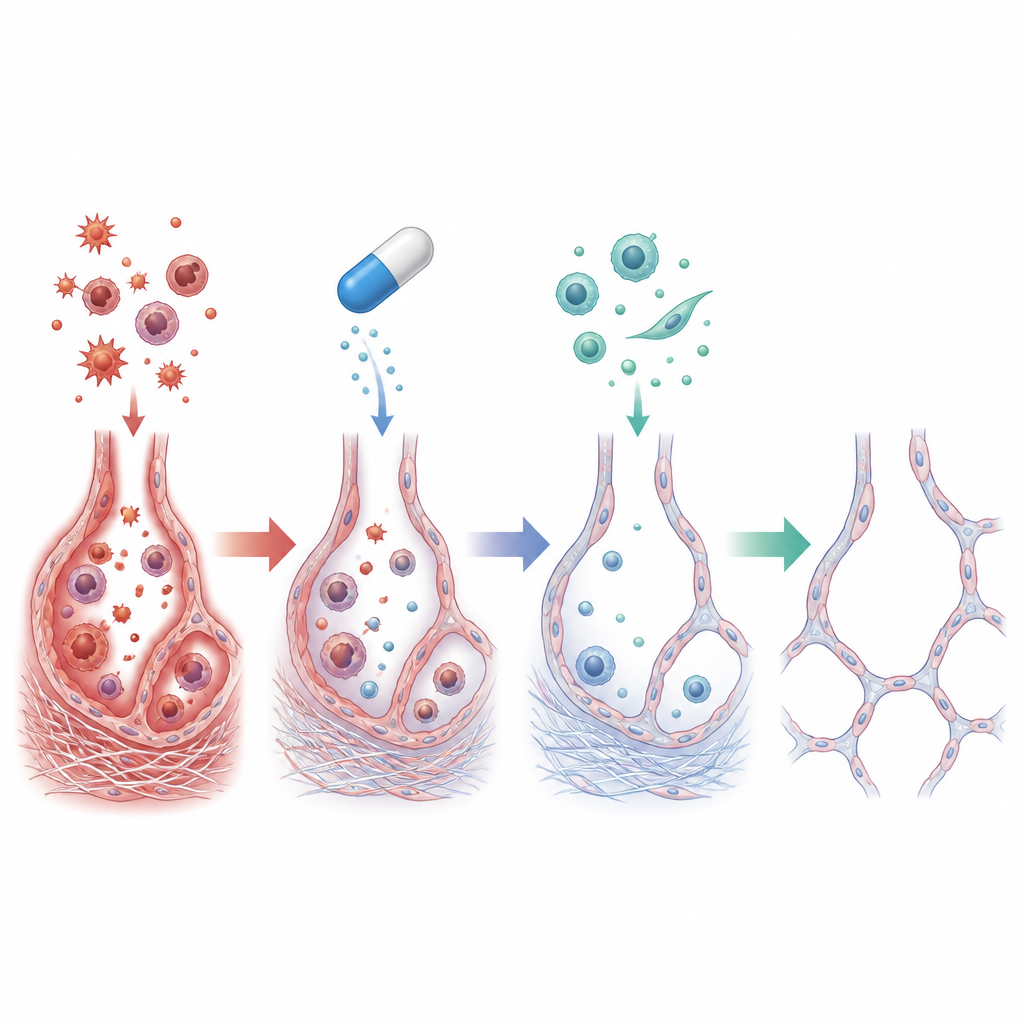
Co działo się w uszkodzonych płucach
U szczurów, które otrzymywały jedynie amiodaron, płuca wykazywały intensywne zapalenie: liczba komórek odpornościowych w płynie dróg oddechowych gwałtownie wzrosła, a poziomy mediatorów zapalenia, takich jak TNF-alfa i IL-1 beta, zwiększyły się wielokrotnie. Odciski chemiczne stresu oksydacyjnego wzrosły — nastąpiło więcej uszkodzeń lipidów i wyczerpanie mechanizmów antyoksydacyjnych. Pod mikroskopem zespół zaobserwował zapadnięte i zdeformowane pęcherzyki otoczone obfitymi depozytami kolagenu. Głębiej w komórkach pojawiły się oznaki, że komórki nabłonkowe wyściełające pęcherzyki zaczynały zachowywać się bardziej jak komórki tworzące blizny — przemiana znana jako przejście nabłonkowo-mezenchymalne, które napędza długotrwałe włóknienie.
Jak cilostazol zmienił obraz choroby
Gdy dodano cilostazol, wiele z tych szkodliwych zmian uległo znacznemu ograniczeniu. Płuca szczurów leczonych ważyły mniej i wyglądały znacznie bliżej normy, z dużo łagodniejszym nagromadzeniem kolagenu i lepiej zachowanymi pęcherzykami. Komórki zapalne i cytokiny spadły w kierunku poziomów kontrolnych, a markery uszkodzeń oksydacyjnych zmalały, podczas gdy naturalne mechanizmy antyoksydacyjne odbiły się. Na poziomie molekularnym cilostazol zwiększył poziom cAMP i podniósł aktywność ochronnych uczestników, takich jak SIRT1 i EPAC1, jednocześnie tłumiąc sygnały związane z bliznowaceniem, w tym TGF-beta1 i wimentynę. Razem te zmiany sugerują, że cilostazol nie tylko uciszył zapalenie i stres oksydacyjny, lecz także przerwał programowanie komórkowe prowadzące do przekształcenia zdrowych komórek wyściółki w komórki produkujące blizny.
Od płuc szczurów do pomysłów na przyszłe terapie
W badaniu stwierdzono, że cilostazol może wyraźnie złagodzić uszkodzenia i bliznowacenie płuc wywołane amiodaronem u szczurów poprzez przywrócenie zdrowszej równowagi sygnałów komórkowych i blokowanie kluczowych kroków prowadzących do trwałego włóknienia. Chociaż wyniki te nie pokazują jeszcze, jak cilostazol sprawdzi się u ludzi, wskazują na praktyczną strategię: ponowne wykorzystanie zatwierdzonego leku w celu ochrony płuc pacjentów polegających na silnych lekach sercowych. Potrzebne będą dalsze badania w różnych modelach i w końcu badania kliniczne, ale rezultaty przekazują jasny komunikat dla czytelników niebędących specjalistami: część szkód wywoływanych przez niezbędne leki może być możliwa do zapobieżenia przez łączenie ich z odpowiednio dobranymi partnerami.
Cytowanie: El-Gammal, M.A., Yousef, E.H., Abd Elhameed, A.G. et al. Cilostazol mitigates amiodarone-induced pulmonary toxicity and fibrosis by regulating the cAMP/TGF-β1 pathway-mediated epithelial-to-mesenchymal transition in rats. Sci Rep 16, 15055 (2026). https://doi.org/10.1038/s41598-026-45341-3
Słowa kluczowe: włóknienie płuc, toksyczność płucna amiodaronu, cilostazol, choroba płuc wywołana lekami, szlak sygnalizacji cAMP