Clear Sky Science · it
Cilostazolo mitiga la tossicità polmonare e la fibrosi indotte dall’amiodarone regolando la transizione epitelio-mesenchimale mediata dalla via cAMP/TGF-β1 nei ratti
Perché questo studio sui polmoni è importante
La fibrosi polmonare è un danno progressivo che causa cicatrici nei polmoni rendendo ogni respiro più faticoso, e può essere scatenata da alcuni farmaci salvavita per il cuore. Questo studio nei ratti esplora se un farmaco già disponibile, il cilostazolo, possa proteggere i polmoni dai danni indotti dall’antiaritmico amiodarone, ampiamente usato. Tracciando sia il danno polmonare visibile sia i segnali chimici nascosti nelle cellule polmonari, i ricercatori pongono una domanda speranzosa: possiamo continuare a usare trattamenti cardiaci essenziali proteggendo meglio i polmoni?
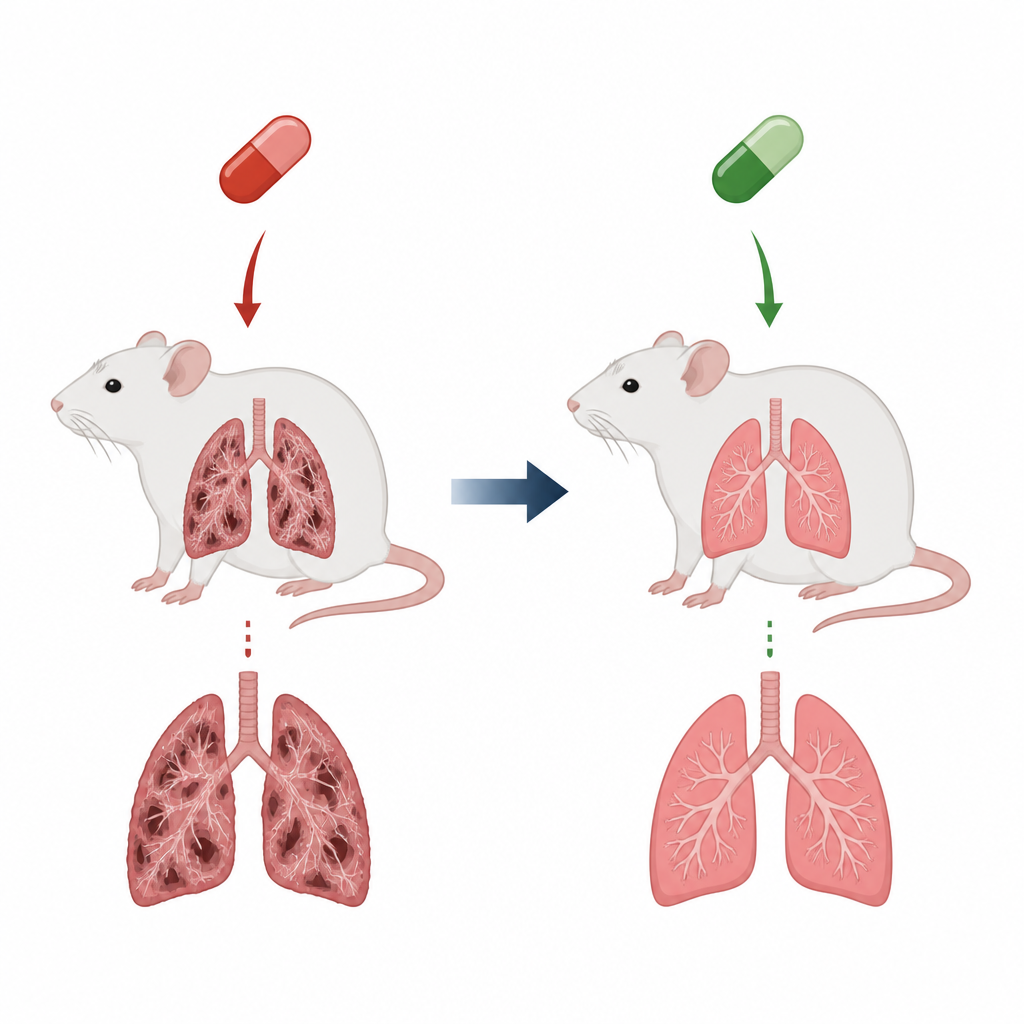
Un farmaco cardiaco con un costo nascosto
L’amiodarone viene prescritto per correggere gravi aritmie cardiache, ma un serio svantaggio è il suo potenziale di danneggiare il tessuto polmonare e portare a fibrosi polmonare. Nella fibrosi, i delicati alveoli che scambiano ossigeno diventano rigidi e cicatrizzati, rendendo la respirazione faticosa e riducendo l’aspettativa di vita. In questo modello murino, dosi giornaliere di amiodarone per diverse settimane hanno riprodotto molte caratteristiche di questa condizione: polmoni più pesanti, vie aeree infiammate piene di cellule immunitarie e spessi depositi di collagene che alteravano la normale struttura polmonare. Questi cambiamenti rispecchiano ciò che i clinici temono nei pazienti che sviluppano cicatrizzazione polmonare legata a farmaci.
Testare un farmaco partner protettivo
Il cilostazolo è una compressa già impiegata per migliorare il flusso sanguigno nelle arterie ostruit e per ridurre il rischio di alcuni tipi di ictus. Agisce in parte aumentando i livelli di una piccola molecola di segnalazione chiamata cAMP, che può attenuare l’infiammazione e limitare la fibrosi nei tessuti. I ricercatori hanno diviso i ratti in tre gruppi: controlli sani, animali che ricevevano solo amiodarone e animali trattati con cilostazolo prima di ogni dose di amiodarone. Hanno quindi raccolto il fluido dalle vie aeree, esaminato fette di tessuto al microscopio e misurato marker chimici di ossidazione, infiammazione e cicatrizzazione per verificare se il cilostazolo potesse attenuare il danno polmonare.
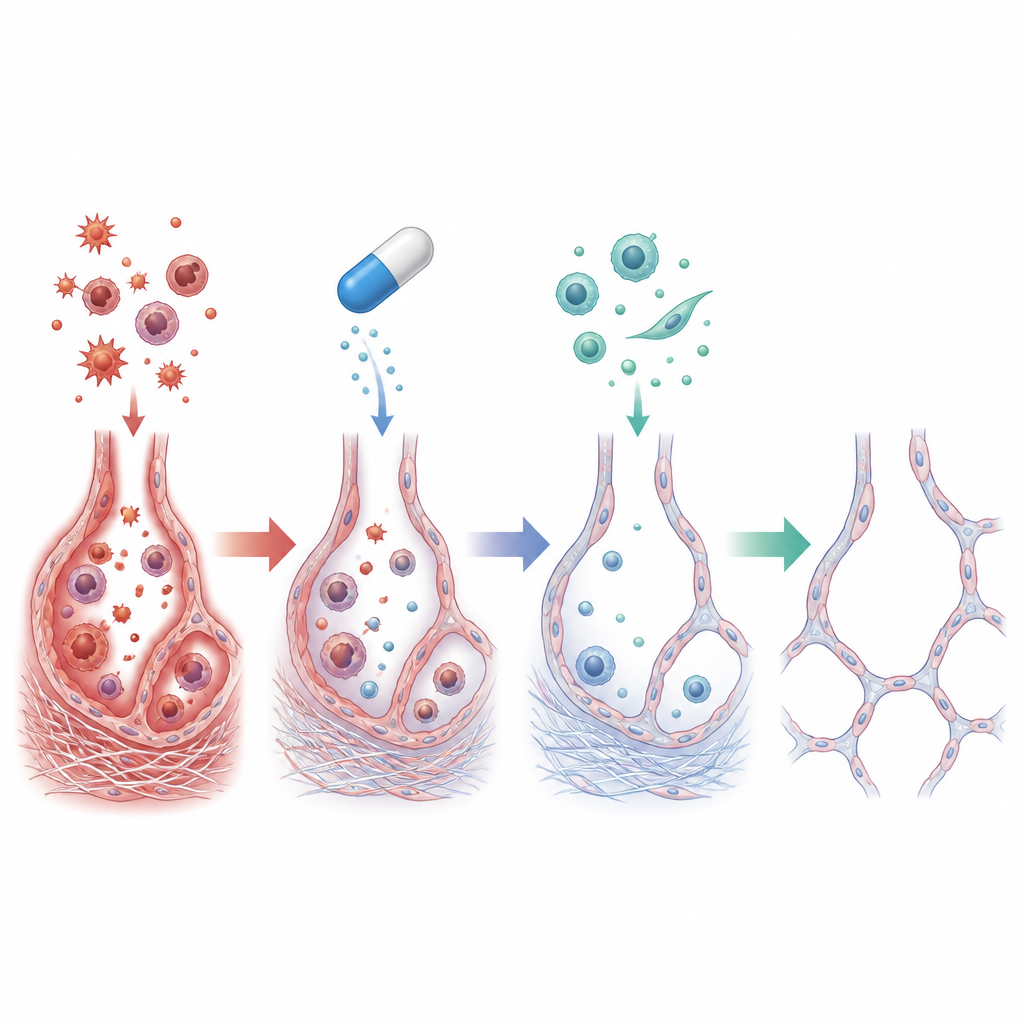
Cosa è successo all’interno dei polmoni danneggiati
Nei ratti che hanno ricevuto solo amiodarone, i polmoni hanno mostrato un’infiammazione intensa: il conteggio delle cellule immunitarie nel liquido delle vie aeree è aumentato drasticamente e i livelli di mediatori infiammatori come TNF-alfa e IL-1 beta sono cresciuti di molto. Sono aumentate le tracce chimiche dello stress ossidativo, con più danni lipidici e difese antiossidanti depauperate. Al microscopio il team ha osservato alveoli collassati e deformati circondati da pesanti depositi di collagene. Più in profondità nelle cellule, c’erano segnali che le cellule epiteliali che rivestono gli alveoli stavano iniziando a comportarsi più come cellule produttrici di cicatrici, un cambiamento noto come transizione epitelio-mesenchimale che guida la fibrosi persistente.
Come il cilostazolo ha modificato il quadro
Quando è stato aggiunto il cilostazolo, molti di questi cambiamenti dannosi sono stati nettamente ridotti. I polmoni dei ratti trattati pesavano meno e apparivano molto più vicini alla norma, con accumuli di collagene molto più lievi e alveoli meglio conservati. Cellule infiammatorie e citochine sono scese verso i livelli dei controlli, e i marker di danno ossidativo sono diminuiti mentre gli antiossidanti naturali sono risaliti. A livello molecolare, il cilostazolo ha aumentato il cAMP e l’attività di fattori protettivi come SIRT1 ed EPAC1, riducendo al contempo segnali associati alla cicatrizzazione, inclusi TGF-beta1 e vimentina. Nel loro insieme, questi cambiamenti suggeriscono che il cilostazolo non solo ha quietato l’infiammazione e lo stress ossidativo, ma ha anche interrotto il riprogrammamento cellulare che trasforma le cellule epiteliali sane in cellule produttrici di cicatrici.
Dai polmoni di ratto a idee per trattamenti futuri
Lo studio conclude che il cilostazolo può attenuare marcatamente il danno polmonare e la fibrosi indotti dall’amiodarone nei ratti ripristinando un equilibrio più sano dei segnali cellulari e bloccando passaggi chiave che portano alla fibrosi permanente. Sebbene questi risultati non dimostrino ancora come il cilostazolo si comporterà negli esseri umani, indicano una strategia pratica: riproporre un farmaco approvato per proteggere i polmoni dei pazienti che dipendono da potenti medicinali cardiaci. Serviranno ulteriori studi in modelli diversi e, infine, trial clinici, ma i risultati offrono un messaggio chiaro per i non specialisti: una parte del danno causato da farmaci essenziali potrebbe essere prevenuta abbinandoli a partner scelti con cura.
Citazione: El-Gammal, M.A., Yousef, E.H., Abd Elhameed, A.G. et al. Cilostazol mitigates amiodarone-induced pulmonary toxicity and fibrosis by regulating the cAMP/TGF-β1 pathway-mediated epithelial-to-mesenchymal transition in rats. Sci Rep 16, 15055 (2026). https://doi.org/10.1038/s41598-026-45341-3
Parole chiave: fibrosi polmonare, tossicità polmonare da amiodarone, cilostazolo, malattia polmonare indotta da farmaci, segnalazione cAMP