Clear Sky Science · he
צילוסטזול מפחית רעילות ריאתית ופיברוזה הנגרמות על-ידי אמיאודרון על-ידי ויסות מעבר אפיתלי-למזנכימלי המתווך על-ידי נתיב cAMP/TGF-β1 בעכברים
מדוע מחקר הריאות הזה חשוב
פיברוזיס ריאתי הוא נזק צלקתי איטי לריאות שמקשה על כל נשימה, והוא יכול להיגרם על-ידי חלק מתרופות הלב שיכולות להציל חיים. מחקר זה בעכברים בוחן האם תרופה קיימת, צילוסטזול, יכולה להגן על הריאות מפגיעה הנגרמת על-ידי תרופת נגד הפרעות קצב הנפוצה אמיאודרון. על-ידי מעקב אחר שני סוגי סימנים — הנזק הגלוי בריאות והאותות הכימיים החבויים בתוך תאי הריאה — החוקרים שואלים שאלה תקווה: האם נוכל לשמור על טיפולי לב חיוניים תוך הגנה טובה יותר על הריאות?
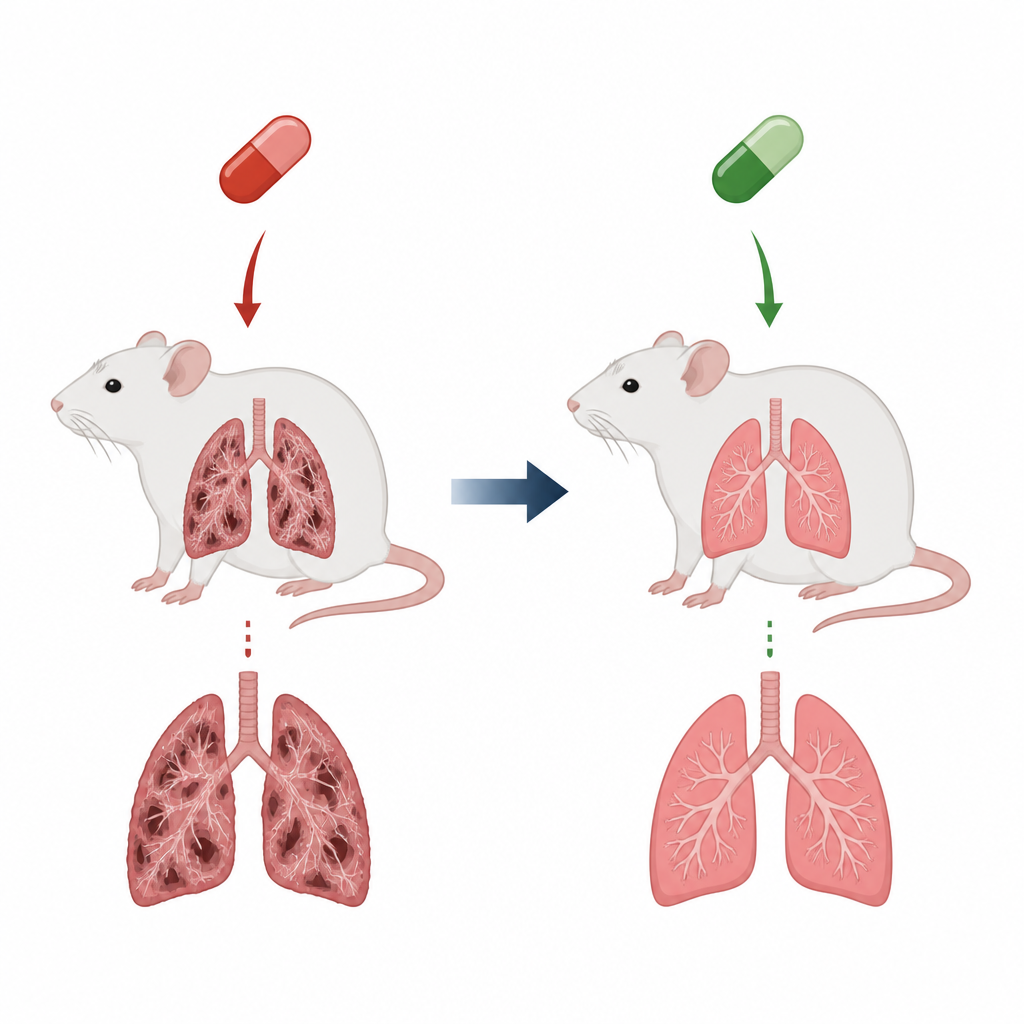
תרופת לב עם עלות נסתרת
אמיאודרון נרשמת לתיקון הפרעות קצב מסכנות חיים, אך חסרון משמעותי הוא היכולת שלה לפגוע ברקמת הריאה ולהוביל לפיברוזיס ריאתי. בפיברוזיס, הנאדיות העדינות שמחליפות חמצן נהיות נוקשות ומצולקות, מה שמקשה על הנשימה ומקצר את תוחלת החיים. במודל העכברים הזה, מינונים יומיים של אמיאודרון למשך מספר שבועות שיחזרו תכונות רבות של מצב זה: ריאות כבדות יותר, דרכי נשימה אנדמיות בדלקת ומלאות תאי מערכת החיסון, ורצועות עבות של קולגן שהעוותו את מבנה הריאה התקין. שינויים אלה משקפים את מה שרופאים חוששים שיקרה בחולים שמפתחים צלקת ריאתית בעקבות תרופה.
מבחן של תרופת שותף מגן
צילוסטזול היא גלולה שכבר משמשת לשיפור זרימת הדם בעורקים חסומים ברגליים ולהפחתת סיכון לסוגים מסוימים של שבץ. חלק מפעולתה הוא על ידי העלאת רמות מולקולת איתות קטנה הנקראת cAMP, שיכולה להרגיע דלקת ולהגביל הצטלקות ברקמות. החוקרים חילקו את העכברים לשלוש קבוצות: בקרה בריאה, בעלי חיים שקיבלו אמיאודרון בלבד, ובעלי חיים שקיבלו צילוסטזול לפני כל מנה של אמיאודרון. הם אספו אז נוזל מהריאות, בחנו פרוסות רקמה במיקרוסקופ ומדדו סימני חמצון, דלקת והצטלקות כדי לבדוק האם צילוסטזול מסוגל להחליש את נזק הריאה.
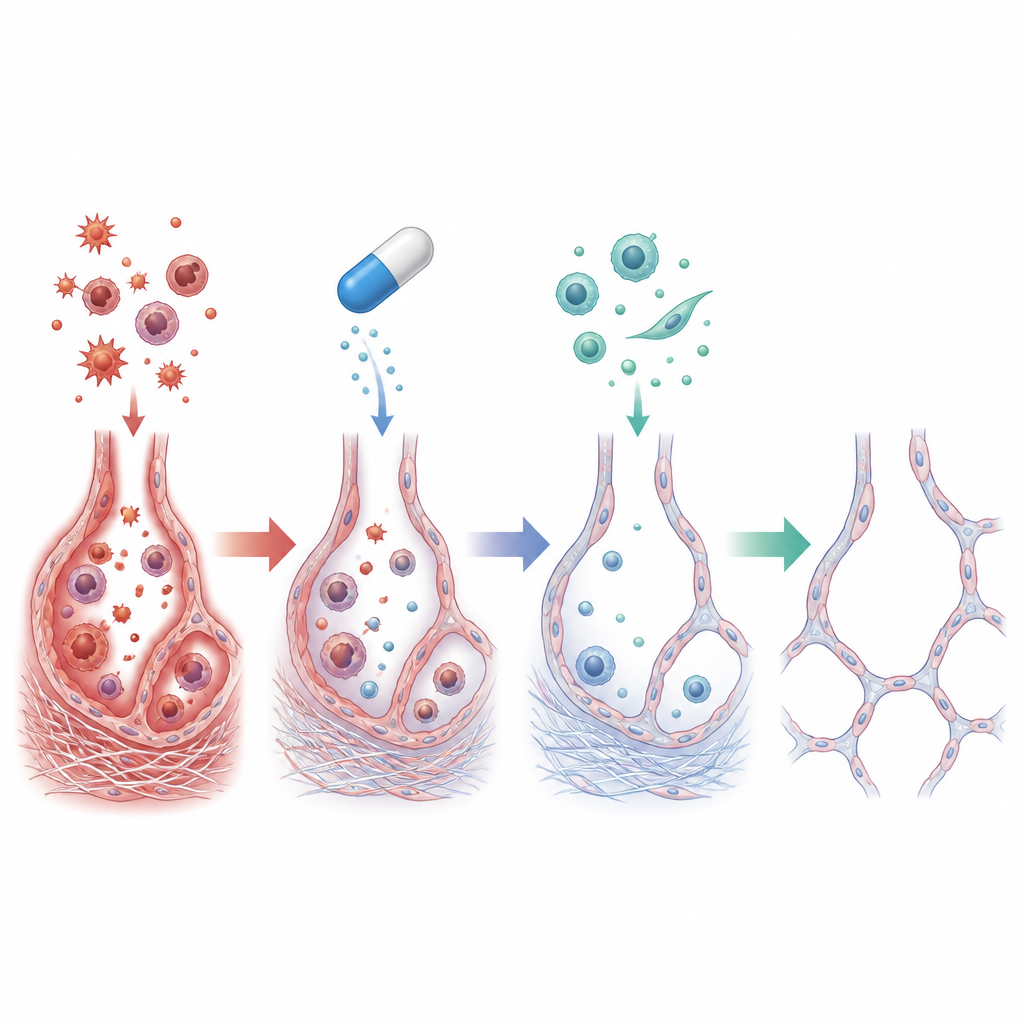
מה התרחש בתוך הריאות הפגועות
בעכברים שקיבלו רק אמיאודרון, הריאות הראו דלקת עזה: ספירת תאי מערכת החיסון בנוזל דרכי הנשימה קפצה, ורמות של שליחים דלקתיים כגון TNF-אלפא ו-IL-1 ביתא עלו כמה מונים. טביעות כימיות של מתח חמצוני עלו, עם יותר נזק לשומנים והגנה אנטי-חמצונית מותשת. תחת המיקרוסקופ נראו נאדיות שקועות ומעוותות המוקפות בהפקדות קולגן כבדות. בתוך התאים, נצפו סימנים שהתאים האפיתליים שמרפדים את הנאדיות החלו להתנהג יותר כמו תאים שיוצרים צלקת — שינוי הידוע כמעבר אפיתלי-למזנכימלי שמניע פיברוזיס מתמשך.
כיצד צילוסטזול שינה את התמונה
כאשר הוסיפו צילוסטזול, רבים מהשינויים המזיקים האלה הופחתו באופן בולט. ריאות מהחיונים המטופלים היו קלות יותר ונראו קרובות יותר לנורמה, עם הצטברות קולגן מתונה בהרבה ונאדיות משומרות טוב יותר. תאי דלקת וציטוקינים ירדו לעבר רמות הבקרה, וסימני נזק חמצוני ירדו בעוד שהנוגדי חמצון הטבעיים התאוששו. ברמה המולקולרית, צילוסטזול הגביר cAMP והגביר פעילות של שחקנים מגן כגון SIRT1 ו-EPAC1, תוך דיכוי אותות המקושרים להצטלקות, כולל TGF-beta1 וווימנטין. יחד, השינויים הללו מצביעים על כך שצילוסטזול לא רק השקט דלקת ומתח חמצוני אלא גם פסק את התכנות התאית שהופכת תאים מפרישי שכבה בריאה לתאים שמפיקים צלקת.
ממריאות של עכברים לרעיונות טיפוליים עתידיים
המסקנה של המחקר היא שצילוסטזול יכול לרכך במידה ניכרת את פגיעה הריאה וההצטלקות הנגרמות על-ידי אמיאודרון בעכברים על-ידי שיקום איזון בריא יותר של אותות תאיים וחסימת שלבים מרכזיים שמובילים לפיברוזיס קבוע. בעוד שהתוצאות הללו אינן מוכיחות עדיין כיצד צילוסטזול יתנהג בבני אדם, הן מצביעות על אסטרטגיה מעשית: שימוש מחודש בתרופה מאושרת כדי להגן על ריאות של חולים שתלויים בתרופות לב עוצמתיות. נדרשת עבודה נוספת במודלים שונים ובסופו של דבר ניסויים קליניים, אך הממצאים מספקים מסר ברור לקהל הרחב: חלק מהנזק הנגרם על-ידי תרופות חיוניות עשוי להיות נמנע על-ידי צירופן לתרופות שותפות נבחרות בקפידה.
ציטוט: El-Gammal, M.A., Yousef, E.H., Abd Elhameed, A.G. et al. Cilostazol mitigates amiodarone-induced pulmonary toxicity and fibrosis by regulating the cAMP/TGF-β1 pathway-mediated epithelial-to-mesenchymal transition in rats. Sci Rep 16, 15055 (2026). https://doi.org/10.1038/s41598-026-45341-3
מילות מפתח: פיברוזיס ריאתי, רעילות ריאות כתוצאה מאמיאודרון, צילוסטזול, מחלות ריאה הנגרמות מתרופות, איתות cAMP