Clear Sky Science · sv
Mångsidig och portabel Cas12a‑baserad detektion av markörer för antibiotikaresistens
Varför det är viktigt att följa osynliga mikrober
Antibiotikaresistens låter abstrakt tills en rutininfektion inte längre svarar på läkemedel. Bakterier som kan stå emot våra preparat dyker upp inte bara på sjukhus, utan också på gårdar och i floder och jordar. För att ligga steget före detta hot behöver forskare snabba, prisvärda metoder för att upptäcka de genetiska varnande tecknen för resistens där de än uppträder. Denna artikel beskriver en ny laboratorieverktygslåda, kallad C12a, som använder CRISPR‑genklippningsteknik för att detektera viktiga resistensgener i bakterier från människor, djur och miljö.
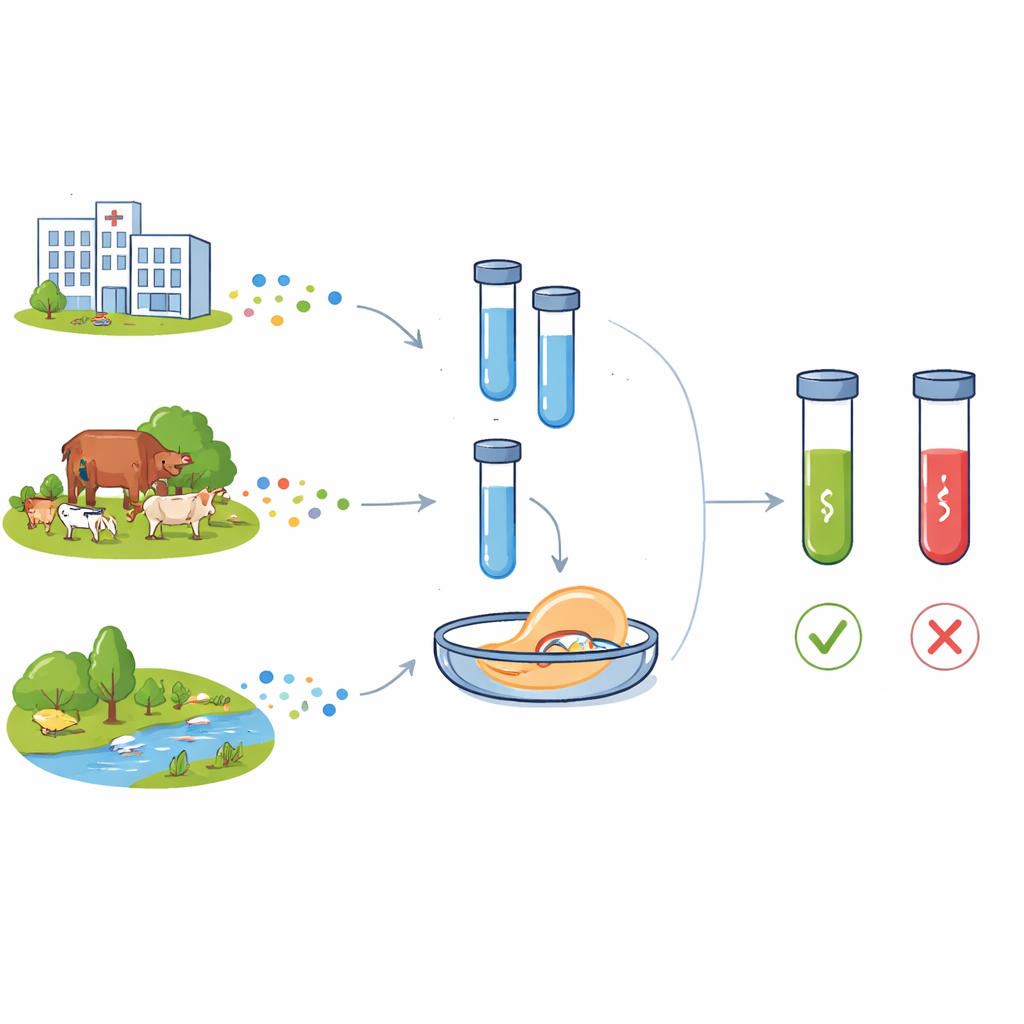
Ett växande problem som sträcker sig bortom sjukhusets väggar
Moderna antibiotika förändrade medicinen och gjorde tidigare dödliga infektioner behandlingsbara och möjliggjorde komplex kirurgi och intensivvård. Men omfattande användning inom humanvård, djurhållning och dåligt renat avloppsvatten har påskyndat utvecklingen och spridningen av antimikrobiell resistens. Två resistensgener är särskilt oroande: blaCTX‑M‑15, som skyddar bakterier mot en bred klass beta‑laktamantibiotika som används hos människor, och floR, som ger skydd mot amfenikolpreparat som används i stor utsträckning hos djur. Båda generna förekommer nu i bakterier från sjukhus, samhällen, gårdar och vatten och rör sig ofta mellan arter på rörliga genetiska element. Ett annat genetiskt element, klass 1‑integron (spåras via intI1‑genen), bär ofta kluster av resistensgener och ses som en markör för stark mänsklig påverkan på mikrobiella ekosystem.
Att göra CRISPR till en resistensdetektor
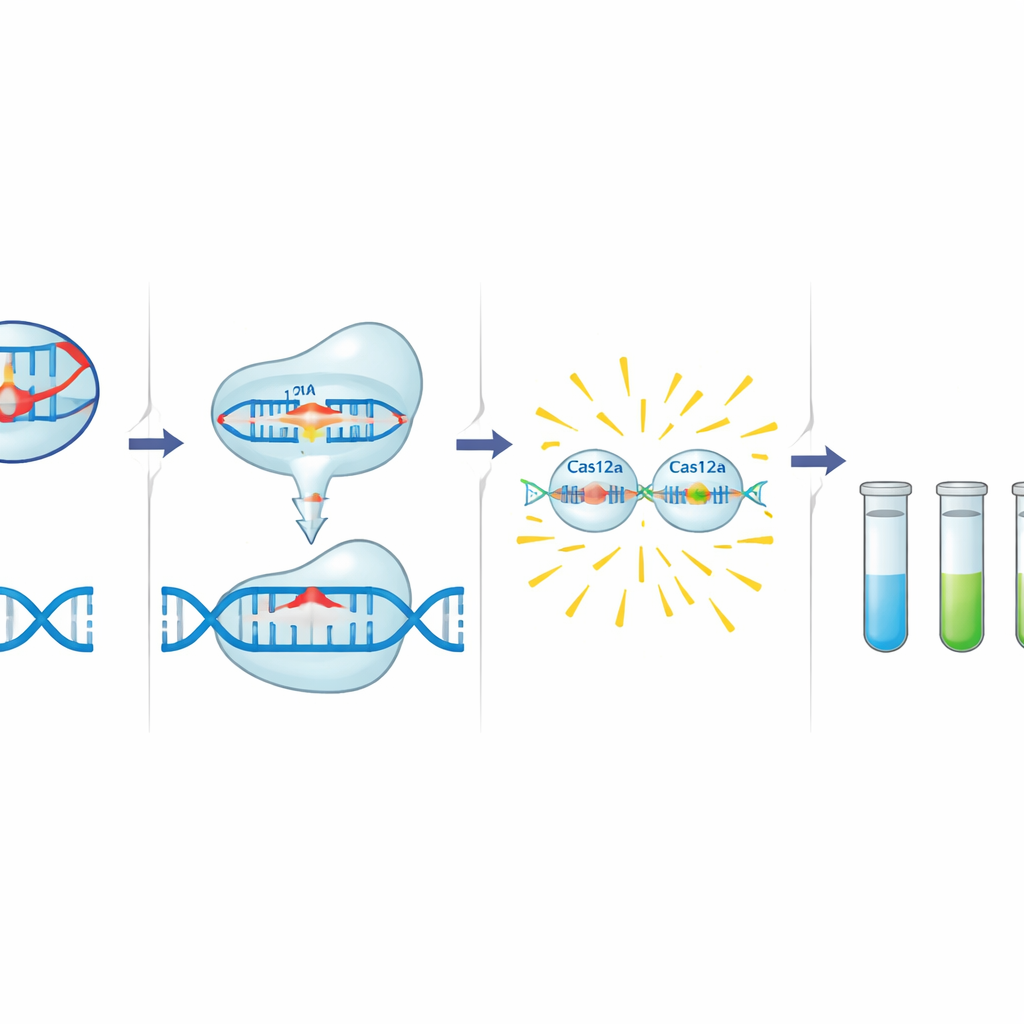
C12a‑verktygslådan bygger på Cas12a, ett CRISPR‑associerat enzym som kan programmeras med en kort guide‑RNA för att känna igen en specifik DNA‑sekvens. När Cas12a hittar sitt mål intill ett kort trigger‑motiv klipper det först det målet och börjar därefter snabbt klyva närliggande enkelsträngat DNA. Författarna utnyttjar detta beteende genom att tillsätta en liten DNA‑probe märkt med en fluorescerande färg och en dämpare. I närvaro av en resistensgen skärs proben av den aktiverade Cas12a och frigör en stark signal. Före denna detektionssteg amplifieras en liten region av målgenen med standard‑PCR, en region som inkluderar både Cas12a‑triggern och guidens bindningsställe, vilket ger ett andra lager av specificitet. Teamet designade och optimerade guider och primrar för tre mål: blaCTX‑M‑15 (C12abCTX), floR (C12aFLO) och klass 1‑integronens integrasgen intI1 (C12aINT).
Hur känslig och tillförlitlig är verktygslådan?
För att bedöma prestanda mätte forskarna hur små mängder DNA systemet säkert kunde detektera. Med rena fragment av målgenerna upptäckte C12abCTX och C12aFLO koncentrationer så låga som 70 respektive 50 attomolar—mycket lägre än vad som kan ses genom att bara köra PCR‑produkter på gel. När de testade verkliga bakteriekulturer kunde assayen detektera ungefär 77 celler per milliliter för blaCTX‑M‑15 och 173 celler per milliliter för floR. I samlingar av Escherichia coli från barns avföringsprover stämde resultaten från C12a‑verktygslådan överens med standardtester för antibiotikakänslighet och, där sådana fanns, med helgenomsekvensering: prover som genetiskt var positiva för resistensgenerna gav starka fluorescenssignaler medan negativa prover höll sig på bakgrundsnivåer.
Koppla resistensgener till större risk
Författarna undersökte också om deras verktyg kunde flagga bakterier som bär många resistensegenskaper samtidigt. Med C12aINT sökte de i samma isolat efter klass 1‑integronens integrasgen. De fann intI1 i nästan alla prov som bar antingen blaCTX‑M‑15 eller floR. Genomanalyser visade att dessa integroner ofta hyste kluster av gener som ger resistens mot flera antibiotikafamiljer och till och med mot desinfektionsmedel, även om studiens huvudmålgener oftast var lokaliserade andra ställen i genomet. Detta stöder idén att spårning av intI1 kan fungera som en praktisk proxy för människodrivet antibiotikatryck och multiresistens, samtidigt som det understryker behovet av att direkt testa specifika högriskgener.
Från högteknologiskt labb till fältkit
En viktig styrka hos C12a‑verktygslådan är dess anpassningsbarhet till olika laboratorieförutsättningar. I fullt utrustade miljöer mättes reaktionerna med en mikrotiterplatteläsare, vilket gav kvantitativa kurvor över tid. I enklare laboratorier kunde samma reaktioner ses med en grundläggande blåljustransilluminator, där bara rör som innehöll resistensgener lyste upp. För portabel fälttestning ersatte teamet fluorescensavläsningen med lateralflödesremsor, liknande formatet på ett graviditetstest, som visade band endast när CRISPR‑reaktionen aktiverats. I dessa uppställningar och för olika provtyper—including total DNA direkt från feces—identifierades närvaro eller frånvaro av målgenerna konsekvent, med endast måttliga förluster i känslighet i lågresurslägen.
Vad detta betyder för kampen mot resistenta infektioner
Tillsammans presenterar resultaten C12a som en mångsidig proof‑of‑concept‑plattform för att bevaka hur antibiotikaresistensgener rör sig genom människor, djur och miljö. Metoden är ännu inte en klinisk diagnostik och den detekterar genetisk potential för resistens snarare än hur en specifik infektion kommer att svara på behandling. Ändå gör dess snabbhet, låga detektionsgränser och kompatibilitet med både avancerade instrument och enkla fältverktyg den till en lovande byggsten för framtida övervakningssystem. Genom att göra det enklare att upptäcka resistenshotspots på sjukhus, gårdar och i vattendrag kan CRISPR‑baserade verktygslådor som C12a hjälpa folkhälsoansvariga och forskare att reagera snabbare och utforma smartare strategier för att bevara effekten av våra återstående antibiotika.
Citering: Vargas-Reyes, M., Alcántara, R., Alfonsi, S. et al. Versatile and portable Cas12a-mediated detection of antibiotic resistance markers. Sci Rep 16, 11509 (2026). https://doi.org/10.1038/s41598-026-42073-2
Nyckelord: antimikrobiell resistens, CRISPR‑diagnostik, Cas12a, antibiotikaresistensgener, One Health‑övervakning