Clear Sky Science · es
Detección versátil y portátil mediada por Cas12a de marcadores de resistencia a antibióticos
Por qué importa rastrear gérmenes invisibles
La resistencia a los antibióticos suena abstracta hasta que una infección común deja de responder a los medicamentos. Las bacterias que eluden nuestros fármacos emergen no solo en hospitales, sino también en granjas, ríos y suelos. Para adelantarse a esta amenaza, los científicos necesitan métodos rápidos y asequibles para detectar las señales genéticas de resistencia allí donde aparezcan. Este artículo describe una nueva caja de herramientas de laboratorio, denominada C12a, que utiliza la tecnología CRISPR de corte de genes para detectar genes clave de resistencia en bacterias provenientes de personas, animales y el medio ambiente.
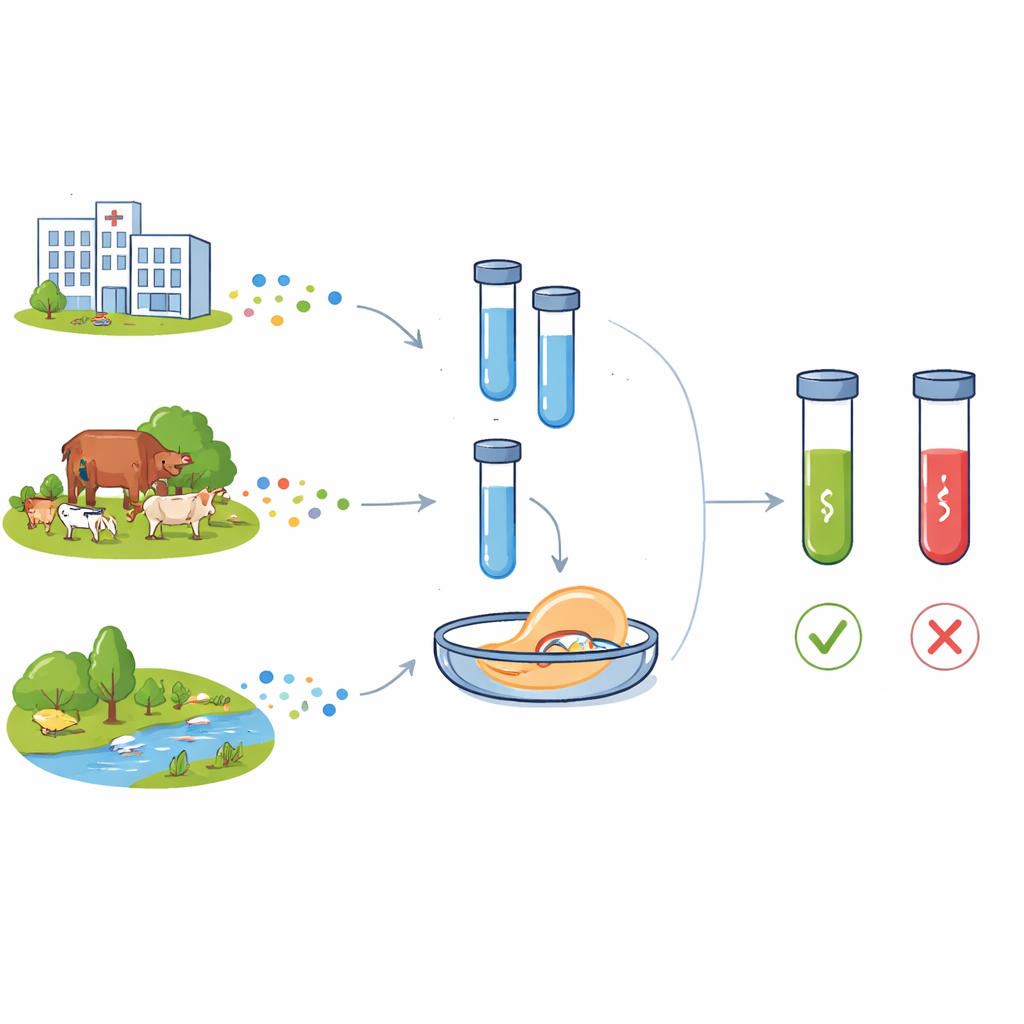
Un problema creciente que traspasa las paredes hospitalarias
Los antibióticos modernos transformaron la medicina, convirtiendo infecciones que antes eran mortales en enfermedades tratables y posibilitando cirugías complejas y cuidados intensivos. Pero el uso intensivo en la medicina humana, la producción ganadera y los efluentes mal tratados ha acelerado la evolución y la propagación de la resistencia antimicrobiana. Dos genes de resistencia son especialmente preocupantes: blaCTX-M-15, que protege a las bacterias frente a una amplia clase de antibióticos beta‑lactámicos usados en humanos, y floR, que confiere resistencia a los amfenicoles ampliamente empleados en animales. Ambos genes aparecen ahora en bacterias de hospitales, comunidades, granjas y aguas, a menudo moviéndose entre especies en elementos genéticos móviles. Otro elemento genético, el integrón de clase 1 (seguido mediante el gen intI1), suele portar agrupaciones de genes de resistencia y se considera un marcador de fuerte impacto humano en los ecosistemas microbianos.
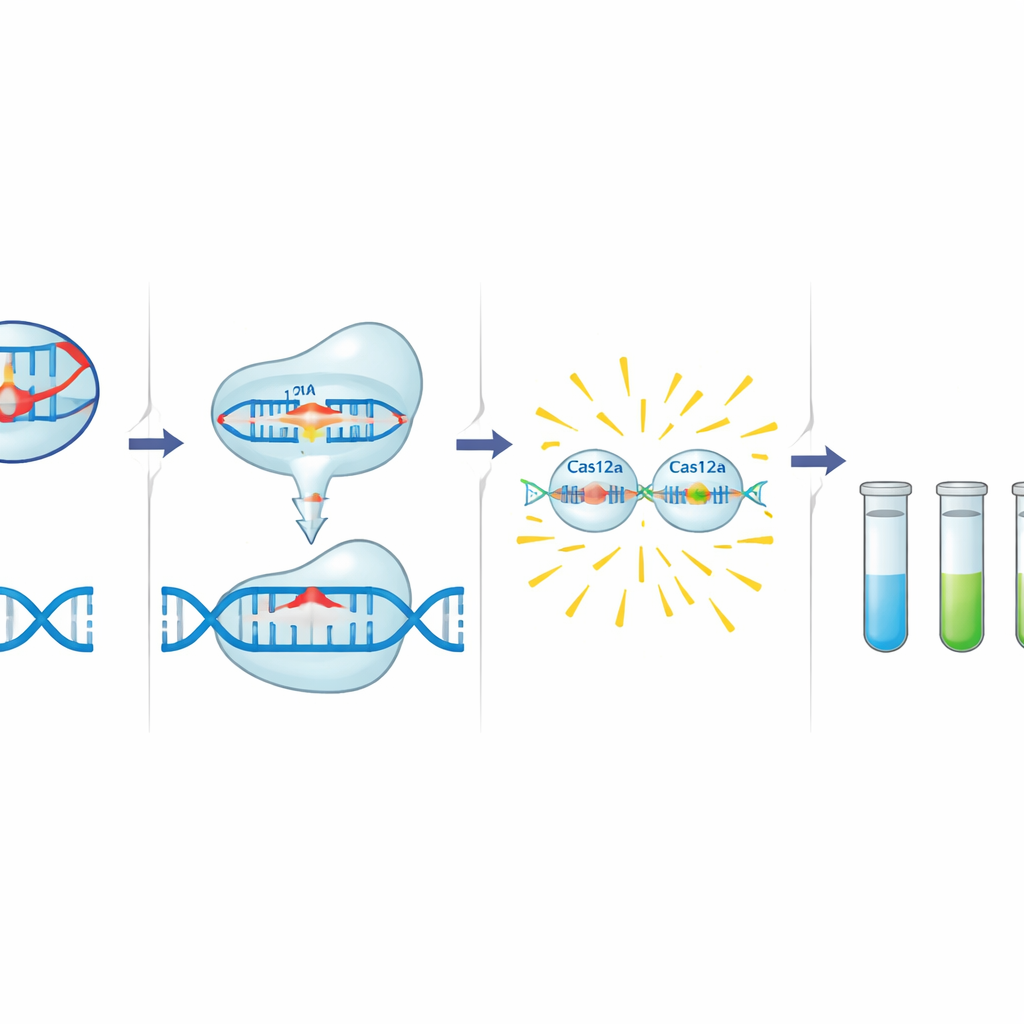
Convertir CRISPR en un detector de resistencia
La caja de herramientas C12a se basa en Cas12a, una enzima asociada a CRISPR que puede programarse con un ARN guía corto para reconocer una secuencia específica de ADN. Cuando Cas12a encuentra su objetivo junto a un pequeño motivo iniciador, primero corta ese ADN y luego comienza a degradar rápidamente ADN monocatenario circundante. Los autores aprovechan este comportamiento añadiendo una sonda de ADN diminuta marcada con un tinte fluorescente y un apagador. En presencia de un gen de resistencia, Cas12a activada corta la sonda y libera una señal luminosa. Antes de este paso de detección, una reacción PCR estándar amplifica una pequeña región del gen objetivo que incluye tanto el motivo iniciador de Cas12a como el sitio de unión del guía, añadiendo una segunda capa de especificidad. El equipo diseñó y optimizó guías y cebadores para tres dianas: blaCTX-M-15 (C12abCTX), floR (C12aFLO) y el gen integrasa del integrón de clase 1 intI1 (C12aINT).
¿Qué tan sensible y fiable es la caja de herramientas?
Para evaluar el rendimiento, los investigadores midieron la mínima cantidad de ADN que el sistema podía detectar de forma fiable. Usando fragmentos purificados de los genes objetivo, C12abCTX y C12aFLO detectaron concentraciones tan bajas como 70 y 50 attomolar, respectivamente—muy por debajo de lo que se observa al simplemente visualizar productos de PCR en un gel. Cuando probaron cultivos bacterianos reales, los ensayos pudieron detectar alrededor de 77 células por mililitro para blaCTX-M-15 y 173 células por mililitro para floR. En colecciones de Escherichia coli procedentes de muestras de heces infantiles, los resultados de la caja C12a coincidieron con las pruebas estándar de susceptibilidad a antibióticos y, cuando hubo datos disponibles, con el secuenciamiento del genoma completo: las muestras genéticamente positivas para los genes de resistencia dieron señales fluorescentes fuertes, mientras que las muestras negativas se mantuvieron en niveles de fondo.
Vincular genes de resistencia con un riesgo más amplio
Los autores también exploraron si sus herramientas podían identificar bacterias que portan múltiples rasgos de resistencia a la vez. Usando C12aINT, buscaron el gen integrasa del integrón de clase 1 en los mismos aislados. Encontraron intI1 en casi todas las muestras que llevaban blaCTX-M-15 o floR. Los análisis genómicos mostraron que estos integrones a menudo alojaban agrupaciones de genes que confieren resistencia a varias familias de antibióticos e incluso a desinfectantes, aunque los genes objetivo principales de este estudio solían ubicarse en otras partes del genoma. Esto respalda la idea de que rastrear intI1 puede servir como un proxy conveniente del esfuerzo humano sobre la presión antibiótica y la resistencia multidrogas, aunque subraya la necesidad de probar directamente genes específicos de alto riesgo.
Del laboratorio de alta tecnología al kit de campo
Una fortaleza clave de la caja C12a es su adaptabilidad a distintas realidades de laboratorio. En un entorno completamente equipado, las reacciones se midieron con un lector de microplacas, produciendo curvas cuantitativas a lo largo del tiempo. En laboratorios más sencillos, las mismas reacciones podían visualizarse con un transiluminador de luz azul básico, donde solo los tubos que contenían genes de resistencia brillaban. Para pruebas portátiles en el lugar, el equipo reemplazó la lectura de fluorescencia por tiras de flujo lateral, similares a una prueba de embarazo, que mostraron bandas solo cuando la reacción CRISPR se había activado. A través de estos formatos y tipos de muestra —incluida la ADN total directamente de heces—, la presencia o ausencia de los genes objetivo se identificó de forma consistente, con solo pérdidas modestas de sensibilidad en los modos de recursos limitados.
Qué significa esto para combatir las infecciones resistentes
En conjunto, los resultados presentan a C12a como una plataforma de prueba de concepto versátil para vigilar cómo se desplazan los genes de resistencia a los antibióticos entre personas, animales y el medio ambiente. El enfoque aún no es un diagnóstico clínico, y detecta el potencial genético de resistencia más que la respuesta que dará una infección específica al tratamiento. Aun así, su rapidez, bajos límites de detección y compatibilidad tanto con instrumentos sofisticados como con herramientas sencillas de campo lo convierten en un bloque de construcción prometedor para futuros sistemas de vigilancia. Al facilitar la detección de puntos críticos de resistencia en hospitales, granjas y vías fluviales, las cajas de herramientas basadas en CRISPR como C12a podrían ayudar a los responsables de salud pública e investigadores a reaccionar más rápido y diseñar estrategias más inteligentes para preservar la eficacia de nuestros antibióticos restantes.
Cita: Vargas-Reyes, M., Alcántara, R., Alfonsi, S. et al. Versatile and portable Cas12a-mediated detection of antibiotic resistance markers. Sci Rep 16, 11509 (2026). https://doi.org/10.1038/s41598-026-42073-2
Palabras clave: resistencia antimicrobiana, diagnósticos CRISPR, Cas12a, genes de resistencia a antibióticos, vigilancia One Health