Clear Sky Science · ru
Универсальный и портативный метод на базе Cas12a для обнаружения маркеров резистентности к антибиотикам
Почему важно отслеживать невидимые микробы
Понятие «резистентность к антибиотикам» кажется абстрактным, пока обычная инфекция перестаёт реагировать на лечение. Бактерии, способные противостоять нашим препаратам, появляются не только в больницах, но и на фермах, в реках и почвах. Чтобы опережать эту угрозу, учёным нужны быстрые и доступные способы выявлять генетические признаки резистентности там, где они возникают. В этой статье описан новый лабораторный набор инструментов под названием C12a, который использует технологию CRISPR для обнаружения ключевых генов резистентности в бактериях от людей, животных и окружающей среды.
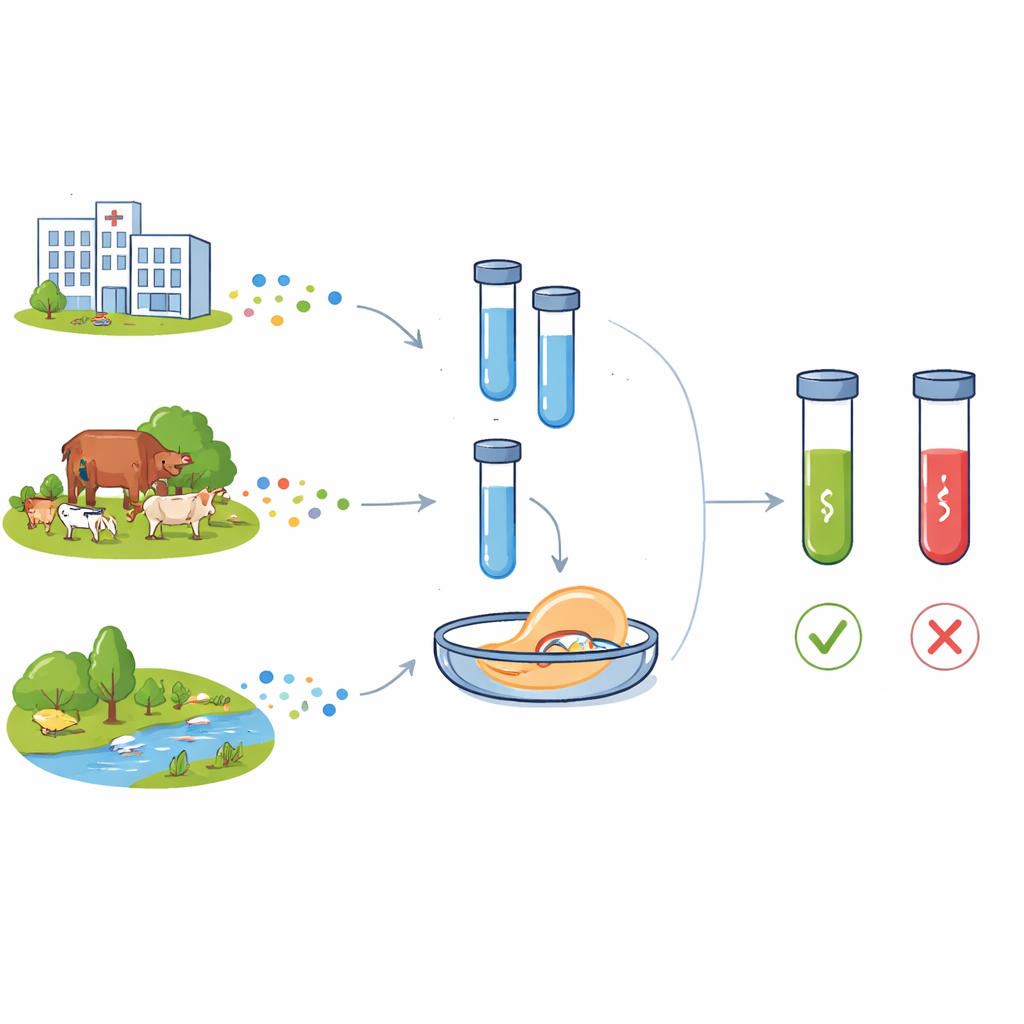
Растущая проблема, выходящая за пределы больниц
Современные антибиотики преобразили медицину, превратив ранее смертельные инфекции в излечимые болезни и позволив проводить сложные операции и интенсивную терапию. Но широкое применение в медицине, животноводстве и недостаточно очищенные стоки ускорили эволюцию и распространение антимикробной резистентности. Особенно тревожны два гена резистентности: blaCTX-M-15, который защищает бактерии от широкого класса бета‑лактамных антибиотиков, применяемых у людей, и floR, обеспечивающий защиту от амфеникольных препаратов, широко используемых у животных. Оба гена теперь встречаются в бактериях из больниц, сообществ, хозяйств и водоёмов, часто переходя между видами на мобильных генетических элементах. Ещё один элемент — интегрон класса 1 (отслеживаемый по гену intI1) — часто несёт кластеры генов резистентности и считается маркером сильного антропогенного воздействия на микробные экосистемы.
Преобразование CRISPR в детектор резистентности
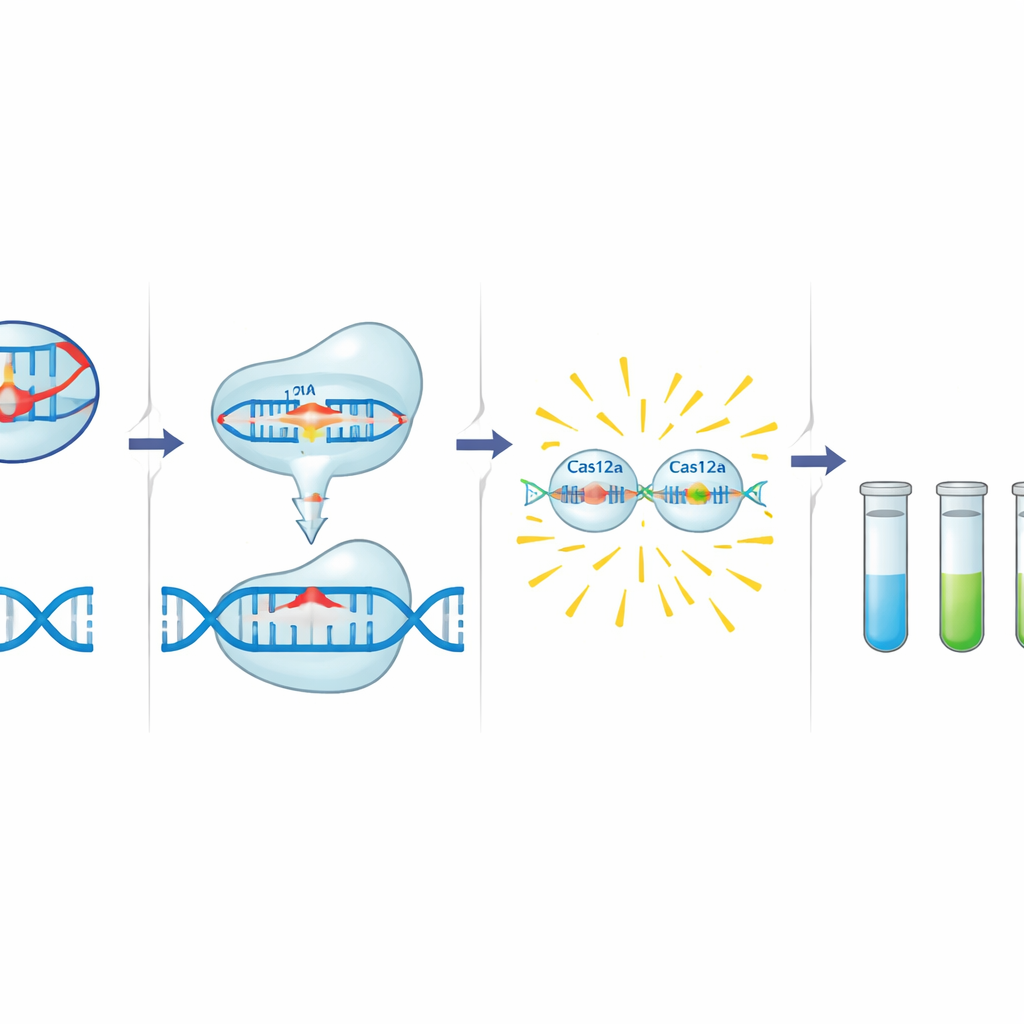
Набор C12a основан на Cas12a — ферменте, ассоциированном с CRISPR, который можно запрограммировать короткой направляющей РНК для распознавания определённой последовательности ДНК. Когда Cas12a находит мишень рядом с коротким сигнальным мотивом, он сначала разрезает эту ДНК, а затем начинает быстро расщеплять соседнюю одноцепочечную ДНК. Авторы используют это поведение, добавляя крошечный ДНК-зонд, меченый флуоресцентным красителем и тушителем. В присутствии гена резистентности активированный Cas12a расщепляет зонд и высвобождает яркий сигнал. Перед этим этапом детекции стандартная ПЦР усиливает небольшой участок целевого гена, который включает и сигнальный мотив Cas12a, и сайт связывания направляющей, что добавляет второй уровень специфичности. Команда разработала и оптимизировала направляющие и праймеры для трёх целей: blaCTX-M-15 (C12abCTX), floR (C12aFLO) и интегразного гена интегрона класса 1 intI1 (C12aINT).
Насколько чувствителен и надёжен набор?
Для оценки эффективности исследователи измеряли, какое минимальное количество ДНК система способна надёжно обнаруживать. При использовании очищенных фрагментов целевых генов C12abCTX и C12aFLO обнаруживали концентрации до 70 и 50 аттомоляр соответственно — значительно ниже порога, видимого при обычном анализе продуктов ПЦР на геле. При тестировании реальных бактериальных культур анализы могли обнаруживать примерно 77 клеток на миллилитр для blaCTX-M-15 и 173 клетки на миллилитр для floR. В коллекциях Escherichia coli из детских образцов кала результаты набора C12a совпадали со стандартными тестами на чувствительность к антибиотикам и, где были доступны, с анализом целого генома: образцы, генетически позитивные по генам резистентности, давали сильные флуоресцентные сигналы, тогда как негативные образцы оставались на уровне фонового сигнала.
Связывание генов резистентности с более широким риском
Авторы также проверяли, могут ли их инструменты выявлять бактерии, несущие множество признаков резистентности одновременно. С помощью C12aINT они искали в тех же изолятах ген интегразы интегрона класса 1. Они обнаружили intI1 почти во всех образцах, содержащих либо blaCTX-M-15, либо floR. Анализы геномов показали, что эти интегроны часто содержат кластеры генов, обеспечивающих резистентность к нескольким классам антибиотиков и даже к дезинфектантам, хотя основные исследованные в этой работе целевые гены обычно располагались в других местах генома. Это поддерживает идею, что отслеживание intI1 может служить удобным прокси маркером антропогенного антибиотического давления и многопрепаратной резистентности, но при этом подчёркивает необходимость прямого тестирования на конкретные гены высокого риска.
От высокотехнологичной лаборатории к полевому набору
Ключевая сильная сторона набора C12a — его адаптируемость к разным лабораторным условиям. В полностью оснащённых лабораториях реакции измеряли на микропланшетном ридере, получая количественные кривые во времени. В более простых лабораториях те же реакции можно было визуализировать на базовом трансиллюминаторе с синим светом, где светились только пробирки с генами резистентности. Для переносного полевого тестирования команда заменила флуоресцентный считыватель на экспресс‑полоски наподобие теста на беременность, которые показывали полосы только при активации реакции CRISPR. Во всех этих форматах и с разными типами образцов — включая общую ДНК непосредственно из фекалий — присутствие или отсутствие целевых генов определялось последовательно, с лишь умеренным снижением чувствительности в режимах для ресурсов с ограничениями.
Что это значит для борьбы с устойчивыми инфекциями
В совокупности результаты представляют C12a как универсальную платформу proof‑of‑concept для мониторинга передвижения генов резистентности через людей, животных и окружающую среду. Подход пока не является клиническим диагностическим тестом и выявляет генетический потенциал резистентности, а не то, как конкретная инфекция отреагирует на лечение. Тем не менее его скорость, низкие пределы обнаружения и совместимость как с высокоточным оборудованием, так и с простыми полевыми средствами делают его перспективным компонентом будущих систем надзора. Упрощая выявление очагов резистентности в больницах, на фермах и в водоёмах, CRISPR‑основанные наборы вроде C12a могут помочь органам общественного здравоохранения и исследователям быстрее реагировать и разрабатывать более продуманные стратегии по сохранению эффективности оставшихся антибиотиков.
Цитирование: Vargas-Reyes, M., Alcántara, R., Alfonsi, S. et al. Versatile and portable Cas12a-mediated detection of antibiotic resistance markers. Sci Rep 16, 11509 (2026). https://doi.org/10.1038/s41598-026-42073-2
Ключевые слова: антибактериальная резистентность, диагностика CRISPR, Cas12a, гены устойчивости к антибиотикам, надзор One Health