Clear Sky Science · it
Rilevamento versatile e portatile mediato da Cas12a di marcatori di resistenza agli antibiotici
Perché è importante tracciare i germi invisibili
La resistenza agli antibiotici sembra un concetto astratto finché un’infezione di routine non risponde più ai farmaci. I batteri che ignorano le nostre terapie emergono non solo negli ospedali, ma anche nelle fattorie e nei fiumi e nei terreni. Per restare davanti a questa minaccia, gli scienziati hanno bisogno di modi rapidi e accessibili per individuare i segnali genetici di resistenza ovunque compaiano. Questo articolo descrive una nuova cassetta degli attrezzi di laboratorio, chiamata C12a, che sfrutta la tecnologia CRISPR per rilevare geni chiave di resistenza in batteri provenienti da persone, animali e ambiente.
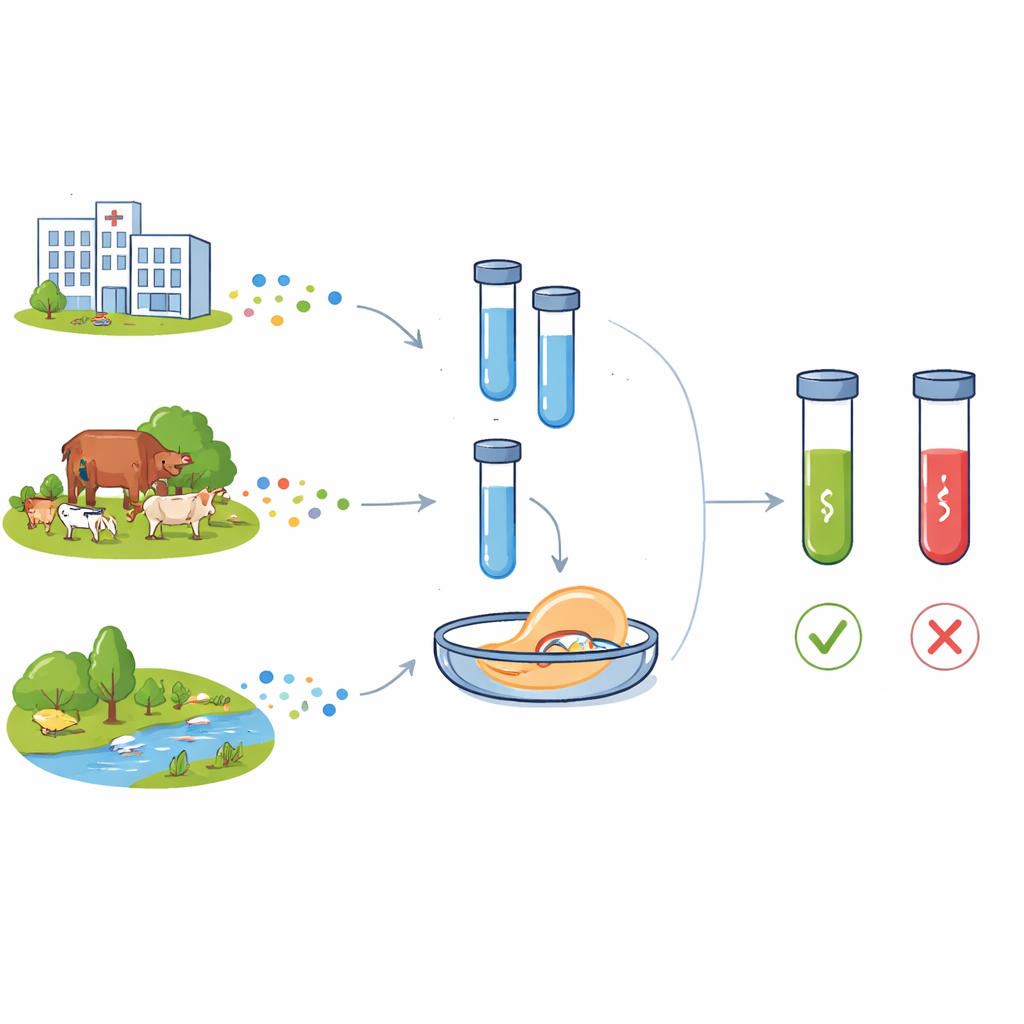
Un problema crescente che oltrepassa le mura degli ospedali
Gli antibiotici moderni hanno trasformato la medicina, trasformando infezioni un tempo letali in malattie trattabili e permettendo interventi chirurgici complessi e cure intensive. Ma l’uso intensivo nella medicina umana, nella produzione zootecnica e lo scarso trattamento dei rifiuti hanno accelerato l’evoluzione e la diffusione della resistenza antimicrobica. Due geni di resistenza sono particolarmente preoccupanti: blaCTX-M-15, che protegge i batteri da un’ampia classe di beta‑lattamici usati in medicina umana, e floR, che difende dagli amfenicoli ampiamente usati negli animali. Entrambi i geni ora compaiono in batteri provenienti da ospedali, comunità, fattorie e acque, spesso spostandosi tra specie su elementi genetici mobili. Un altro elemento genetico, l’integrone di classe 1 (tracciato dal gene intI1), porta frequentemente cluster di geni di resistenza ed è considerato un marcatore dell’impatto umano sugli ecosistemi microbici.
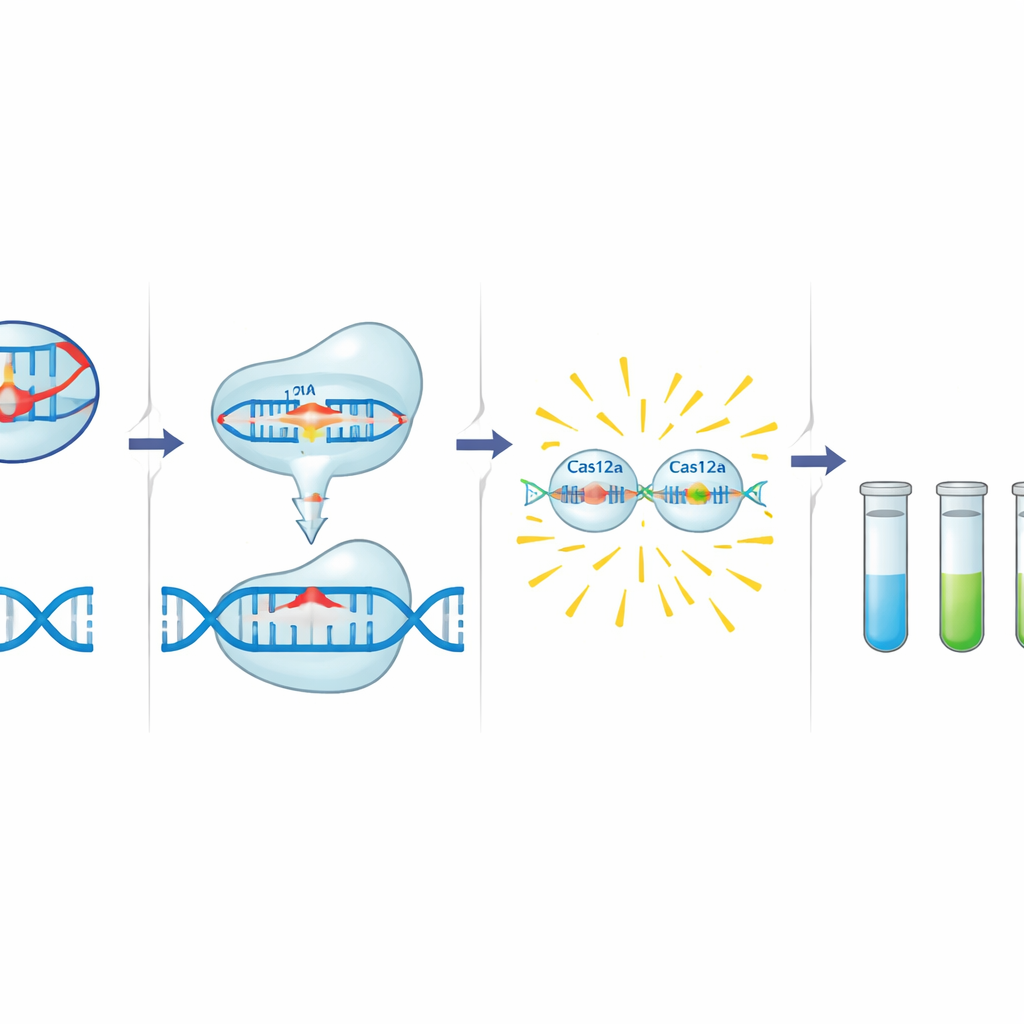
Trasformare CRISPR in un rilevatore di resistenza
La cassetta C12a si basa su Cas12a, un enzima associato a CRISPR che può essere programmato con una breve guida di RNA per riconoscere una specifica sequenza di DNA. Quando Cas12a trova il suo bersaglio vicino a un breve motivo di attivazione, taglia innanzitutto quel DNA e poi comincia a degradare rapidamente il DNA a singolo filamento nelle vicinanze. Gli autori sfruttano questo comportamento aggiungendo una piccola sonda di DNA marcata con un colorante fluorescente e un quencher. In presenza di un gene di resistenza, Cas12a attivato taglia la sonda, rilasciando un segnale luminoso. Prima di questo passo di rilevamento, una reazione PCR standard amplifica una piccola regione del gene target che include sia il motivo di attivazione di Cas12a sia il sito di legame della guida, aggiungendo un secondo livello di specificità. Il gruppo ha progettato e ottimizzato guide e primer per tre target: blaCTX-M-15 (C12abCTX), floR (C12aFLO) e il gene dell’integrasi dell’integrone di classe 1 intI1 (C12aINT).
Quanto è sensibile e affidabile la cassetta?
Per valutare le prestazioni, i ricercatori hanno misurato quanta poca quantità di DNA il sistema poteva rilevare in modo affidabile. Utilizzando frammenti purificati dei geni target, C12abCTX e C12aFLO hanno rilevato concentrazioni fino a 70 e 50 attomolari, rispettivamente—molto al di sotto di quanto si vede semplicemente correndo prodotti PCR su un gel. Quando hanno testato colture batteriche reali, gli assay potevano rilevare circa 77 cellule per millilitro per blaCTX-M-15 e 173 cellule per millilitro per floR. In collezioni di Escherichia coli da campioni fecali pediatrici, i risultati della cassetta C12a hanno corrisposto ai test standard di suscettibilità agli antibiotici e, quando disponibile, al sequenziamento dell’intero genoma: i campioni positivi geneticamente per i geni di resistenza hanno prodotto forti segnali di fluorescenza, mentre i campioni negativi sono rimasti a livelli di fondo.
Collegare i geni di resistenza a un rischio più ampio
Gli autori hanno anche esplorato se i loro strumenti potessero segnalare batteri che portano molteplici tratti di resistenza contemporaneamente. Usando C12aINT, hanno cercato negli stessi isolati il gene dell’integrasi dell’integrone di classe 1. Hanno riscontrato intI1 in quasi tutti i campioni che portavano blaCTX-M-15 o floR. Le analisi genomiche hanno mostrato che questi integroni spesso ospitavano cluster di geni che conferivano resistenza a più famiglie di antibiotici e persino a disinfettanti, sebbene i principali geni target di questo studio fossero di solito localizzati altrove nel genoma. Questo supporta l’idea che il tracciamento di intI1 possa servire come un proxy comodo per la pressione antibiotica guidata dall’uomo e per la resistenza multidroga, pur sottolineando la necessità di testare direttamente specifici geni ad alto rischio.
Dal laboratorio high‑tech al kit da campo
Un punto di forza della cassetta C12a è la sua adattabilità a diverse realtà di laboratorio. In un ambiente completamente attrezzato, le reazioni sono state misurate con un lettore di piastre microtitolatrici, producendo curve quantitative nel tempo. In laboratori più semplici, le stesse reazioni potevano essere osservate con un banale transilluminatore a luce blu, dove solo le provette contenenti geni di resistenza brillavano. Per i test portatili in sito, il team ha sostituito la lettura della fluorescenza con strisce a flusso laterale, simili a un test di gravidanza, che mostravano bande solo quando la reazione CRISPR era stata attivata. In tutti questi allestimenti e tipi di campione—incluso il DNA totale direttamente da feci—la presenza o assenza dei geni target è stata identificata in modo coerente, con solo modestissime perdite di sensibilità nelle modalità a risorse limitate.
Che cosa significa per la lotta alle infezioni resistenti
Nel complesso, i risultati presentano C12a come una piattaforma proof‑of‑concept versatile per monitorare il movimento dei geni di resistenza agli antibiotici tra persone, animali e ambiente. L’approccio non è ancora una diagnostica clinica e rileva il potenziale genetico di resistenza più che come una specifica infezione risponderà a un trattamento. Tuttavia, la sua rapidità, i bassi limiti di rilevamento e la compatibilità sia con strumenti sofisticati sia con semplici strumenti da campo lo rendono un promettente elemento di costruzione per futuri sistemi di sorveglianza. Rendendo più facile individuare i punti caldi di resistenza in ospedali, fattorie e corsi d’acqua, cassette di strumenti basate su CRISPR come C12a potrebbero aiutare funzionari della sanità pubblica e ricercatori a reagire più rapidamente e a progettare strategie più intelligenti per preservare l’efficacia dei nostri antibiotici residui.
Citazione: Vargas-Reyes, M., Alcántara, R., Alfonsi, S. et al. Versatile and portable Cas12a-mediated detection of antibiotic resistance markers. Sci Rep 16, 11509 (2026). https://doi.org/10.1038/s41598-026-42073-2
Parole chiave: resistenza antimicrobica, diagnostica CRISPR, Cas12a, geni di resistenza agli antibiotici, sorveglianza One Health