Clear Sky Science · de
Vielseitiger und portabler Cas12a-vermittelter Nachweis von Antibiotikaresistenz-Markern
Warum das Nachverfolgen unsichtbarer Keime wichtig ist
Antibiotikaresistenz wirkt abstrakt, bis eine routinemäßige Infektion nicht mehr auf Medikamente anspricht. Bakterien, die unsere Wirkstoffe abwehren können, treten nicht nur in Krankenhäusern auf, sondern auch auf Höfen, in Flüssen und im Boden. Um dieser Bedrohung voraus zu bleiben, benötigen Wissenschaftler schnelle, kostengünstige Methoden, um die genetischen Warnzeichen von Resistenz überall zu erkennen. Diese Arbeit beschreibt einen neuen Laborkasten namens C12a, der CRISPR-Genstein-Technologie nutzt, um zentrale Resistenzgene in Bakterien von Menschen, Tieren und der Umwelt nachzuweisen.
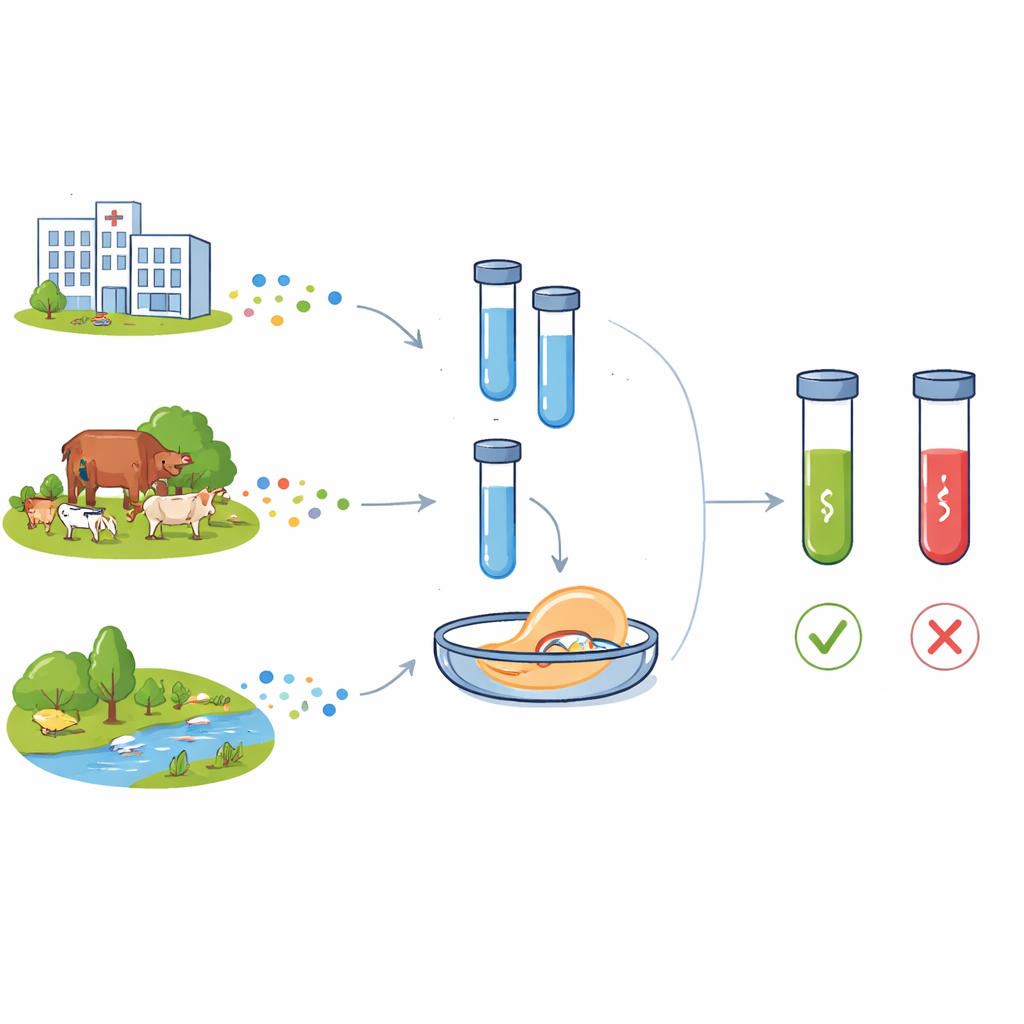
Ein wachsendes Problem, das Krankenhausmauern durchdringt
Moderne Antibiotika haben die Medizin revolutioniert, einst tödliche Infektionen behandelbar gemacht und komplexe Operationen sowie Intensivmedizin ermöglicht. Doch starker Einsatz in der Humanmedizin, der Tierhaltung und unzureichend behandelter Abwässer hat die Evolution und Verbreitung antimikrobieller Resistenz beschleunigt. Zwei Resistenzgene sind besonders besorgniserregend: blaCTX-M-15, das Bakterien vor einer breiten Klasse von Beta-Lactam-Antibiotika schützt, die beim Menschen eingesetzt werden, und floR, das gegen Amphenicole wirkt, die vielfach in der Tiermedizin verwendet werden. Beide Gene treten mittlerweile in Bakterien aus Krankenhäusern, Gemeinschaften, auf Bauernhöfen und in Gewässern auf und bewegen sich oft zwischen Arten auf mobilen genetischen Elementen. Ein weiteres genetisches Element, das Klasse-1-Integron (verfolgt durch das intI1-Gen), trägt häufig Cluster von Resistenzgenen und gilt als Marker für starken menschlichen Einfluss auf mikrobielle Ökosysteme.
CRISPR als Resistenzdetektor nutzen
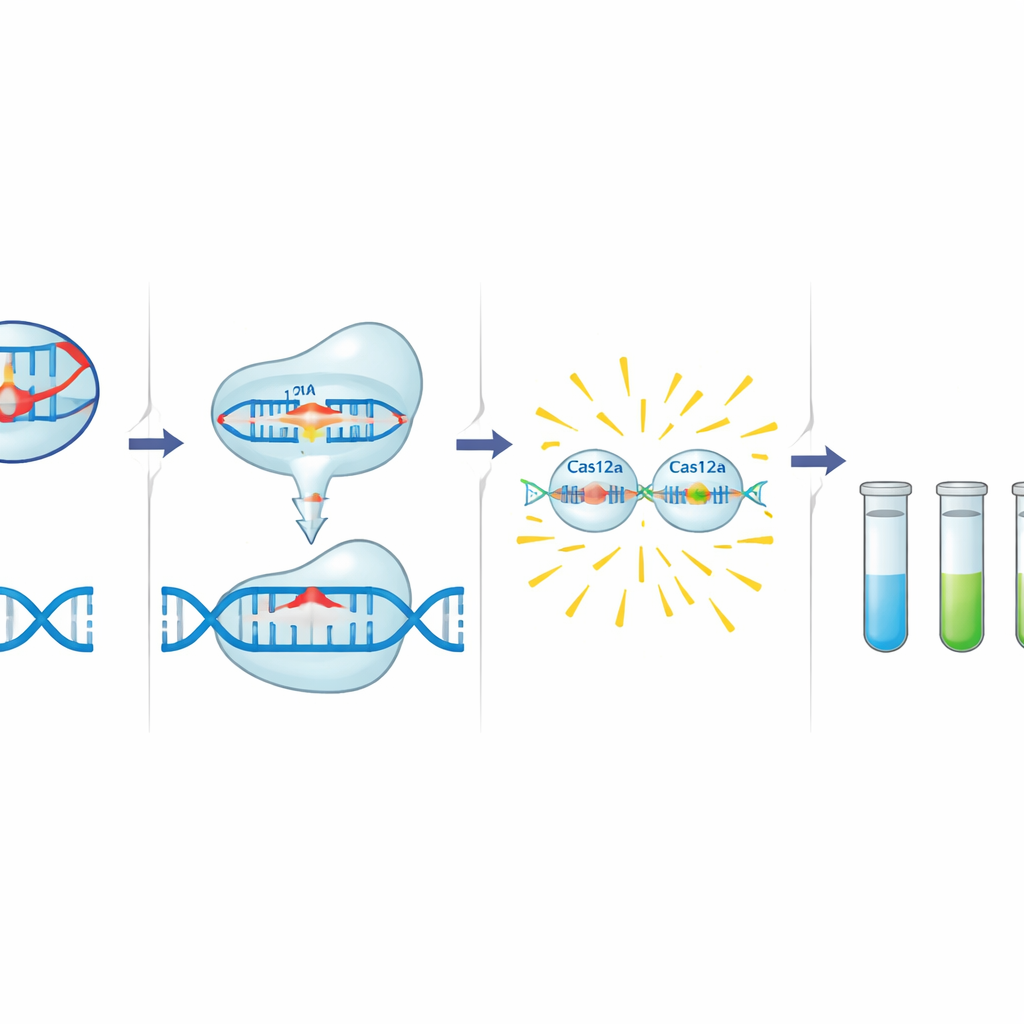
Der C12a-Kasten baut auf Cas12a auf, einem CRISPR-assoziierten Enzym, das mit einer kurzen guide-RNA so programmiert werden kann, dass es eine spezifische DNA-Sequenz erkennt. Findet Cas12a sein Ziel neben einem kurzen Auslösemotiv, schneidet es zunächst diese DNA und beginnt dann, schnell umliegende einzelsträngige DNA zu zerschneiden. Die Autoren nutzen dieses Verhalten, indem sie eine winzige DNA-Sonde mit einem Fluoreszenzfarbstoff und einem Quencher ergänzen. In Anwesenheit eines Resistenzgens schneidet aktiviertes Cas12a die Sonde und setzt ein helles Signal frei. Vor diesem Nachweisschritt verstärkt eine Standard-PCR eine kleine Region des Zielgens, die sowohl das Cas12a-Auslösemotiv als auch die Bindungsstelle der Guide enthält, und fügt so eine zweite Spezifitätsebene hinzu. Das Team entwarf und optimierte Guides und Primer für drei Ziele: blaCTX-M-15 (C12abCTX), floR (C12aFLO) und das Integrase-Gen des Klasse-1-Integrons intI1 (C12aINT).
Wie sensibel und verlässlich ist der Kasten?
Zur Bewertung der Leistung bestimmten die Forschenden, wie wenig DNA das System zuverlässig nachweisen kann. Mit gereinigten Fragmenten der Zielgene detektierten C12abCTX und C12aFLO Konzentrationen von nur 70 bzw. 50 Attomolar — deutlich unterhalb dessen, was allein durch Gel-Analyse von PCR-Produkten sichtbar wäre. Bei Tests mit echten Bakterienkulturen konnten die Assays etwa 77 Zellen pro Milliliter für blaCTX-M-15 und 173 Zellen pro Milliliter für floR nachweisen. In Sammlungen von Escherichia coli aus Stuhlproben von Kindern stimmten die Ergebnisse des C12a-Kastens mit Standard-Tests zur Antibiotikaempfindlichkeit und, wenn verfügbar, mit Ganzgenomsequenzierungen überein: Proben, die genetisch positiv für die Resistenzgene waren, zeigten starke Fluoreszenzsignale, während negative Proben auf Hintergrundniveau blieben.
Resistenzgene mit breiterem Risiko verknüpfen
Die Autoren untersuchten außerdem, ob ihre Werkzeuge Bakterien markieren können, die mehrere Resistenzmerkmale gleichzeitig tragen. Mit C12aINT suchten sie in denselben Isolaten nach dem Integrase-Gen des Klasse-1-Integrons. Sie fanden intI1 in nahezu allen Proben, die entweder blaCTX-M-15 oder floR trugen. Genomanalysen zeigten, dass diese Integrons häufig Cluster von Genen beherbergten, die gegen mehrere Antibiotikaklassen und sogar gegen Desinfektionsmittel wirkten, obwohl die in dieser Studie zentralen Zielgene meist an anderer Stelle im Genom lokalisiert waren. Das stützt die Idee, dass das Tracking von intI1 als praktischer Proxy für vom Menschen verursachten Antibiotikadruck und Multiresistenz dienen kann, unterstreicht jedoch gleichzeitig die Notwendigkeit, gezielt nach spezifischen Hochrisikogenen zu testen.
Vom Hightech-Labor zum Feldkit
Eine zentrale Stärke des C12a-Kastens ist seine Anpassungsfähigkeit an unterschiedliche Laborbedingungen. In voll ausgestatteten Einrichtungen wurden Reaktionen mit einem Mikroplattenleser gemessen, der quantitative Kurven über die Zeit lieferte. In einfacheren Laboren konnten dieselben Reaktionen mit einem einfachen Blaulicht-Transilluminator betrachtet werden, wobei nur Röhrchen mit Resistenzgenen leuchteten. Für tragbare Vor-Ort-Tests ersetzte das Team die Fluoreszenzablesung durch Lateral-Flow-Streifen, ähnlich einem Schwangerschaftstest, die nur dann Banden zeigten, wenn die CRISPR-Reaktion aktiviert worden war. Über diese Aufbauten und Probentypen hinweg — einschließlich Gesamt-DNA direkt aus Kotproben — wurde das Vorhandensein oder Fehlen der Zielgene konsistent identifiziert, mit nur moderaten Sensitivitätseinbußen in ressourcenarmen Modi.
Was das für den Kampf gegen resistente Infektionen bedeutet
Insgesamt stellen die Ergebnisse C12a als vielseitige Proof-of-Concept-Plattform dar, um das Vorkommen von Antibiotikaresistenzgenen bei Menschen, Tieren und in der Umwelt zu beobachten. Der Ansatz ist noch kein klinisches Diagnoseverfahren und detektiert die genetische Potenz zur Resistenz, nicht zwangsläufig, wie eine konkrete Infektion auf eine Behandlung reagieren wird. Dennoch machen seine Geschwindigkeit, die niedrigen Nachweisgrenzen und die Kompatibilität mit sowohl anspruchsvollen Instrumenten als auch einfachen Feldwerkzeugen ihn zu einem vielversprechenden Baustein für künftige Überwachungssysteme. Indem es einfacher wird, Resistenz-Hotspots in Krankenhäusern, auf Höfen und in Gewässern zu erkennen, könnten CRISPR-basierte Werkzeuge wie C12a Gesundheitsbehörden und Forschenden helfen, schneller zu reagieren und klügere Strategien zu entwerfen, um die Wirksamkeit unserer verbleibenden Antibiotika zu erhalten.
Zitation: Vargas-Reyes, M., Alcántara, R., Alfonsi, S. et al. Versatile and portable Cas12a-mediated detection of antibiotic resistance markers. Sci Rep 16, 11509 (2026). https://doi.org/10.1038/s41598-026-42073-2
Schlüsselwörter: antimikrobielle Resistenz, CRISPR-Diagnostik, Cas12a, Antibiotikaresistenz-Gene, One-Health-Überwachung