Clear Sky Science · ar
الكشف المتعدد الاستخدام المحمول بوساطة Cas12a عن علامات مقاومة المضادات الحيوية
لماذا يهم تتبُّع الجراثيم غير المرئية
قد تبدو مقاومة المضادات الحيوية مفهوماً تجريدياً حتى يصبح عدوى روتينية غير مستجيبة للأدوية. البكتيريا القادرة على التحلل من تأثير أدويةنا تظهر ليس فقط في المستشفيات، بل أيضاً في المزارع والأنهار والترب. لمواكبة هذا التهديد، يحتاج العلماء إلى طرق سريعة وميسورة لاكتشاف العلامات الجينية للمقاومة أينما ظهرت. تصف هذه الورقة مجموعة أدوات مخبرية جديدة تُسمى C12a تستخدم تقنية القص الجيني CRISPR لاكتشاف جينات المقاومة الرئيسية في بكتيريا مصدرها البشر والحيوانات والبيئة.
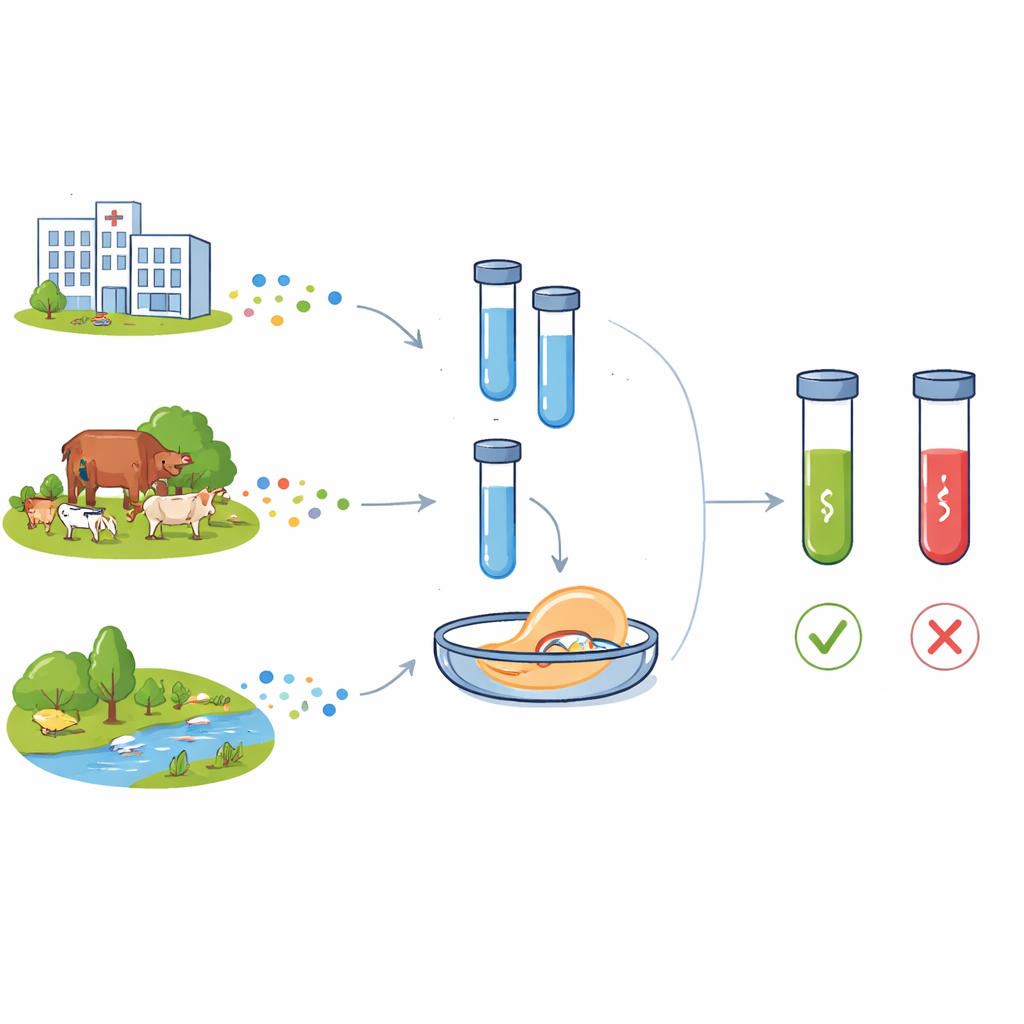
مشكلة متنامية تتجاوز جدران المستشفى
حوّلت المضادات الحيوية الحديثة الطب، فحوّلت عدوى كانت مميتة إلى أمراض قابلة للعلاج ومكنت إجراء عمليات جراحية معقدة ورعاية مركزة. لكن الاستخدام المكثف في الطب البشري، وإنتاج الماشية، والمخلفات المعالجة بشكل سيئ سرّع تطور وانتشار مقاومة المضادات الحيوية. هناك جينان للمقاومة يثيران قلقاً خاصاً: blaCTX-M-15، الذي يحمي البكتيريا من فئة واسعة من مضادات بيتا‑لاكتام المستخدمة لدى البشر، وfloR، الذي يقي من أدوية الأمفينيكول المستخدمة على نطاق واسع في الحيوانات. كلا الجينين يظهران الآن في بكتيريا من المستشفيات والمجتمعات والمزارع والمياه، وغالباً ما ينتقلان بين الأنواع عبر عناصر جينية متنقلة. عنصر جيني آخر، التكاملون من الفئة 1 (الذي يتتبع عبر جين intI1)، يحمل في كثير من الأحيان عنقوداً من جينات المقاومة ويُعتبر علامة على التأثير البشري القوي على نظم الميكروبات البيئية.
تحويل CRISPR إلى كاشف للمقاومة
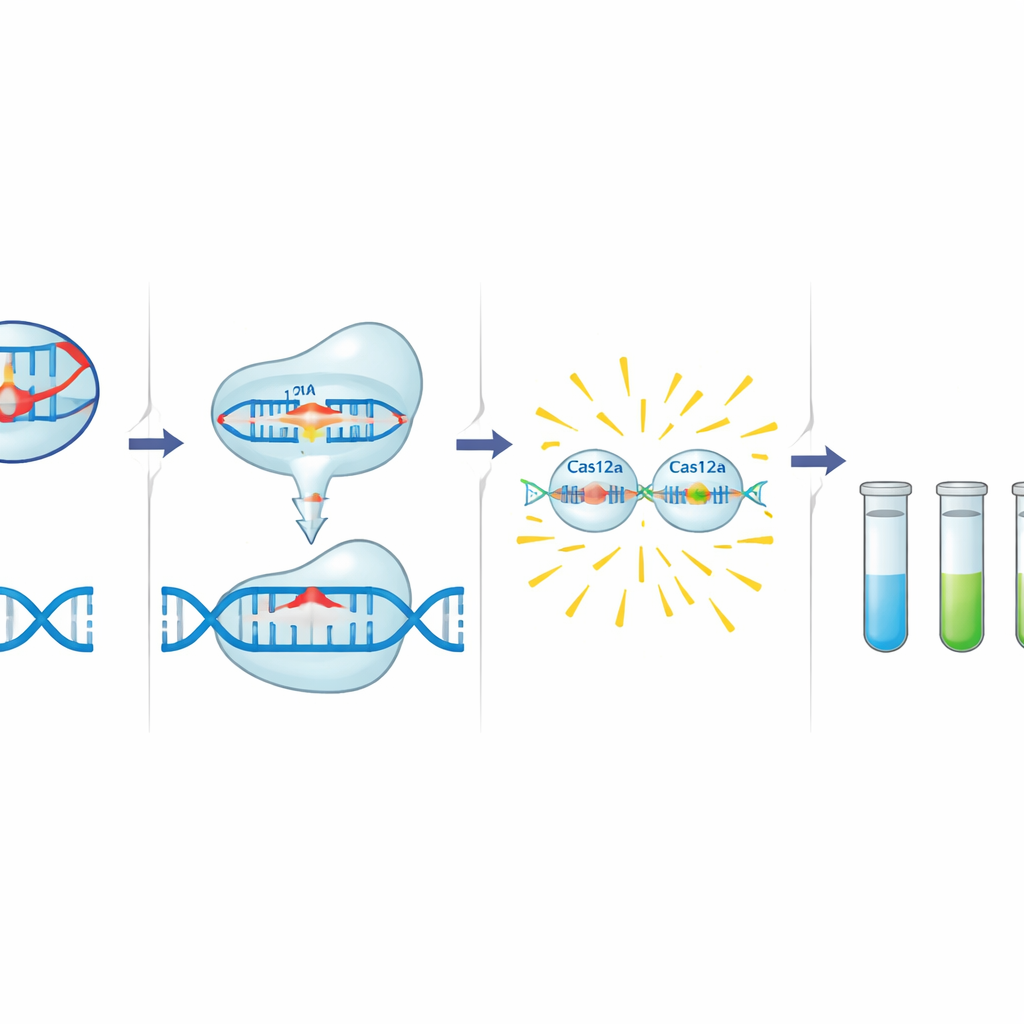
تبني مجموعة أدوات C12a على Cas12a، إنزيم مرتبط بنظام CRISPR يمكن برمجته بإرشادRNAقصير للتعرُّف على تسلسل DNA محدد. عندما يجد Cas12a هدفه بجانب نمط محفز قصير، يقطع ذلك الـDNA أولاً ثم يبدأ بسرعة في تقطيع الـDNA أحادي السلسلة القريب. يستغل المؤلفون هذا السلوك بإضافة مجس DNA صغير موسوم بصبغة فلورية وكاشف. في وجود جين مقاومة، يقطع Cas12a المنشط المجس، مطلقاً إشارة ساطعة. قبل خطوة الكشف هذه، تضاعف تفاعل PCR القياسي منطقة صغيرة من الجين المستهدف تتضمن كلاً من نمط المحفز لمِحرِّك Cas12a وموقع ارتباط الإرشاد، مضيفاً طبقة ثانية من التحديد. صممت الفريق وحسّن أدلة (guides) ومقادير بادئات (primers) لثلاثة أهداف: blaCTX-M-15 (C12abCTX)، floR (C12aFLO)، وجين إنتيغراز التكاملون من الفئة 1 intI1 (C12aINT).
ما مدى حساسية وموثوقية هذه الأدوات؟
لتقييم الأداء، قاس الباحثون أدنى كمية من الـDNA التي يمكن للنظام الكشف عنها بشكل موثوق. باستخدام شظايا منقاة من الجينات المستهدفة، كشفت C12abCTX وC12aFLO عن تراكيز منخفضة تصل إلى 70 و50 أتومولار على التوالي—وهما أقل بكثير مما يمكن رؤيته ببساطة عبر تشغيل منتجات PCR على هلام. عند اختبارهم لزراعات بكتيرية حقيقية، استطاعت الفحوصات كشف نحو 77 خلية/مل لكل من blaCTX-M-15 و173 خلية/مل لـfloR. في مجموعات من Escherichia coli المأخوذة من عينات براز أطفال، طابقت نتائج مجموعة C12a اختبارات الحساسية التقليدية للمضادات الحيوية و، حيث توفرت، تسلسل الجينوم الكامل: أعطت العينات الإيجابية جينياً للإصلاح إشارات فلورية قوية، بينما بقيت العينات السلبية عند مستويات الخلفية.
ربط جينات المقاومة بالمخاطر الأوسع
استكشف المؤلفون أيضاً ما إذا كانت أدواتهم تستطيع الإشارة إلى البكتيريا التي تحمل صفات مقاومة متعددة في آن واحد. باستخدام C12aINT، بحثوا نفس العزلات عن جين إنتيغراز التكاملون من الفئة 1. وجدوا intI1 في كل العينات تقريباً التي حملت إما blaCTX-M-15 أو floR. أظهرت تحليلات الجينوم أن هذه التكاملونات غالباً ما احتوت عنقوداً من الجينات التي تمنح مقاومة لعائلات مضادات حيوية متعددة وحتى لمطهّرات، رغم أن الجينات الهدف الرئيسية لهذه الدراسة كانت عادة موضوعة في أماكن أخرى من الجينوم. يدعم هذا الفرضية القائلة إن تتبع intI1 يمكن أن يعمل كبديل عملي لمؤشر الضغط البشري على المضادات والمقاومة متعددة الأدوية، بينما يؤكد أيضاً الحاجة إلى اختبار مباشر للجينات عالية الخطورة المحددة.
من المختبر عالي التقنية إلى طقم ميداني
قوة رئيسية في مجموعة أدوات C12a هي قابليتها للتكيّف مع واقع مختبرات مختلفة. في بيئة مجهزة بالكامل، قيسّت التفاعلات بواسطة قارئ ألواح دقيقات، منتجة منحنيات كمية بمرور الوقت. في مختبرات أبسط، يمكن مشاهدة نفس التفاعلات بمُنَوِّر أشعة زرقاء أساسي، حيث تتوهج الأنابيب التي تحتوي على جينات مقاومة فقط. للاختبارات المحمولة الميدانية، استبدل الفريق القراءة الفلورية بشرائط التدفق الجانبي، شبيهة بصيغة اختبار الحمل، والتي أظهرت خطوطاً فقط عندما يتم تفعيل تفاعل CRISPR. عبر هذه الإعدادات وأنواع العينات—بما في ذلك الحمض النووي الكلي مباشرة من البراز—تم تحديد وجود أو غياب الجينات المستهدفة بثبات، مع خسائر متواضعة فقط في الحساسية في أوضاع الموارد المحدودة.
ماذا يعني هذا في مكافحة العدوى المقاومة
تقدّم النتائج معاً C12a كمنصة إثبات مفهوم مرنة لمراقبة جينات مقاومة المضادات الحيوية أثناء تنقّلها بين البشر والحيوانات والبيئة. النهج ليس بعد تشخيصاً إكلينيكياً، وهو يكشف عن الإمكانية الجينية للمقاومة بدل كيفية استجابة عدوى محددة للعلاج. ومع ذلك، فإن سرعته وحدود كشفه المنخفضة وتوافقه مع كل من الآلات المتقدمة والأدوات الميدانية البسيطة تجعله لبنة واعدة لأنظمة المراقبة المستقبلية. بجعل اكتشاف بؤر المقاومة في المستشفيات والمزارع والمجاري المائية أكثر سهولة، قد تساعد مجموعات أدوات CRISPR مثل C12a مسؤولي الصحة العامة والباحثين على الاستجابة بسرعة وتصميم استراتيجيات أذكى للحفاظ على فعالية مضاداتنا المتبقية.
الاستشهاد: Vargas-Reyes, M., Alcántara, R., Alfonsi, S. et al. Versatile and portable Cas12a-mediated detection of antibiotic resistance markers. Sci Rep 16, 11509 (2026). https://doi.org/10.1038/s41598-026-42073-2
الكلمات المفتاحية: مقاومة الميكروبات للمضادات الحيوية, تشخيصات CRISPR, Cas12a, جينات مقاومة المضادات الحيوية, مراقبة نهج الصحة الواحدة